Mikro- ja megamaailma füüsika
- 1 Aine ehituse alused
- Sissejuhatus
- 1.1 Molekulid. TahkisLisamaterjalidLisaülesanded
- 1.2 Gaas ja vedelikLisamaterjalidLisaülesanded
- 1.3 ÕhuniiskusLisamaterjalidLisaülesanded
- 1.4 Kastepunkt. Ilm ja kliimaLisamaterjalidLisaülesanded
- 1.5 IlmaennustusLisamaterjalidLisaülesanded
- 1.6 HügromeeterLisamaterjalidLisaülesanded
- 1.7 PindpinevusLisamaterjalidLisaülesanded
- 1.8 Tilk ja mullLisamaterjalidLisaülesanded
- 1.9 FaasidiagrammLisamaterjalidLisaülesanded
- 2 Mikromaailma füüsika
- Raadiumitüdrukud
- 2.1 AatomLisamaterjalidLisaülesanded
- 2.2 KvantmehaanikaLisamaterjalidLisaülesanded
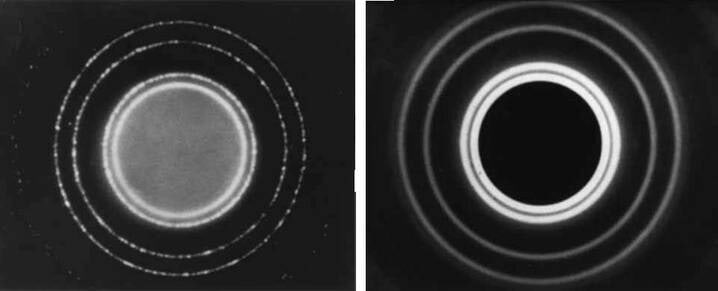
- 2.3 Elektronide difraktsioonLisamaterjalidLisaülesanded
- 2.4 MääramatusseosLisamaterjalidLisaülesanded
- 2.5 AatomituumLisamaterjalidLisaülesanded
- 2.6 TuumareaktsioonLisamaterjalidLisaülesanded
- 2.7 TuumarelvLisamaterjalidLisaülesanded
- 2.8 TuumaenergeetikaLisamaterjalidLisaülesanded
- 2.9 Radioaktiivsus ja kiirgusKüsimusedLisamaterjalid
- 3 Megamaailma füüsika
- SissejuhatusLisamaterjalidLisaülesanded
- 3.1 AstronoomiaLisamaterjalidLisaülesanded
- 3.2 TaevasLisamaterjalidLisaülesanded
- 3.3 Tähtkujud taevakaartidelLisamaterjalidLisaülesanded
- 3.4 TaevamehaanikastLisamaterjalidLisaülesanded
- 3.5 Kalender ja kellLisamaterjalidLisaülesanded
- 3.6 PäikesesüsteemLisamaterjalidLisaülesanded
- 3.7 Päikesesüsteemi väikekehadLisamaterjalidLisaülesanded
- 3.8 Kosmoselennud ja –uuringudLisamaterjalidLisaülesanded
- 3.9 Päike ja teised tähedLisamaterjalidLisaülesanded
- 3.10 Galaktikad ja UniversumLisamaterjalidLisaülesanded
- 3.11 Kust tuli Kuu?LisamaterjalidLisaülesanded
Antoine Lavosier tegi 1772. aastal hirmkalli eksperimendi. Ta koondas päikesekiired hapniku keskkonda paigutatud teemandile ja põletas selle ära. Selle reaktsiooni ainsaks saaduseks oli süsihappegaas. 18. sajandi lõpuaastateks oli katset nii palju korratud ja täiustatud, et Smithson Tennant võis teatada tavalise söe ja teemandi keemilisest samasusest. Põlemisel andsid võrdsed söe, tahma, grafiidi ja teemandi kogused võrdse mahu süsihappegaasi. Vaadates või katsudes korraga briljanti ja söetükki, tundus nende keemilise identsuse idee äärmiselt kahtlane.
Ometi leppisid teadlased pikapeale tõsiasjaga, et teemant ei sisalda lisaks süsinikule mingeid tundmatuid elemente. Sellega oli lahti tee kunstteemantide tootmiseks. Kohe selle kallale asutigi ja vähem kui saja aasta pärast andsid esimesed leiutajad teda, et grafiiti on võimalik muuta teemandiks mitmel erineval moel. Kahjuks korduskatsed ei õnnestunud ja tehisteemantide tegeliku tootmiseni kulus veel aastakümneid. Lisaks teemantide tootmise tehnoloogiale kuuluvad 20. sajandi saavutuste hulka süsiniku teisendid, mille olemasolust ja tootmise võimalusest ei osatud unistadagi: fullereenid, süsiniknanotorud, grafeen jt. Millised on need aine ehituse saladused, mis tuli teadlastel lahendada, enne kui teemandikaevandamise kõrvale tekkis teemanditootmine ja süsinikmaterjalide nanotehnoloogia?
Aine kolm olekut – tahke, vedel ja gaasiline - on tuttavad meile kõigile. Kuumutamisel muutuvad tahked ained vedelaks, edasisel kuumutamisel lähevad keema ja aurustuvad. Üldiselt see nii ongi, aga isegi igapäevaste loodusnähtuste jälgimisel võib märgata teatud kõrvalekaldumist sellest lihtsast reeglist. Vesi, lihtne, aga väga eriline aine, käitub selles mõttes väga viisakalt. Tavapärastel temperatuuridel esineb vesi tõesti kolmes olekus. Temperatuuri tõusu järjekorras: jää, vesi ja veeaur. Jääd ja vedelat vett teame kõik hästi, auruga on veidi keerulisem. Kuna veeaur on nähtamatu, st vaatlemisel õhuga täiesti sarnane, siis me kipume aurustumisega kaasnevat udu (väikeseid veepiisku) tihti veeauruks nimetama. See pole küll terminoloogiliselt ega sisuliselt õige, aga „kus udu, seal auru”, nii et teatud seos on siin olemas. Üks kõrvalekalle lihtsast kolme oleku mudelist on see, et vesi aurustub ka ilma keemiseta. Kui veeklaas lauale jätta, on see olenevalt tingimustest mõne päeva või mõne nädalaga tühi. Vähe sellest, jää võib ka ilma vedelaks muutumata „ära aurata”. Kui märg pesu talvekülmaga nöörile riputada, siis kuivab see tuule käes ära vaatamata sellele, et algul kõvaks külmub. Seda nähtust nimetatakse sublimeerumiseks. Jääkristallide sublimeerumine ei ole küll nii igapäevane nähtus kui vedela vee aurustumine, aga hea tahtmise juures täiesti märgatav ja mõõdetav. Paistab, et isegi lihtsate ainete korral tekib küsimusi. Kes on näinud vedelat süsihappegaasi või gaasilist süsinikku? Miks on ainete sulamis- ja keemistemperatuurid nii erinevad?
Aine oleku ja ülemineku ühest olekust teise määravad suures osas molekulaarjõud. Nagu me teame, hoiavad aatomeid molekulides keemilised sidemed. Aatomitevaheliste sidemete pikkused ja nendevahelised nurgad molekulis panevad olulises osas paika aine keemilised ja füüsikalised omadused. Keemilised sidemed, mida põhjustab laetud osakeste vaheline elektromagnetiline vastastikmõju, on üsna tugevad. Lisaks toimib aatomite ja molekulide vahel veel teisi, palju nõrgemaid jõude.
Molekulid kipuvad omavahel tõmbuma, kui nad üksteisele piisavalt lähedale satuvad. Tõmbumise põhjuseks on molekulide polaarsus. Aatomid on küll tervikuna elektriliselt neutraalsed, aga molekuli moodustades ei jaga nad elektrone ühtlaselt. Seepärast on paljud molekulid polaarsed, ühest kohast positiivse, teisest negatiivse laenguga (joonis 1.1.1.). Isegi molekulides, kus laengud on jagatud ühtlaselt, võivad elektronid ajutiselt ümber paikneda. Sellest tekib molekulide ajutine polariseerumine. Sama molekuli erinevate aatomite juures indutseeruvad erinimelised laengud, mille kaudu molekulid üksteist mõjutavad. Neid molekulidevahelisi, suhteliselt nõrku mõjusid nimetatakse van der Waalsi jõududeks.
Vesinikside. Ühendites, kus vesinik on seotud hapniku, lämmastiku või fluoriga (rühmad -OH, -NH ja -FH), on vesinikul positiivne osalaeng ja sideme teisel poolel negatiivne osalaeng. Selliste molekulide vesinikule kontsentreerunud positiivne laeng moodustab täiendavaid sidemeid teiste molekulide negatiivselt laetud aatomitega. Neid sidemeid kutsutakse vesiniksidemeteks. Vesiniksidemed võivad tekkida molekulide vahel. Näiteks moodustavad vee molekulid omavahel palju vesiniksidemeid, mis ongi suures osas vee väga eriliste omaduste põhjuseks. Vesiniksidemed võivad tekkida ka suurte molekulide sees, hoides biomolekule vajalikul viisil kokkupakituna. Vesiniksidemed on piisavalt tugevad, et molekule üksteisega seotuna hoida, samas piisavalt nõrgad, et elukeskkonna tavapärastel temperatuuridel katkeda. Sel moel on vesiniksidemed bionähtustes väga olulised. Vesiniksidet võib vaadelda kui teatud vahepealset nähtust molekulaarjõudude ja keemilise sideme vahel.
Hollandi füüsikateoreetiku, Amsterdami ülikooli esimese füüsikaprofessori Johannes Diderik van der Waalsi põhihuvi oli suunatud termodünaamikale. Tema nime kannavad peale jõudude veel reaalgaase kirjeldav van der Waalsi võrrand (Nobeli preemia 1910), mitmest molekulist koosnevad, molekulidevaheliste jõududega seotud van der Waalsi molekulid ja aatomite mõõtmeid kirjeldavad van der Waalsi raadiused. Eraldi väärib mainimist tema kapillaarsuse (ptk 1.7.) termodünaamiline teooria 1893. aastast, mis tekitas vaidlusi, sest molekulide ja soojusliikumise olemasolu ei olnud selleks ajaks veel üldiselt tunnustatud.
Aine kogust (üht tükki ainet), mis on kogu tervikuna samade füüsikaliste omadustega, nimetatakse faasiks. Vaatleme näiteks klaasitäit vett jääkuubikutega. Kuigi jää ja vesi on keemiliselt sama aine, on nende füüsikalised omadused ilmselt erinevad. Jää ja vesi on omakorda klaasis. Jääkuubikutega vees on: A) jääkuubikud, tahke faas; B) vesi, vedel faas, C) klaas, teine tahke faas, D) kui see kõik asub õhus, tuleb juurde veel gaasiline faas. Kõikide faaside vahel on piirpinnad, kus õhukeses kihis toimuvad pinnanähtused. Selge, et vee ja jää pinnakihis toimub sulamine, vee ja õhu piirpinnal aurustumine. Samas võib jää ja vee piirpinnal toimuda hoopis tahkumine, kui temperatuur on piisavalt madal. Vee ja õhu piirpinnal võib toimuda lisaks aurustumisele ka kondenseerumine ja gaaside lahustumine. Ka klaasi ja vee või klaasi ja õhu piirpinnal toimuvad teatud nähtused. Näiteks lahustuvad mõned klaasi komponendid vähesel määral vees. Kui vesi ei ole päris puhas, adsorbeeruvad lahustunud ained klaasile.
Kõigis neis näidetes on faasidevaheline piirpind ühtlasi erinevas olekus ainete piirpinnaks. Kuid esineb ka seda, et erinevad faasid moodustuvad samast ainest samas olekus. Kõige tuntum mitme tahke faasiga aine on süsinik, seda eelkõige tänu oma kahe loodusliku teisendi, grafiidi ja teemandi täiesti erinevatele füüsikalistele omadustele (ptk Faasidiagramm). Veelgi lisavad süsinikule kuulsust kunstlikult loodud teisendid (uued faasid), fullereen, grafeen jt.
Tahkete faaside eripära on kuju. Tahked kehad avaldavad vastupanu deformatsioonile, vedelikud ja gaasid seda ei tee. Samas on vedelatel ja tahketel faasidel ka ühiseid omadusi, näiteks kindel ruumala, mida ei ole jälle gaasidel. Seepärast kannavad tahked ja vedelad faasid ühist nimetust, kondensaine. Gaaside ja vedelike ühine omadus, kindla kuju puudumine, tingib nende voolavuse. Seepärast on nende ühine nimetus voolis. Esineb ained ja ainete segusid, kus selline lihtne sildistamine ei tööta kuigi hästi. Näiteks väga viskoossed vedelikud ja puisteained kipuvad tihti käituma kuidagi vahepealselt.
Aatomid, keemilised sidemed ja molekulide struktuur määravad ainete omadusi. Samas on paljud nähtused ja protsessid, mis ainetega toimuvad (olekute muutused, lahustumine, osmoos, pindpinevus), juhitud molekulaarjõududest. Molekulaarnähtuse hulgas on erilisel kohal see, mis toimub faaside piirpinnal, aine või faasi pinnakihis. Tuntuimad pinnanähtused on märgamine ja kapillaarsus, mis seostuvad vee ja teiste vedelike pinnakihi erilise omaduse, pindpinevusega (ptk Pindpinevus).
Mainime veel, et sõnal „faas“ on muidki tähendusi. Võnkumiste ja lainete, ka elektromagnetlainete, kirjeldamisel, astronoomias, meditsiinis, bioloogias ja materjalide töötlemisel on „faasil“ hoopis teised tähendused.
Esmapilgul tundub sulamine olevat lihtne nähtus. Vaatame, kuidas jääkuubikud vees sulavad. Jää sulamistemperatuur ja vee tahkumistemperatuur (jäätumistemperatuur) on 0°C. Samuti on jäätükkidega vee temperatuur null kraadi. Igapäevaselt tähendab see, et kui nullkraadine jäätükkidega veeklaas jätta lauale tasapisi soojenema, siis nii kaua, kuni jääd veel on, ei lähe jäätükkide vahel olev vesi soojemaks. Soojushulk, mis soojast toaõhust vette ja jäässe üle kandub, kulub jää sulatamiseks, mitte vee soojendamiseks.
Tahkes olekus (näiteks kristallides) on molekulide (aatomite, ioonide) asukohad üksteise suhtes määratud keemiliste sidemete pikkuste ja sidemete asenditega. Öeldakse, et selline tahkis on atomaatselt korrastatud struktuuriga. Samas on molekulidele iseloomulik pidev, korrapäratu, kaootiline, juhusliku loomuga liikumine, mida nimetatakse soojusliikumiseks. Nii ei ole ka tahkes olekus molekulid omal kohal päris paigal. Piltlikult võib seda kujutada kui aatomite juhuslikku rabelemist talle määratud koha ümber. Molekule ja kristallvõret joonistades või vastavaid mudeleid kokku pannes kujutatakse aatomeid ainult lihtsuse mõttes paigalseisvate kerakestena. Aatomitevahelise kauguse määrab siin ära potentsiaalse energia miinimumi printsiip. Aatomid asuvad üksteisest keskmiselt sellisel kaugusel, kus neil on „kasulik” olla, kus nendevahelise seose energia on kõige väiksem (joonis 1.1.3.).
Igapäevaelukogemustest on hästi teada, et sulatamiseks on vaja energiat kulutada, st ainet on vaja soojendada. Energia jäävuse seadus ütleb, et ainete tahkumisel peab sama suur kogus energiat eralduma. Näiteks 1 kg alumiiniumi sulatamisel tuleb kõigi aatomite potentsiaaliaugust (joonis 1.1.3.) väljatoomiseks teha kokku 321 kJ tööd. Seda kokkulepitud ainekoguse (ühikulise massi) sulatamiseks kuluvat soojushulka nimetatakse sulamissoojuseks. Kui sulaalumiinium vormi valatakse ja tahkuda lastakse, siis lähevad aatomid jälle oma minimaalse energiaga kohtadele tagasi (kaugus üksteisest r0) ja sulatamiseks kulutatud soojushulk eraldub. Tahkumisel eralduvat soojust on võrreldes sulamiseks kuluvaga raskem märgata. Tundub üsna loogiline küsida, kas tõesti kinnikülmuv järv soojendab jääkristallide moodustumisel vabaneva energia arvel iseennast ja ilma. Kuigi see võib intuitiivselt paista veidi kahtlane, siis just nii see ongi. Veekogud saavad külmuda ainult siis, kui õhk on piisavalt külm, et tahkumisel eralduv soojushulk vastu võtta ja ära kanda.
Selline sulamist kirjeldav molekulaarmudel on õige mitmetel lihtsatel juhtudel, aga tegelikult on palju aineid ja suur hulk nähtusi, kus sulamise ja tahkumise kirjeldamine on hoopis keerulisem.
Näiteid pole vaja kaugelt otsida. Mitmed ained esinevad ainult gaasi ja tahkisena. Süsihappegaas, nagu nimetuski ütleb, on tuntud enamasti gaasina. Tahket süsihappegaasi on võimalik valmistada nii süsihappelume kui kuiva jääna, aga vaevalt on keegi näinud vedelat süsihappegaasi. Kuiv jää normaalrõhul ei sula, vaid muutub gaasiliseks ilma vahepealse vedela olekuta ehk sublimeerub (ptk Faasidiagramm).
Segude (näiteks sulamite) sulamisel ja eriti tahkumisel sõltub palju komponentide vahekorrast ja temperatuurimuutuse kiirusest. Metallide tehnoloogias on teadmised neist protsessidest väga olulised. Näitena meenutame, kuidas muudab raua tahkumist ja saadud materjali omadusi mõneprotsendiline süsinikusisaldus (teras, malm) või jahtumisrežiim (karastamine).
Kuigi üldiselt on sulamis- ja tahkumistemperatuur võrdsed, on võimalik ka vedelike allajahtumine. Näiteks puhta vee temperatuur võib langeda alla null kraadi, ilma et jääkristallid tekiksid. Paistab, et jäätumine ei „suuda otsustada”, kuhu tekib esimene kristallike. Sellise vedeliku paneb kiiresti tahkuma vähimgi häirimine, nt loksutamine või lisandid. Samamoodi võib aur alla jahtuda. See juhtub tihti veeauruga atmosfääris ja on oluline nähtus pilvede tekkimisel (ptk Kastepunkt. Ilm ja kliima).
Kristalsetel ainetel on olemas kindel sulamistemperatuur. Aga on olemas hulk amorfseid aineid, mis muutuvad vedelikuks teatud temperatuurivahemikus ja ka nende tahkumine ei sarnane sugugi vee jäätumisega. Näidetena väärivad eelkõige nimetamist pigi, vaha, termoplastilised polümeerid ja klaas. Klaas on nende hulgas nii eriline ja oluline, et sellele sarnaseid, molekulaarstruktuurilt korrastamata ja seepärast ka täpse sulamistemperatuurita aineid nimetataksegi tihti klaasideks. Kuumutamisel muutuvad klaasid algul pehmeks ja temperatuuri tõusuga viskoossus väheneb, kuni saabub üsna tavalise vedeliku sarnane olek. Seepärast võib öelda, et klaasidel sulamistemperatuuri ei ole.
Tuleb siiski märkida, et on mitmeid omadusi (soojuspaisumine, erisoojus), mis klaasi sulatamisel muutuvad palju järsemalt kui viskoossus. Temperatuuri, mille juures mingi füüsikaline omadus järsult muutub, nimetatakse siirdetemperatuuriks.
Olek ei pea siirdetemperatuuril järsult muutuma. Nagu me kõik klaasi näite varal teame, on amorfsed materjalid siirdetemperatuurist oluliselt madalamal temperatuuril vägagi kristalsete ainete sarnased. Külma ilmaga võib pigi haamriga kildudeks lüüa, kuigi kuumal suvepäeval kipub ta laiali valguma. Mitmed igapäevastel temperatuuridel elastsed või plastilised ained muutuvad külma käes ootamatult hapraks. Näiteid võib leida nii igapäevaelust kui kosmosetehnikast.
Klaasi amorfsete omaduste tõestuseks kirjeldatakse tihti väga vanade aknaklaaside alumise serva paksemaks vajumist. Kuna klaasil on omadusi, mis lubavad teda pidada mitte kristalseks aineks, vaid väga suure viskoossusega vedelikuks, siis sadade aastatega võiksid aknaklaasid tasapisi allapoole voolata ja alt paksemaks muutuda. Tegelikult ei ole selle nähtuse esinemise kohta selgeid tõendeid. Vanad aknaklaasid on tõepoolest enamasti alt paksemad. Samas ei ole kusagil märgatud raamidest väljavajumist ja muid nähtusi, mis peaksid ilmnema viskoosse vedeliku valgumisel. Miks on siis keskaegsed kirikuakende klaasid alumisest servast paksemad?
Erinevad klaasisordid on erineva keemilise koostisega ja nende füüsikalised omadused on erinevad. Klaasi pehmenemise temperatuurivahemik on sorditi erinev. Kuumuskindlad sordid ja optiline klaas on selles mõttes sarnasemad kristallidega, akna- ja pudeliklaas käitub laiemas temperatuurivahemikus viskoosse vedelikuna. Tootmise ja klaasikunsti, eriti klaasipuhumise jaoks on see omadus oluline. Näiteks kroonklaasi meetodi etappideks olid suure anuma puhumine, lahtilõikamine ja selle klaaskettaks vormimine. Peaaegu vedelast klaasist puhutud pudeli põhi on lahti lõigatud ja kiire pöörlemise tulemusel venib ikka veel poolpehme klaas üha suuremaks, tasasemaks ja õhemaks kettaks. Tehnoloogia ja klaasisordi nimi tulevad sellest, et pudelist siledaks kettaks venimisel on toorik vahepeal kroonikujuline. Saadud ketas lõigatakse pärast ettevaatlikku jahutamist tahvliteks. Seejuures on hea, kui klaas püsib laiemas temperatuurivahemikus pehme ja vormitav. Saadakse üsna suured klaaskettad, mis on paratamatult keskelt paksemad kui servast. Nende tahvliteks lõikamisel saadud aknaklaasi üks serv või nurk jääb paksem. Tuleb tunnistada, et me ei tea, miks ehitajad paigaldasid klaasi alati või vähemalt valdavalt paksema servaga allapoole, aga on üsna selge, et just nii nad tegid. Ka kõigis muudes kohtades peale akende, kus vana klaasi on leitud, ei ole märgata voolamisega sarnanevat deformatsiooni. Näiteks maa seest või varemete alt välja kaevatud klaasesemed ei ole sajanditega kuidagi pinnase või kivide survele järgi andnud. Klaas on igapäevase õhutemperatuuri juures ikkagi lihtsalt tahke aine.
Sulamistemperatuuri määramiseks on mõistlik võtta võimalikult väike ainekogus (peenikeses torus, õhukese kihina) ja lasta temperatuuril aeglaselt tõusta, jälgides samal ajal ümbritseva keskkonna temperatuuri. Sulamise hetke on kerge märgata, muutus on selgelt näha. Samuti on võimalik mitmesuguste anduritega registreerida aine optiliste või soojuslike omaduste muutust sulamise hetkel ja salvestada samal hetkel temperatuurinäit.
Lihtsas sulamistemperatuuri määramise seadmes on elavhõbetermomeetri reservuaari külge on kinnitatud peenikeses klaasist torukeses (d≈1 mm) peenestatud aine. Termomeeter on pannakse õliga täidetud anumasse, Thiele katseklaasi, mida gaasipõletiga aeglaselt kuumutatakse. Sulamistemperatuuri vaadatakse hetkel, kui aineproov muutub läbipaistvaks, st vedelaks.
Aine olekud, keemilised sidemed, molekulaarijõud
Aine olekud ja olekumuutused on määratud keemiliste sidemete ja molekulaarjõudude iseloomuga.
Tahkis
Tahkistes (tahketes kehades) on aineosakesed tihedalt üksteise kõrval. Tahkes olekus on aineosakeste kineetiline energia palju väiksem kui osakeste vahel mõjuv tõmbejõudude potentsiaalne energia. Tahkiste eripära ilmneb deformeerimisel: ainult tahkised avaldavad deformeerimisele vastupanu. Vedelike ja tahkiste ühiseks omaduseks on ruumala jäävus, mispärast neid nimetatakse kondensaineteks.
Kõik me oleme kunagi oodanud, et vesi kannus keema läheks. Teame, et temperatuuri tõusuga kaasneb kõigepealt kiirem aurustumine, molekulid hakkavad veepinnalt üha rohkem lahkuma. Muidugi aurustub veidike ka külm vesi – kuna molekulide soojusliikumise kiirused on erinevad, siis leidub alati osakesi, millel on juhuslikult piisavalt liikumisenergiat, et pinnakihist välja pääseda. Vee all, pinnast kaugemal võib samuti olla lahkumiseks piisavalt kiireid molekule. Kui neid on vähe, siis nad välja ei pääse, sest kaotavad aeglasemate molekulidega põrkudes kiiruse.
Aurustumisel pöördub osa molekule pidevalt õhust vette tagasi. Selle tulemusena on veepinna kohal õhk püsivalt niiske, st sisaldab veidi veeauru (ptk Õhuniiskus). Temperatuuri tõusuga saavad vee molekulid hoogu juurde ja hakkavad üha enam veepinnalt lahkuma. Kuid see pole veel keemine. Keemistemperatuuril on kiireid molekule juba nii palju, et intensiivne aurustumine algab kogu vedelikus, mitte ainult pinnal. Tekivad aurumullid, mis kiiresti pinnale tõusevad, vesi on keema läinud. Kuni vett kannus veel on, temperatuur ei tõuse, selles mõttes on keemine sarnane sulamisega (ptk Molekulid. Tahkis).
Mõnikord, kui puhast vett kuumutatakse väga ühtlaselt, ilma segamata (näiteks mikrolaineahjus), võib temperatuur tõusta veidi üle keemistemperatuuri ilma aurumullide tekkimiseta. Kui sellist ülekuumutatud vedelikku veidi liigutada, algab keemine väga äkki. Pliidil ülekuumutatud vett teha ei saa, sest alt soojendamine põhjustab konvektsiooni, segab vett pidevalt ja mullid hakkavad tasapisi tekkima nõu kuumal põhjal.
Vee keemistemperatuur valiti juba väga ammu meie igapäevaselt kasutatava praktilise temperatuuriskaala (Celsiuse skaala) üheks aluseks, kindlaks punktiks. Arvatavasti just seepärast teavad kõik, et vesi keeb 100°C juures. Tegelikult sõltub vee keemistemperatuur üsna palju välisrõhust. Keemisel tekivad mullid saavad „ennast täis puhuda” ainult siis, kui aururõhk ületab välisrõhu. Teekannus on väliseks veele mõjuvaks rõhuks õhurõhk. See on küll veidi muutuv, aga igapäevasel teekeetmisel ei pruugi keemistemperatuuri muutuse pärast muretseda.
Mägedes, kus õhurõhk on oluliselt väiksem, tuleb toiduvalmistamisel arvestada, et vesi keeb madalamal temperatuuril. 6000-meetristele mägedele tõustes peavad alpinistid laagris toitu valmistades arvestama umbes 80°C juures keeva veega. Tõsiasja, et puhta vee keemistemperatuur lahtises anumas on otseselt seotud õhurõhuga ning selle kaudu ka päris rahuldavalt kõrgusega merepinnast (ja ka sügavusega allpool merepinda), kasutasid vanasti maadeavastajad ja loodusuurijad kõrguse määramiseks.
| Joonis 1.2.2. Keedunõus kaitseventiiliga kõrgendatud rõhku hoides on võimalik keeta vett kõrgemal temperatuuril kui 100°C. Survemahutis (autoklaavis) kaheatmosfäärilise rõhu all keeb vesi umbes 120°C juures. Sellist kõrgel rõhul ja temperatuuril keetmist kasutatakse steriliseerimiseks ja materjalide töötlemiseks. |
Keemistemperatuur. Siiani on jutuks olnud ainult vee keemine. Sobivatel tingimustel keevad ja moodustavad seejuures auru kõik ained, kui nad just kuumutamisel ei lagune. Keemistemperatuur ja selle sõltuvus rõhust on aine olulised füüsikalised omadused. Keemistemperatuuri atmosfäärirõhul on lihtne määrata. Seda muidugi juhul, kui aine üldse atmosfäärirõhul vedelas olekus esineb (ptk Molekulid. Tahkis). Kui vedelik keeb, st aurumullid tekivad ühtlaselt kogu nõus ja termomeeter näitab püsivalt ühte temperatuuri, siis ongi tegemist keemistemperatuuriga. Sulamistemperatuuri määramine on selles mõttes keerulisem, et alati peab kasutama hästi väikest ainekogust (ptk Molekulid. Tahkis).
Segude ja lahuste keemisel on olukord keerulisem. Lahuste keemistemperatuur on kõrgem kui puhtal lahustil. Selle põhjuseks on, et paljud lahustunud ained ei osale aurustumisel, ei lähe üle gaasilisse faasi (aurumullidesse). Lendumatu lahustunud aine aururõhku ei tekita. Keemiseks vajaliku välisrõhuga võrdse aururõhu saavutamiseks tuleb lahust kuumutada veidi kõrgemale temperatuurile. Lahuste keemistemperatuuri erinevus lahustite omast on huvitav nähtus. On selgunud, et keemistemperatuuri muutus sõltub ainult lahustunud osakeste kontsentratsioonist. Ei ole oluline, milline aine on lahustunud ja kas osakesed on ioonid, aatomid või molekulid.
Leidub päris palju kokandusnõuandeid, kus soovitatakse kindlasti lisada soola keeduvette, mitte hiljem valmistoidule. Väidetavalt tõstab soola lisamine keemistemperatuuri nii palju, et makaronid keevad kiiremini pehmeks. Jätame maitse-eelistused kõrvale ja küsime, kas keemistemperatuuri tõusust võib oodatud kasu olla?
Lahuste keemistemperatuuri tõus () sõltub lahuse molaalsusest (), lahusti omadusi kirjeldavast ebullioskoopilisest konstandist () ja isotoonilisest kordajast ().
Kui keeduveele lisada ühe liitri kohta 2 teelusikatäit soola (12 g), siis on saadud lahuse molaalsus 0,2 mol/kg. Vee ebullioskoopiline konstant on 0,512 K·kg·mol-1. Isotooniline kordaja kirjeldab aine lahustumisel tekkivate ioonide arvu, keedusoola korral .
Soola lisamisest saadav keemistemperatuuri tõus on tühine, toidu valmimise kiirust see ei mõjuta. Samas on muidugi võimalik, et mingid muud kaalutlused, maitse-eelistused, traditsioonid vms põhjendavad keedusoola koguse ja lisamise aja.
Lahustunud aineks on siin keedusool, mille sulamistemperatuur on 801°C ja keemistemperatuur 1413°C. Kuna vesi ja ka soolvesi keevad palju madalamal temperatuuril, kui keedusool sulab, siis võib öelda, et lahustatud on tahke aine. Täpsemalt, lahustunud aine oleks lahuse keemise temperatuuril tahke. See ei pruugi alati nii olla, näiteks vedelikud võivad lahustuda üksteises ja gaasid võivad lahustuda vedelikes. Isegi tahkes aines võib lahustuda gaas või vedelik.
Mõned vedelikud segunevad suvalistes vahekordades, näiteks vesi ja etanool. Teised ained moodustavad ühte nõusse valamisel selge piirpinna, näiteks vesi ja bensiin. Täpsemalt uurides selgub siiski, et piirpinnaga eraldatud vedelikud on mõlemad lahused. Bensiini ja vee näites on pealmises kihis bensiin, milles on lahustunud veidi vett ja allpool vesi, milles natuke bensiini. Kui segus on mitu piisavalt erineval temperatuuril keevat vedelikku, võib nende eraldamiseks või puhastamiseks üritada madalaima keemistemperatuuriga aine välja keeta. Seda meetodit nimetatakse destilleerimiseks. Lahustunud gaasid lahkuvad vedelikust muidugi ammu enne keemistemperatuurini jõudmist. Destillatsioon on oluline keemiatööstuse protsess ja just seepärast palju uuritud, teoreetiliselt ja tehnoloogiliselt hästi läbitöötatud. Vaatamata sellele peab ütlema, et vedelike eraldumine keemisel pole kõigis variantides sugugi lihtne nähtus.
| Joonis 1.2.3. Õli ja vesi lahustuvad üksteises väga vähe. Õli tihedus on väiksem kui veel, seepärast on õlikiht peal, vesi all. Samamoodi supipotis, rasvatilgad ujuvad supi peal. Muud lahustund ained jaotuvad kahe kihi vahel vastavalt sellele, kui hästi nad lahustuvad ühes või teises vedelikus. See võimaldab näiteks õlist ja kütustest mõningaid lisandeid välja pesta. | Joonis 1.2.4. Vedel lämmastik keeb. Kulbitäis veeldatud lämmastikku on anumast välja valatud ja keeb keemistemperatuuril. Lämmastiku keemistemperatuur on -196 °C (77 K), mis tähendab, et toatemperatuuril olev nõu on tema jaoks „väga kuum küttekeha”. Udu, mis keevat lämmastikku ümbritseb, tekib õhus leiduva veeauru kondenseerumisest (ptk 1.3.). |
Oleme kasutanud segamini mõisteid aur ja gaas. Tegelikult on muidugi iga gaas millegi aur. Näiteks väga madalal temperatuuril ja kõrgel rõhul gaasid veelduvad. Tavatingimustel veeldatud gaasid keevad. Lämmastik on meie atmosfääri põhigaas, teda on õhus kõige rohkem ja me räägime lämmastikust kui gaasist. Samas oleks täiesti korrektne ja teatud juhtudel isegi mõistlik rääkida vedela lämmastiku aurust.
Ained, mida me igapäevaselt nimetame tahketeks (metallid, soolad) sulavad siiski kõrgel temperatuuril, keevad ja aurustuvad. Gaasi ja auru mõisted on tavakeeles seotud sellega, mis olekus ainetega me igapäevaelus ja tehnikas kokku puutume. Näiteks halogeenid lihtainetena: räägime ja kirjutame nagu oleks kloor alati gaas, broom vedelik ja jood kristall. Seepärast on tavatingimustes juttu broomi ja joodi aurudest, aga samas kloorist kui gaasist.
Aine kolm olekut on küll selgelt erinevad, aga neil on paariti mõningaid sarnaseid omadusi. Gaaside ja vedelike ühiseks omaduseks on voolamine ja ainekoguse kindla kuju puudumine, nende ühine nimetus on voolis. Tahkised ja vedelikud on kindla tihedusega olekud, tihedus sõltub temperatuurist ja rõhust suhteliselt vähe. Tahkes ja vedelas olekus lahustuvad ained üksteises enamasti kindlates vahekordades, seepärast saame rääkida küllastunud lahustest, eutektilistest sulamitest ja aseotroopsetest segudest. Tahkiste ja vedelike ühine nimetus on kondensaine. Kuid just gaasiline olek on mõnes mõttes üsna eriline.
Gaasid segunevad kõigis vahekordades. Gaaside tihedus sõltub rõhust ja temperatuurist väga palju, nad on kokkusurutavad ja paisuvad. Ligilähedaselt on gaasi tihedus võrdeline rõhuga ja pöördvõrdeline absoluutse temperatuuriga. Täpselt kehtib see ideaalgaasi korral, aga mitte kõik gaasid ei allu piisavalt hästi ideaalse gaasi mudelile. Meenutame, et ideaalgaasi mudel on rakendatav hõredatele gaasidele (molekulide mõõtmed on võrreldes molekulidevahelise kaugusega tühised), kus molekulid üksteist ei mõjuta (va omavahelised elastsed põrked).
Reaalsed gaasid võivad seega erineda ideaalgaasi mudelist kahel põhjusel:
A) Rõhk. Molekulaarjõud (ptk Van der Waalsi jõud ja vesinikside) mida ideaalgaasi mudelis ei arvestata, sest molekulid on üksteisest kaugel, hakkavad kõrgemal rõhul ja madalamal temperatuuril siiski mõjuma.
Rõhk anuma seinale koosneb mikrotasandil üksikute molekulide elastsetest põrgetest. Ideaalse gaasi molekulid just nii anuma seinale rõhuvadki. Reaalses gaasis on põrke momendil gaasi molekuli ees anuma sein, aga „selja tagant” mõjutavad teda teised gaasi molekulid. Mida tihedamalt molekule ja mida polaarsemad molekulid, seda suurem on mõju.
B) Ruumala. Ideaalgaasi mudel eeldab, et molekulid on punktmassid, st mõõtmeteta. Sel juhul oleks kogu gaasi ruumala gaasi molekulide liikumiseks vaba. Reaalses gaasis võtavad molekulid ise ka ruumi, mida suuremad molekulid ja mida rohkem molekule ruumalaühikus, seda enam.
Reaalseid gaase kirjeldavad ebatavalistes oludes (kondenseerumistemperatuuri lähedal, väga kõrgel rõhul) mitmed reaalgaasi mudelid, kus klassikalisele gaasi olekuvõrrandile lisanduvad vajalikud täiendused.
Milline gaas on kõige ideaalsem? Ideaalse gaasi mudelile vastab kõige täpsemalt gaas, mille molekul on kõige väiksem, ei ole polaarne ja peaaegu ei polariseeru ka ajutiselt. See on heelium, mille molekul koosneb ühest pisikesest aatomist. Ka vesiniku molekul on väike, aga koosneb kahest aatomist, mis võimaldab õige veidi suuremate molekulaarjõudude teket.
Uurime ühte konkreetset reaalgaasi näidet. Millistel tingimustel ja kuivõrd kaldub lämmastik ideaalgaasi mudelist kõrvale?
Meenutame, et ideaalse gaasi olekuvõrrand seob gaasi koguse (), rõhu (), ruumala () ja temperatuuri () gaasi olekuvõrrandisse. R = 8314 J·K-1·kmol-1 (universaalne gaasikonstant).
ja
Saadud jagatis on võrdne ühega, kuni gaas käitub vastavalt ideaalgaasi mudelile. Kui uurida reaalse lämmastiku kokkusurumist või paisumist erinevatel temperatuuridel, siis tuleb välja mitu erinevust.
Joonis 1.2.5. ei ole tegelikult tehtud gaaside ruumala, rõhu ja temperatuuri mõõtmise järgi, vaid kajastab üht enamlevinud reaalgaasi kirjeldust, van der Waalsi võrrandit:
Võrreldes ideaalgaasi lihtsa võrrandiga, võime siin märgata „parandusi”. Konstant kirjeldab molekulide vahelisi mõjusid ja molekulide ruumala.
Ideaalgaas
Keemine
Keemine on vedeliku üleminek vedelast faasist gaasilisse, nii et aurustumine ei toimu mitte ainult vedeliku pinnalt, vaid kogu ruumalas tekkivate aurumullidena.
Tahkis ja teised
Tahkiste (tahkete kehade) eripära ilmneb deformeerimisel. Ainult tahkised avaldavad deformeerimisele vastupanu. Vedelike ja tahkiste ühine omadus on säilitada ruumala, mispärast neid nimetatakse kondensaineks.
Gaasid ja vedelikud
Gaasid ja vedelikud erinevad küll kokkusurutavuse poolest, aga tänu kindla kuju puudumisele on mõlemad voolavad, sellest ka nende ühine nimetamine voolisteks.
Ideaalse gaasi mudel reaalsuses
Õhu komponentide mahuline vahekord on üsna püsiv. Kuiv õhk koosneb lämmastikust (78%), hapnikust (21%) ja veel umbes kümnest gaasist (kokku 1%). Selle viimase ühe protsendi hulgas on kõige rohkem argooni (0,93%), aga ka atmosfääri toimimise seisukohalt väga olulist süsinikdioksiidi ja metaani. Selline oleks kuiva atmosfääri koostis, aga meie igapäevane õhk sisaldab peale nimetatu alati veel väikeses koguses veeauru. Veeaur on ainus atmosfääri komponent, mille sisaldus õhus pidevalt muutub. Õhus olev veeauru kogus muutub nii ööpäeva jooksul kui ka aastaaegade lõikes. Muutused on tihedalt seotud temperatuuriga ja omavad suurt tähtsust kliima kujunemisel. Kogu atmosfäärist on mahuliselt umbes 0,4% veeaur. Maapinna lähedal on veeauru õhus tavaliselt 1-4%. Veeauru sisaldust õhus nimetatakse õhuniiskuseks.
Soojal suvepäeval (õhutemperatuur 25°C) võib ühes kuupmeetris õhus olla näiteks 15 g vett. Veeauru sisaldust õhus võib arvuliselt väljendada mitmel moel, massi, ruumala või rõhu kaudu. Kõige lihtsam ongi märkida ühes kuupmeetris õhus sisalduva vee mass. Seda nimetatakse absoluutseks õhuniiskuseks () või veeauru tiheduseks. Grammi kuupmeetri kohta ongi tiheduse ühik, õhu tihedus on näiteks 1,29 kg/m3 ehk 1290 g/m3.
Niisiis, kirjeldataval suvepäeval võib näiteks olla õhu absoluutne niiskus
Samadel tingimustel (õhurõhk ja temperatuur) võib absoluutne niiskus olla väiksem, aga ka veidi suurem, kuid üle 23g/m3 see olla ei saa, kui temperatuur ei tõuse. Kui õhk muutub näiteks veekogudest aurustumise tõttu järjest niiskemaks, siis ühel hetkel tekib küllastunud veeaur. Küllastus tähendab seda, et nii palju, kui molekule läheb üle gaasi faasi, läheb neid ka tagasi vedeliku faasi. Normaalsel atmosfäärirõhul 25°C juures ei saa veeauru tihedus olla suurem kui 23g/m3. Seda nimetatakse küllastunud veeauru tiheduseks (). Kui vesi veekogude pinnalt, vihmapiiskadelt või taimede lehtedelt aurustub, siis absoluutne niiskus kasvab, aga ei ületa tavaliselt küllastatud auru tihedust. See tähendab, et maksimaalne absoluutne niiskus samadel tingimustel on
Küllastumine sõltub temperatuurist, igal õhutemperatuuril on oma küllastunud auru tihedus, mis on laboratoorselt määratud (ptk 1.6.) ja mida võib vaadata vastavast tabelist. Kõrgemal temperatuuril on küllastunud auru tihedused suuremad. Väga kuuma ja märja ilmaga (37°C) võiks ühes kuupmeetris õhus olla isegi 44 g veeauru, aga tihtipeale on kuumad ilmad pigem kuivad ja küllastus saabub hoopis temperatuuri langemise tõttu. Enamasti on õhus veeauru küllastusest vähem, aga välitingimustes võib õhuniiskus küllatuseni tõusta näiteks vihmase ilmaga või veepinnalt aurustumise tulemusena. Kuigi väike vihmasadu ei pruugi küllastuse saabumiseks piisavalt auru lisada, on siiski kindel, kestva saju ja uduga on õhu absoluutne niiskus maksimaalne võimalik.
Õhu veesisaldust kirjeldatakse mõnikord nii, nagu imaks õhk endasse vett või hoiaks kõrgemal temperatuuril tänu soojusliikumisele rohkem veeauru kinni. See pole õige ettekujutus.
On tõepoolest ahvatlevalt lihtne kirjeldada õhuniiskust, eriti küllastumist, nagu hoiaksid õhu gaaside molekulid vee molekule (veeauru) õhus justkui üksteisele palli põrgatades. Kuna kõrgemal temperatuuril on soojusliikumine intensiivsem, siis tundub loogiline, et kiiresti liikuvad lämmastiku ja hapniku molekulid nügivad vee molekule enam, ei lase neil kokku saada ja piiskadeks kondenseeruda. Tegelikult see nii ei ole.
Browni liikumise kirjeldused, eriti arvutimudelid, on meile siin karuteene teinud. Kipume mõtlema, et nii nagu vee molekulid põrgatavad ringi väikseid tahkeid kehakesi, nii ka molekulid poksivad üksteist. Tegelikult on vee molekulid õhu põhiliste koostisosade molekulidest väiksemad ja neid on õhus väga vähe. Ka lämmastikku ja hapnikku on tegelikult üsna vähe, st molekulid on gaasis päris hõredalt ja tühja ruumi jääb palju. Toatemperatuuril on õhu molekulide vahelised keskmised kaugused umbes 10 korda suuremad molekulide mõõtmetest ja keskmine molekuli liikumiskiirus umbes 600 m/s. Kui vaadata mõnda arvutimudelit, kus soojusliikumist visualiseeritakse, siis on molekulid enamasti kujutatud üsna suurelt, nad liiguvad väga aeglaselt ja kohtuvad liiga tihti. Näitlikkuse mõttes on see vajalik, sest 600 m/s liikuva molekuli kujutamine tühise kihutava täpikesena arvutiekraanil ei visualiseeriks midagi.
Küllastunud veeauru tihedus ei sõltu teiste gaaside juuresolekust. Vabalt veepinnalt auraks ka täiesti tühjas ruumis temperatuuril 25°C nii palju vett, et küllastunud auru tihedusoleks ikka 23 g/m3. Kõrgemal temperatuuril rohkem, madalamal vähem. Lämmastiku molekulid ei takista molekulide lahkumist veepinnalt ega ka soosi seda.
Tuleb meenutada, et vesi on teistest õhu gaasidest erinev. Lämmastik ja hapnik on maapealsete temperatuuride juures alati gaasid, aga vesi tuleb ette tahkes, vedelas ja gaasifaasis (ptk 1.1 ja 1.2.). Kui veepinnalt aurustub sama palju molekule, kui sinna tagasi kondenseerub, siis ongi tegemist küllastumisega. Madalal temperatuuril tekib samasugune tasakaal jää ja auru vahel. Lisaks sellele on vee molekulid polaarsed, mõjutavad üksteist teatud määral ja veeaur ei käitu seepärast päris ideaalse gaasina (ptk 1.2.).
Suhteline õhuniiskus. Kui on teada, et õhus on tõesti kuupmeetri kohta 15 g veeauru (), aga nimetatud temperatuuril võiks olla kuni 23 g (A25°C), siis ei ole raske välja arvutada, millise osa (mitu %) võimalikust moodustab tegelik. Seda suhet väljendatakse peaaegu alati protsentides ja nimetatakse suhteliseks (relatiivseks) õhuniiskuseks (). Suhteline õhuniiskus on inimeste tervise ja enesetunde hindamise seisukohalt oluline näitaja. Ka ilmaennustuses on suhteline niiskus parem näitaja kui absoluutne.
Kui juba nimetatud arvud valemisse panna, siis tuleb välja, et meie näidispäeva suhteline õhuniiskus on
Mugav on, kui eluruumides on õhu suhteline niiskus parajalt keskmine. Nii liiga kuiv kui ka liiga niiske õhk on pikema aja jooksule tervisele kahjulikud. Näiteks kooliruumides peab vastavalt tervisekaitsenõuetele õhuniiskus olema 30%–70%. Eluruumides peetakse siiski paremaks hoida niiskus vahemikus 40%–60%. Kahjuks on talvisel ajal köetud ruumides õhuniiskus tihti alla 30%, mis pole tervisele hea.
Tabel Küllastunud õhuniiskus erinevatel temperatuuridel.
Veeaur õhus
Õhu koostises on peaaegu alati väike kogus veeauru. Veeauru mass ühes kuupmeetris õhus on õhu absoluutne niiskus ehk veeauru tihedus.
Selle, kui palju veeauru maksimaalselt õhus võib olla, määrab eelkõige temperatuur. Eelneva peatüki näites oli 25°C õhus 1 m3 kohta 15 g veeauru, mis on 65% küllastusest. Kui seesama õhk jahtub, siis jääb absoluutne niiskus samaks, ikka endiselt 15 g/m3. Aga suhteline niiskus enam sama ei ole, sest madalamal temperatuuril on küllastunud auru tihedus väiksem. Näiteks 20°C juures on küllastunud auru tihedus 17,3 g/m3. Suhteline niiskus on nüüd 86,7%. Ilmselgelt saabub temperatuuri edasisel langemisel olukord, kus küllastus ja tegelik auru tihedus on võrdsed. Suhteline niiskus on siis 100%. Kui temperatuur veelgi langeb, siis tekib olukord, kus õhus peaks olema rohkem veeauru, kui seal antud temperatuuril saab olla. Ei ole midagi parata, osa veeaurust peab kondenseeruma vedelaks veeks. Looduses kohtame me seda olukorda üsna tihti, tegemist on udu ja kastega. Temperatuuri, mille juures veeaur hakkab kondenseeruma, nimetatakse kastepunktiks.
| Joonis 1.4.1 Sinise joonega on tähistatud küllastunud veeauru tiheduse temperatuurist sõltuvuse graafik, st veeauru absoluutse tiheduse väärtused, mis erinevate temperatuuride korral tähendavad suhtelist niiskust 100%. Punktis A on õhutemperatuur 25°C ja absoluutne õhuniiskus on 10 g/m³. Suhteline niiskus on sel juhul 43,5%. Temperatuuri langedes õhu absoluutne niiskus (õhu tegelik veesisaldus) ei muutu, küll aga suureneb suhteline niiskus. Punktis B on temperatuur 11°C, absoluutne õhuniiskus on endiselt 10 g/m³, aga suhteline niiskus on nüüd 100%. Edasisel jahtumisel osa veeaurust kondenseerub või härmatub. Õhu tegelik veeauru sisaldus väheneb seeläbi, aga suhteline jääb ikka 100%. Kui seesama õhk jahtuks näiteks 0°C, oleks 1 m³ veeauru juba alla 5 g, ja suhteline niiskus ikka 100%. Igast kuupmeetrist oleks kondenseerunud üle 5 g vett. | Joonis 1.4.2 Veepiisad külmal pudelil. Külmad kehad jahutavad lähema õhukihi nii palju maha, et kastepunkt saab ületatud ja piisad tekivad jahedale pinnale. Tegemist on sama nähtusega, mis põhjustab kaste langemist rohule ja lehtedele, kui õhutemperatuur maapinnal kastepunktini langeb. Kui mõni keha on väga külm, siis jõuab ta õhku natuke laiemalt jahutada ja võib näha tekkimas väikest udupilve, mis soojas õhus kiiresti hajub, st tekkinud udupiisad aurustuvad uuesti (joonis 1.2.4.). |
Kastepunkti on väga lihtne märgata. Kui suveõhtul paljajalu murul käies tunnete, et varbad saavad märjaks, siis ongi temperatuur maapinnal langenud kastepunktini. Kui õnnestub sel hetkel määrata temperatuur maapinnal, siis see ongi kastepunkt. Kastepunkti kaudu kalibreeritakse tihti õhuniiskuse mõõteriistu, hügromeetreid.
Kui kastepunkt jääb alla 0°C, siis vedelat vett muidugi tekkida ei saa. Ka seda nähtust me tunneme ja armastame. See on härmatumine.
Pilved. Õhuniiskusel on oluline roll pilvede moodustumisel. Väga üldiselt öeldes saavadki pilved moodustuda ainult õhus olevast veeaurust. Pilvede moodustumiseks ja sademete langemiseks on siiski vaja täita mitu tingimust.
A) Õhus peab olema piisavalt veeauru, et kondenseerumine saaks alata (meie kliimas sellest tavaliselt puudust pole).
B) Õhk peab jahtuma alla kastepunkti.
C) Kondenseerumise algamiseks on vaja kondensatsioonituumi. Tuumadeks kõlbavad soolakristallikesed, tolm, tahm, bakterid ja muu õhusaaste. Tuumosakeste puudumisel võib õhk nii palju jahtuda, st suhteline niiskus tõuseb tublisti üle saja protsendi, aga kondenseerumine ei alga.
D) Erinevate pilvede tekke ja sademete seisukohalt on oluline ka jääkristallide teke.
Kui õhk on piisavalt niiske, on pilvede tekkeks vaja jahtumist. See võib toimuda mitmel moel: erinevate õhumasside segunemisel, õhu jahtumisel kiirgumise või aurustumise tõttu, õhu paisumisel. Rünkpilved (mida üldiselt peetakse kõige ilusamaks ja õigemaks pilveliigiks) tekivad tihti just sellest, et niiske õhk tõustes paisub (rõhk langeb) ja seepärast jahtub alla kastepunkti. Seepärast on rünkpilved enamasti altpoolt tasased - sama niiskusega õhumassi tõusmisel saabub kastepunkt ligikaudu samal kõrgusel.
| Joonis 1.4.3 Pilvevaatlemine on meteoroloogias tähtis oskus. Kaasaegne pilvemääraja eristab kümme põhiliiki. Lisaks kirjeldatakse pilvede looduslikku mitmekesisust paljude erikujudena ja pilvevormidena. Tähtis on pilvede moodustumise viis ja kõrgus. Pilved pakuvad huvi ka paljudele harrastusmeteoroloogidele ja ilmatarkadele, sest teatud määral võimaldab pilvetundmine lühiajaliselt ilma ennustada. |
Kõrbelise kliimaga aladel ei saa sajupilved tekkida just õhu kuivuse tõttu. Kui absoluutne niiskus on väga madal, siis ei vii isegi päris korralik jahtumine kastepunktini, pilvi ei teki ja sademeid ei ole. Kohaliku kliima kujunemisel on olulisemad tegurid õhutemperatuur ja -niiskus, aga ka tuuled, õhurõhk jm. Seepärast päris otsest seost õhuniiskuse ja sademete vahel ei ole. Näiteks maailma kõige kuivemaks kohaks peetavas Atacama kõrbes (Lõuna-Ameerika idarannikul) ei saja peaaegu kunagi, ometi on taevas pilves ja õhk võrreldes teiste kõrbetega suhteliselt niiske. Sademeid arvestatakse seal pikaajalise keskmisena umbes 1 mm aastas, paljudel aastatel ei saja üldse. Eestis sajab tavaliselt 520–820 mm aastas. Atacama vihmapuuduse põhjuseks loetakse ümbritsevate mägede ja püsiva hoovuse mõju õhurõhule ja õhumasside liikumisele. Kuigi seal vihma ei saja, võimaldab niiske õhk mõnikord udu ja kaste tekkimist, millest piisab samblike ja isegi mõnede kaktuste eluspüsimiseks.
Tuleb tunnistada, et kuigi pilvede teket on palju uuritud, ei ole tänaseni lõpuni selged biosfääri ühendite, õhureostuse (sh lennukite heitgaaside) ja kosmilise kiirguse seosed pilvetekkega.
Sõna „ilm” on eesti keeles mõnusalt mitmetähenduslik. Ilmatu suur Maailm, kõik see mis meid ümbritseb. Maa ja ilm, all ja üleval. Meil on varnast võtta tõlkimatu käibenali, et ilmast ilma on ilmaga jama, aga ilma ilmata ka läbi ei saa. Oleme harjunud ilmaennustust kiruma ja vähesed on valmis ilmaennustajaid ehk sünoptikuid teadlasteks pidama. Kindlasti hindame me ilmanähtusi väga subjektiivselt. Vaevalt, et keegi vaidlustab vihmasadude vajalikkuse. Samas on tavapärane pahandada, kui vihma sajab puhkuse ajale planeeritud jalgrattamatka kõigil päevadel ja öödel. Muidugi kerkib siis küsimus, miks on ilma nii raske ennustada?
On tõsi, et me elame muutliku ilmaga kohas. Mitmetes kohtades üle maailma esineb üsna regulaarseid ilmanähtusi (sajab põhiliselt õhtuti, vihmaperiood algab septembris, lumi tuleb maha novembri algul ja püsib aprillini), meil see paraku nii lihtne ei ole.
Vaatame kõigepealt, kuidas ilmanäitajad ühes konkreetses kohas ööpäevade lõikes muutuvad (joonis 1.5.1.). Seejuures märkame mitmeid üsna kohapealse iseloomuga muutusi. Päeval on soojem kui öösel, üks päev on soojem, teine pisut jahedam, öösel on õhuniiskus 100%.
Temperatuur. Graafikutele jääb vähemalt osaliselt kolm ööd. Esimese päeva õhutemperatuuri maksimum on kõrgem kui teisel ehk nagu tavaliselt öeldakse, esimene päev oli soojem.
Teise päeva temperatuuri käigus on märgatav jõnks, mille põhjus ei selgu esitatud graafikutelt.
Õhuniiskus. Laias laastus on temperatuuri ja suhtelise õhuniiskuse graafikud vastupidised, st kui on soe, on suhteline niiskus väiksem. Jahedatel öödel tõuseb niiskus 100%-ni, on kastene või udune. Kõige esimene öö on olnud jahedam ja ka õhuniiskuse graafik püsib pikalt 100% peal.
Niiskuse graafik teeb teisel päeval väga täpselt kaasa temperatuuri kõikumised, kõik täpselt tagurpidi. Ka temperatuurigraafikule vastav jõnks on samal kellaajal.
Sademed. Esimesel hommikul, kui temperatuur oli juba tõusnud, ei hakanud õhuniiskuse graafik sugugi langema. Selle põhjuseks oli hommikune vihmasadu. Kui sadu lakkas, sai ka niiskuse graafik „laest lahti”.
Õhtust kastet ja hommikust udu, isegi väikest vihmasabinat saab edukalt seletada kohalike veekogude pinnalt ja taimelehtedelt aurustunud vee kondenseerumisega. Suuremad sajud ja lumetuisud peavad ilmselgelt pärinema mõnelt suuremalt veeauru allikalt, küllap siis ookeanilt.
Vaatame ühte konkreetset näidet sellest, kuidas suvised vihmasajud Eestisse jõuavad (joonis 1.5.2.). 24. juunil on olnud üsna ilus, kuigi mitte eriti soe suvepäev. Õhtul on meil vahelduva pilvitusega ilm, mõõdukas tuul puhub kirdest. Tähelepanelik vaatleja võib märgata, et päike loojub pilvedesse. See ei ennusta head ilma, sest väga tihti tulevad meile järgmiseks päevaks just need pilved, mis õhtul edelast paistavad. Vanarahva ilmatarkuski ütleb, et kui loojuv päike tagasi vaatab, tuleb homme ilus päev. Meteoroloogiasatelliitide piltidelt võib näha, et eelmisel päeval Atlandi ookeanil aurustunud veest on moodustunud pilvekeeris, mis liigub üle Kesk-Euroopa ja peaks 25. juunil ületama Eesti. Kindlasti tuleb sajune päev. Pöörlev niiske õhumass ei ole küll ise külm, aga tõmbab tuule suunda muutes meile põhja poolt külmemat õhku ja seepärast on järgmine päev mitte ainult vihmane, vaid ka jahe. Teise päeva õhtuks on sajud taandunud kirdesse, aga satelliidipilt näitab juba uue keerise tekkimist Briti saartest läänes. Esialgu on veel vara öelda, kuhu poole niiske õhumass järgmiseks täpselt pöördub, aga võib-olla juba südaööks saavad sünoptikud ka selle kohta ennustuse tehtud.
Seda piirkonda, mis meie ilma nii oluliselt mõjutab, nimetatakse mõnikord Põhja-Atlandi ilmakatlaks. Selles katlas keedetakse enamasti meie suvised sajud ja sügistormid. Sealse temperatuuri, õhurõhu ja -niiskuse, tuulte jm järgi arvutatakse järgmiste päevade ilmateade. Euroopa ülikoolides ja teadusinstituutides arendatakse ja rakendatakse pidevalt mitmeid ilmamudeleid. Tuleb tunnistada, et tänaseks on kolme päeva ilmateade enamasti palju-palju parem, kui me tahame tunnistada. Ilmaennustajate kirumise traditsioon on visa kaduma. Siiski ei aita ka väga head andmed ja ülivõimsad arvutid teha kuigi täpset ilmaennustust pikemaks ajaks. Näiteks järgmise aasta jaaniõhtut need ilmamudelid planeerida ei aita. Siin Läänemere ääres sõltub igapäevane ilm siiski päris paljudest pisiasjadest ja atmosfäär on nii suur, et piltlikult öeldes „ilm ei tea isegi, milline ta järgmisel suvel tuleb”.
Õnneks on meie ilmad siiski mõõdukad. Ka meid ohustavad tormid ja tuisud, merevee taseme tõus, suured sajud ja üleujutused, rahe ja teisedki äärmuslikud ilmanähtused. Samas oleme mitmestki päris äärmuslikust riskist seni vabad. Atlandi ookeani teisel kaldal tabavad igal aastal Kuubat ja Floridat troopilised orkaanid. On kostnud arvamusi, et kliima muutumine võib viia selleni, et ka meid hakkavad orkaanid kimbutama. Tegelikult seda ohtu siiski pole, kliima peaks selleks ikka väga-väga palju muutuma, et troopilised tsüklonid Läänemerele jõuaksid. Vaikse ookeani idaosa suurtest ilmariskidest kuulsaim kannab nime El Niño. Tegemist on ookeani pinna erakordse soojenemisega, mille tingivad püsivad muutused tuule suunas. El Niño on perioodiline nähtus, aga väga täpset korda ta ei pea, sama olukord tekib uuesti 4 kuni 7 aasta järel. Sooja pinnavee kogunemine Lõuna-Ameerika rannikule põhjustab olulisi ilmamuutusi. Tavaliselt kuiva kliimaga Peruud ja Ecuadori kimbutavad vihmasajud. Austraalias, kus niigi ollakse tihti hädas kuivuse ja kuumaga, esinevad El Niño aastatel erakordsed põuad. Hoovuste muutumine mõjutab kalavarusid ja seekaudu paljude piirkondade majandust. Klimaatilised muutused ulatuvad kaugele Põhja-Ameerika sisemaale, mõnedel hinnangutel on mõju lausa globaalne.
Õhuniiskuse mõõtmiseks kasutatakse hügromeetreid. Muidugi on olemas ka muude niiskuste (näiteks puidu niiskuse) mõõtmise hügromeetrid, aga siin tuleb juttu õhuniiskuse mõõtmise viisidest. Hügromeetrid on kasutusel kasvuhoonetes, tööstusruumides, inkubaatorites, saunades, muuseumides, ladudes jm. Pole paha ka elu-, töö- ja kooliruumides vahel õhuniiskust kontrollida. Niiskuse mõõtmine on peaaegu alati kaudne. Kõige otsesem viis absoluutse niiskuse mõõtmiseks on kaalumine. Kaaluda tuleks uuritav õhk ja võrdne ruumala kuiva õhku. Masside erinevusest on lihtne arvutada veeauru kogus ühes kuupmeetris ehk absoluutne õhuniiskus. Põhimõtteliselt on selline mõõtmine võimalik, aga igapäevaseks tarvitamiseks kohmakas.
Suhtelise niiskuse igapäevaseks määramiseks kasutatakse mitmete materjalide omaduste muutumist sõltuvalt niiskusest. Õhuniiskusega seotud muutusi võime märgata ka oma tavaliste asjade juures. Puit on näiteks materjal, mille niiskus kõigub koos õhu veesisaldusega ja puitesemete mõõtmed muutuvad. Kapiuksed käivad kuiva ilmaga kergemini, mõni sahtel ei tule niiskel sügisel hästi lahti. Muusikud teavad, et puidust pillid lähevad ilmamuutusega häälest ära. Raamatukogude hoidlates jälgitakse hoolega õhuniiskust, sest liiga kuivas õhus tõmbuvad raamatukaaned kõveraks. Laialt on tuntud mitmete elektrinähtuste seos õhuniiskusega. Mitmesugused niiskumisega ja kuivamisega seotud füüsikaliste omaduste muutused annavad võimaluse konstrueerida erinevaid hügromeetreid.
Juushügromeeter. Suur osa elu- ja tööruumide mõõteriistu, mis aitavad meil valvata, et õhk oleks tubades tervislikult niiske, mõõdavad juuksekarva pikkust. Inimese juustel, aga ka muudel loomsetel- ja isegi tehiskiududel on omadus olla niiskes õhus veidi pikem kui kuivas. Vahe ei ole väga suur, aga piisav, et seda muutust üsna lihtsa ülekandega osuti abil nähtavaks muuta.
Elektrilised hügromeetrid. On olemas aineid, mille elektrilised omadused (takistus või dielektriline läbitavus) sõltuvad niiskusest. Neil nähtustel põhinevad hügromeetrid on tänapäeval laialt levinud, sest võimaldavad väga lihtsalt pikaajalise mõõtmise tulemusi salvestada.
Kuigi need laialt kasutatavad hügromeetrid on lihtsad ja odavad, on neid vaja millegi järgi kalibreerida. Selleks on põhiliselt kasutusel kaks veidi keerulisemat hügromeetri tüüpi, kus ei kasutata niiskusega kaasnevaid materjalide omaduste muutusi, vaid õhu aurusisaldusega kaasnevaid füüsikalisi nähtusi.
Psühromeeter. Õhuniiskuse määramise klassikaline, psühromeetriline meetod seob kokku kaks aurustumisega (ptk Gaas ja vedelik) seotud nähtust.
A) Aurustumise intensiivsus on seotud õhuniiskusega. Igaüks teab, et kuivamine (vee aurustumine asjadelt, riietelt, inimestelt) toimub kuiva ilmaga palju kiiremini. 100% õhuniiskuse korral näiteks pesu üldse ei kuiva. Pesukuivatamisel on teisi nähtusi, mis võivad tublisti abiks olla, näiteks päikesepaiste ja tuul. Mõõteriistades püütakse need segavad nähtused kontrolli alla hoida, nii et aurustumist määraks ainult õhuniiskus.
B) Aurustumiseks kulub energiat ja kui kehalt aurustub vett, siis ta jahtub. Näiteks teame, et märgades riietes on külm. Kokku tähendab see, et kuivas õhus peab märg keha jahtuma rohkem kui niiskes õhus, kui kõik muud tingimused on samad.
Psühromeeter koosneb kahest termomeetrist. Üks on kuiv, teine hoitakse pidevalt märg. Lihtne vahend vedeliktermomeetri niisutamiseks on reservuaari ümber keeratud märg lapp, mis tuleb otsapidi vees hoida. Kui õhk on veeaurust küllastunud (õhuniiskus 100%), siis vesi märjalt lapilt ei aurustu, märg termomeeter ei jahtu ja näitab koos kuivaga ümbritseva keskkonna temperatuuri. Kui suhteline niiskus on väiksem, siis hakkab märjalt termomeetrilt vett aurustuma, see jahtub ja temperatuurinäitudesse tekib vahe. Vahe on seda suurem, mida kuivem on õhk. Psühromeetriga käib kaasas vastav tabel, kust saab leida temperatuurierinevusele vastava õhuniiskuse.
Täpseteks meteoroloogiavaatlusteks ja teiste hügromeetrite kalibreerimiseks kasutatavates psühromeetrites luuakse eriti kontrollitud tingimused. Õhu liikumiskiirus termomeetrite ümber hoitakse ventilaatoriga täpselt võrdne ja termomeetrid on eraldi kaitstud igasuguse välise soojuskiirguse eest.
Jahutatud peegel. Hügromeetrite kalibreerimiseks sobib hästi kastepunkt, temperatuur, mille juures õhus olev veeaur hakkab kondenseeruma (ptk Kastepunkt). Väga hästi on kondenseerumise algus (kaste langemine) näha peegelpinnal. Kastepunkti määramiseks mõõdetakse jahutatava peegli temperatuur täpselt kondenseerumise algushetkel. Peegli uduseks muutumise võib määrata hoolsa vaatlemisega, aga on olemas ka elektroonilised meetodid. Kastepunktile vastava absoluutse niiskuse saab vaadata tabelist. Elektrooniliste seadmete korral on tabel muidugi arvutimälus. Sedasorti hügromeetreid kasutatakse tihti laborites, sest kuigi üsna täpsed ja töökindlad, vajavad nad hooldamist ja puhastamist. Tulemusi võivad häirida tolm ja muu õhusaaste.
Vedeliku ja gaasi piirpinna lähemaks uurimiseks vaatleme kõigepealt vihmapiiska. Kui õhk, mis sisaldab piisavalt veeauru ja kondensatsioonituumi, on piisavalt jahtunud (ptk Kastepunkt), tekivad piisad, mis võivad õhuvooludes hõljuda, aga võivad ka sademetena alla langeda. Kuid mis hoiab vihmapiiska koos?
Vastus on lihtne: kõiki vedelikukoguseid hoiavad koos molekulaarjõud. Piiskades toimivad need jõud sarnaste osakeste vahel (näiteks elavhõbedatilgas või vihmapiisas), neid nimetatakse kohesioonijõududeks (ladina keeles: cohaereo - kokku kuuluma, tervikut moodustama).
Kui vihmapiisk jõuab aknale, siis hoiavad teda seal kinni jälle molekulaarjõud. Kuna klaasi ja vihmavee molekulid on erinevad, siis on tegemist adhesioonijõududega (ladina keeles: adhaereo - kinni hoidma, küljes rippuma).
Kohesioon ja adhesioon osalevad mitmetes huvitavates ja olulistes nähtustes: pindpinevus, vedelike voolamine torudes ja lahtistes voolusängides, tilkumine, märgumine, imbumine poorsetesse ja kiulistesse materjalidesse.
Meenutame, et faasidevahelisel (ptk Faasid) piirpinnal on tihti erilisi omadusi, seal toimuvad mitmed füüsikalised ja keemilised protsessid, ilmneb erinevaid nähtusi. Vihmapiisaski on vedeliku ja gaasi piirpinna molekulid täiesti erilises olukorras. Vedeliku sees on iga molekul ühtlaselt ümbritsetud naabritega ja seotud kohesioonijõududega, mis on keskmiselt võttes tasakaalus (resultantjõud on null). Piirpinnal on olukord teine. Väljaspool (gaasi poolel) on molekule väga vähe, tasakaal on rikutud ja seepärast mõjub pinnakihi molekulidele summaarselt tõmme ainult ühes suunas, sissepoole. See tekitab vedeliku pinnakihis teatava pinge, mida nimetatakse pindpinevusjõuks. Pindpinevust võrreldakse tihti põhjendatult venitatud (pingutatud) elastse kilega. Kui täispuhutud õhupalli pigistada, siis kummikile venib suuremaks. Kui pall uuesti lahti lasta, püüdleb ta tagasi minimaalse pindala poole, täpsemalt minimaalse potentsiaalse energia poole. Sarnaselt toimib ka vihmapiisk. Vee ja õhu piirpind on alati võimalikult väike. Muude mõjude puudumisel on vihmapiisk kerakujuline, sest kera on sama ruumala juures kõige väiksema pindalaga keha.
Vedelike pinnakihil on omadus kokku tõmbuda, olla võimalikult väikese pindalaga. Seda nähtust, pindpinevust, kirjeldab pindpinevusjõud. Kui suur on pindpinevusjõud ja millest ta sõltub?
Vaatleme nüüd ühte koolifüüsikas hästi tuntud pindpinevuse katset. Peenikesest traadist rõngas on vee all. Kinnitame rõnga külge tundliku dünamomeetri ja üritame rõngast ettevaatlikult läbi veepinna välja tõsta. Kui rõngas on juba osaliselt veepinnast kõrgemal, siis on dünamomeetrilt näha, et veepind „ei lase rõngast lahti”. Hea nägemise korral võib paljude veest välja tõstetavate esemete korral märgata, kuidas veepind venib teatud määral asjadele järele. Siin ilmutabki pindpinevusjõud end mõõdetaval moel. Puhta vee ja hea katsekorralduse juures on võimalik ära mõõta, et 15,9 cm läbimõõduga rõnga veepinnalt lahtirebimiseks toatemperatuuril on vaja jõudu umbes 73 mN (). Sellise läbimõõduga rõnga korral on katkirebitavat veepinda üks meeter (), pool meetrit rõnga siseküljel ja sama palju välisküljel. Pindpinevusjõud ühikulise pikkuse kohta kannab nime pindpinevustegur. Kui vesi ei ole puhas või on tegemist hoopis mingi teise vedelikuga, siis saame kirjeldatud katses ka teise jõu. Pindpinevustegur on vedelikku iseloomustav suurus, kõigil vedelikel ja lahustel erinev.
Katse kokkuvõttena võime kirjutada:
Vee pindpinevustegur () on 0,073 njuutonit meetri kohta. Pindpinevustegur kirjeldab jõudu ühikulise pikkuse kohta. Samas kirjeldab pindpinevustegur ka energiat ühikulise pinna kohta ja seega on tal võrdväärne ühik: džauli ruutmeetri kohta (J/m2). Seepärast kõneldakse mõnikord pinnaenergiast ja pindpinevuse piltliku seletamise jaoks on see isegi parem. Meenutame, et potentsiaalse energia miinimumi printsiip on üks füüsika üldprintsiipidest ja vastavalt sellele püüdleb ka vedeliku vaba pind minimaalse energia poole, st minimaalse pindala poole.
Tabel Vedelike pindpinevustegurid temperatuuril 20°C
Pindpinevusjõu ja pinnaenergia kohta võime seega öelda:
jaKus on pindpinevustegur, on vedeliku piirpinna pikkus ja on vedeliku pinna pindala.
Pindpinevusteguri määramise näites venis veepind koos rõngaga ülespoole, kui me rõngast veepinnalt tõstsime, aga tegelikult pole selleks vaja midagi tõsta. Samas nõus, kus katset tegime, võib märgata, kuidas vesi päris servas üsna vähesel määral „üritab mööda seina üles voolata”. Nähtust, kus vedelik tahket pinda mööda laiali valgub, nimetatakse märgamiseks. Ei ole raske märgata, et mitte alati ei märga vedelik tahket ainet. Märgumatust ainest anuma ja vedeliku kokkupuutepiiril ei kõverdu vedeliku pinnakiht mitte üles, vaid alla. See, kas vedelik märgab pinda või mitte, sõltub adhesiooni- ja kohesioonijõudude suhtest.
Üsna ilmekas on märgamist jälgida horisontaalsel pinnal lebava väikese vedelikutilga korral. Gaasi ja vedeliku piirpind moodustab tahke alusega nurga (Θ), mida mõõdetakse vedeliku seest ja nimetatakse märgamisnurgaks. Kui vedelik valgub alusel laiali (märgamine), on tilk lame, märgamisnurk on teravnurk. Nii käituvad näiteks kondensaaditilgad külmal pudelil (joonis 1.4.2.). Ideaalse märgamise korral vajuks vedelik alusele täielikult laiali, moodustades ühe molekuli paksuse kihi. Kui piisk võtab alusel pigem kera kuju (mittemärgamine), on märgamisnurk nürinurk. Tihti käituvad nii hommikused kastetilgad. Piisad pudelil ja taimelehel tekivad mõlemad õhu veeaurust, erinev kuju tuleb tahke pinna erinevusest, täpsemalt adhesioonijõudude erinevusest. Päris kerakujulist piiska ei saa isegi ideaalse mittemärgamise korral. Piisad on raskusjõu tõttu siiski veidi lapikud, mida suuremad, seda enam.
Pindpinevuse ja märgamisega on seotud palju igapäevaseid nähtusi, nagu vee imbumine poorsetesse materjalidesse, vee liikumine pinnases ja taimedes jpm. Vedelike omadust tungida peenikestesse vahedesse, kiudude vahele, pooridesse nimetakse kapillaarsuseks. Vaatleme kapillaarsuse näitena vee käitumist peenikeses püstises klaastorus, kapillaaris. Pole raske märgata, et klaasi ja vee puutepiiril tõuseb vesi veidi mööda klaasi üles. Piisavalt peenikeses vette pistetud torus (joonis 1.7.5.) saavad need veepinna serva kumerdumised keskel kokku. Toru sees tõuseb veepind ümbritsevast veest kõrgemale ja hoiab ligilähedaselt sfäärilist kuju. Vedelikusamba lahtise pinna kõverdunud kuju nimetatakse meniskiks. See tekib kõigis torukestes, pipettides, voolikutes, väikestes mõõtnõudes jm. Paljud inimesed vaatavad värvitud piirituse meniskit oma õuetermomeetri paisumistorus iga päev, aga väiksuse tõttu märgatakse seda harva. Luupi appi võttes on hästi näha sedagi, et elavhõbetermomeetris kõverdub menisk teistpidi, sest elavhõbe klaasi ei märga.
Küsime nüüd, millest sõltub ja kui suur on kapillaartõus? Otsapidi vette pistetud peenikese klaastoru sees tõuseb vesi ümbritsevast veepinnast kõrgemale. Kui kõrgele tõuseb veesammas teatud läbimõõduga klaaskapillaaris?
Kui vesi on kapillaari tõusnud ja püsib seal paigal, siis on tegemist jõudude tasakaaluga. Allapoole suunatud raskusjõud () on tasakaalus pindpinevusjõuga (). Võib öelda, et vee menisk ripub tänu märgamisele servapidi klaasi küljes.
Arvestame, et
ja
Avaldame silindrilises kapillaaris oleva vee massi tiheduse (TeX parse error: Missing superscript or subscript argument) ja vedelikusamba mõõtude (, ) kaudu, vee ja klaasi puutepiiri pikkuse toru läbimõõdu () kaudu ning saame (asendades ja teisendades) kapillaartõusuks:
Kirjeldatud mudel ei ole kuigi täpne. Näiteks arvestasime ülihea märgamisega praktiliselt nullkraadise märgamisnurgaga, mis vee ja klaasi korral muidugi nii ei ole. Ometi annab saadud valem kapillaartõusust hea ettekujutuse. Vedelikud tõusevad kõrgemale peenemates kapillaarides ja suurema pindpinevusteguri korral. Muidugi vähendab kapillaartõusu vedeliku suurem tihedus. Ehitusinsenerid väidavad, et sobivate tingimuste korral võib kapillaartõus näiteks betooni poorides ulatuda kümne kilomeetrini. Kapillaarsusega ja aurustumisega seondub vee ja lahuste liikumine taimedes, pinnases ja ehitusmaterjalides.
Tuletame meelde, et pindpinevust juhivad kohesioonijõud, märgamist aga adhesiooni ja kohesioonijõud koos. Seega on märgamine keeruline ja mitmetahuline nähtus, sõltub nii vedeliku kui tahkise omadustest ja on tundlik vedeliku lisandite ning pinna puhtuse suhtes. Oma osa mängib temperatuur ja aurustumine. Kapillaartõus on küll märgamisega seotud, aga see pole siiski sama nähtus. Hea märgamise korral tõuseb vedelik mööda anuma seina ka laias anumas, mitte ainult kapillaaris. Näiteks õlil ja petrooleumil on omadus mööda nõu seinu „üles ronida” ja nii väliskülg kui lauaplaat mõne päevaga üsna õliseks teha. Samamoodi käituvad alkohol ja kergemad kütused, mis aga aurustumise tõttu lausa pudeli välisküljele ei jõua.
Pindpinevus
Vedeliku ja gaasi piirpinna omadustega seonduvaid nähtusi, mida põhjustab pinnakihi molekulide vaheliste molekulaarjõudude tasakaalustamatus, nimetatakse pindpinevuseks.
Eelmistes peatükkides kirjeldasime pindpinevust ja märgamist kui nähtusi, mis seonduvad vedeliku piirpinna omadustega (gaasiga, tahkisega, teise vedelikuga). Siiamaani käsitlesime neid nähtusi staatilistena. Vihmapiiska kirjeldasime kerakujulisena (ptk Pindpinevus) tekkimise hetkest peale ja ta justkui püsiks sellisena igavesti. Kapillaartõusu mudelis kehtis püsiv tasakaal raskusjõu ja pindpinevusjõu vahel (ptk Kapillaartõus). Tegelikult on võimalus asju nii staatiliselt kirjeldada pigem erand, sest vedelike ja gaaside (vooliste) molekulid on liikumises üsna vabad ja põhiliseks omaduseks on voolamine, sellest nende ühine nimigi. Voolamine on üsna keeruline nähtus, milles osalevad nii voolise osakeste vahelised kohesioonijõud kui ka voolusängi (toru, vooliku, teise vedeliku või gaasi) ja voolava vedeliku vahelised molekulaarjõud . Ka märgumine ja kapillaartõus on dünaamilised nähtused, kus on oma osa vedeliku viskoossusel ja aurustumisel.
Tilkumine. Vaevalt on kuigi paljud inimesed näinud vihmapiisa moodustumist. Esiteks on piisad kõrgel, teiseks on nad algul väga pisikesed. Kuid tilgad tekivad ka tilkumisel, ja tilkuvat kraani on igaüks näinud. Arvatavasti ka kuulnud. Kõige lihtsam ja ilmekam viis tilkade saamiseks ongi lasta vedelikul aeglaselt välja voolata vertikaalse toru alumisest otsast. Kui vedeliku pealevool on piisavalt aeglane, on hästi näha, kuidas veepind hakkab tasapisi allapoole kumerduma. Pealetuleva vedeliku pind venib raskusjõu toimel üha allpoole ja järsku annab miski järele. Tekkinud tilk kukub alla. Kohe hakkab kasvama järgmine. Valmis tilk kukub kahjuks nii kiiresti, et me ei näe täpselt, kuidas ta moodustub, kust ja kuidas veepind järgi annab ja milline on tilga kuju. Kiirkaameraga pildistatult on näha, et eraldunud vedelikukogus võtab kiiresti kera kuju ja pole langedes sugugi „tilgakujuline”. Võib-olla tundub meile, et näeme just sellist tilgakuju hetkel, kui veetilk kraaniavast lahti pääseb. Tuleb tunnistada, et just lahtirebimise hetkel see väga lühikeseks hetkeks nii ongi. Paigalseisvad tilgad (kastepiisad) ja vabalt langevad või hõljuvad tilgad (vihmapiisad) on siiski kerakujulised, kiiremal langemisel natuke langemissuunas lapikuks surutud.
Tilkade mõõtmine pole sugugi keeruline. Tuleb loetud hulk tilku topsikusse koguda ja ära kaaluda. Nii saab arvutada tilga massi ja tilgale mõjuva raskusjõu. Kui vedeliku tihedus on teada, saab arvutada ruumala ja seekaudu ka tilga läbimõõdu.
Tilgutamismeetodil saab määrata vedeliku pindpinevusteguri ja selle kaudu hinnata näiteks lahuste kontsentratsiooni. Kasutades kapillaartõusu juures rakendatud arutluskäiku (ptk 1.7.), on lihtne saada valem pindpinevusteguri arvutamiseks. Tilga lahtirebimise hetkel on allapoole mõjuv raskusjõud ja pindpinevusjõud tasakaalus, mis hoiab tilka toruotsal kinni. Tasakaalutingimus on siis
ja sellest
Piirpinna pikkus, mis lõpuks tilga kasvades enam vastu ei pea, on võrdne toru ümbermõõduga. See ei ole jällegi (sarnaselt kapillaartõusu arvutusele) väga täpne mudel, aga paljudel praktilistel juhtudel päris hästi kasutatav.
Mõnikord on mõistlik pindpinevustegur () arvutada toru läbimõõdu (), vedeliku tiheduse () ja näiteks 100 tilga summaarse ruumala () järgi. See näeks välja nii
ja on üsna hästi kasutatav vedelike (sh segude ja lahuste) kvaliteedi analüüsiks, näiteks kütuste kontrollimiseks.
Mullid. Kondenseerumine ja tilkumine ei ole ainsad viisid tilkade saamiseks. Me kõik tunneme hästi pritsimismeetodit ja tehnikas saadakse vajaliku suuruse ja kontsentratsiooniga piisku pihustamisega. Kuid tilkadel on üks hästituntud analoog, mõnes mõttes ka vastand. Need on mullid, mida me juba nimetasime keemise kirjeldamisel (ptk Gaas ja vedelik). Mulli, nagu tilkagi, piirab gaasi ja vedeliku piirpind. Mullid on tihti kerakujulised nagu tilgadki. Erinevus on selles, et nüüd on piirpind gaasi poolt vaadates nõgus ja vedeliku poolt kumer. Mulli on suletud teatud kogus gaasi ja kuna gaasid on kokkusurutavad, siis on mulli ruumala muutlik. Seoses sellega on mullid tilkadest veelgi dünaamilisemad ja keerukamad uurimisobjektid.
Mullid on väga igapäevane nähtus nii looduses kui tehnikas, võib-olla piiskadest laiemaltki levinud. Lühike ja mitte väga täielik mullitekke nimekiri võiks olla järgmine.
Keemismullid. Keemistemperatuurini kuumutatud vedelikus tekivad aurumullid. Kui aurumull satub konvektsiooni teel kohta, kus temperatuur on keemistemperatuurist madalam, siis aurumull kaob, st kondenseerub uuesti vedelikuks. Intensiivsel kuumutamisel tõusevad keemismullid kiiresti ülespoole ja kasvavad seejuures suuremaks.
Lahustunud gaaside eraldumine, näiteks süsihappegaasi mullide tekkimine karastusjoogi pudeli avamisel.
Õhu segamine vette, näiteks kosest langeva vee või murdlainetuse korral.
Gaasi „puhumine” vedelikku. Näitena võib vaadelda sukelduja väljahingatava õhu pinnaletõusmist või aktiivmuda aereerimist reovee biopuhastis.
Keemilise reaktsiooni gaasilised saadused. Näiteks süsihappegaasi tekkimine söögisooda reageerimisel happega või järvesettest bioloogilisel lagunemisel kerkivad gaasimullid.
Seebimullid. Kindel õhukogus, mis on piiratud õhukese seebiveest kilega, on tuntud seebimullina. Seebivesi ei pea ilmtingimata sisaldama seepi. Kõlbavad ka paljud teised ained, aga tõsi on, et puhtast veest püsivat mulli ei saa. Seebimullide puhumiseks peab pindpinevustegurit vähendama. Seda tehakse pindaktiivsete ainetega. Pindaktiivsete ainete molekuli ehitus on selline, et suur osa neist kogunevad veepinnale, seega ka mullikile pinnale, vähendavad pindpinevustegurit ja veidi ka aurustumist. Mitmesugused pesuained on mullipuhumise juures proovimist väärt.
Tavalised seebimullid ei kesta kaua, enamasti mõned sekundid, harva minuti või rohkem. Lühiealisuse põhjuseks on eelkõige aurustumine ja voolamine. Mullid lihtsalt kuivavad nii õhukeseks, et vedelikukihi sisemine ja välimine külg saavad kokku. Kui õhk on mullist välja pääsenud, püüdleb seebikilet moodustanud vedelik jällegi minimaalse pindala poole, moodustades ideaaljuhul kerakujulise tilga. Tegelikult moodustub küll mitmete kõrvalnähtuste tõttu mitu tilka, aga kerakujulised saavad need igal juhul. Ka raskusjõud on seebimullide vaenlane. Mulli sisemise ja välimise vedelikupinna vahel peab olema piisav seebivee kiht. Kahjuks kipub vesi allapoole voolama, mull jääb ülalt liiga õhukeseks ja lõhkeb. Siiski on võimalik seebivee koostist parandades ja keskkonda niiskena hoides seebimulle säilitada mitmeid päevi, isegi kuid.
Seebikile on ilus füüsikaline analoog matemaatikas tuntud minimaalse pindala probleemile. Kui seebikile mõlemal küljel on sama rõhk, siis kile ei kõverdu. Kui keerata traadist rõngas, kasta see seebivette ja hoida tuuletus õhus, on saadud seebikile täiesti tasane. Mulli korral on aga seebikilesse suletud teatud kogus õhku, rõhk mulli sees on suurem kui väljas ja pind on sfääriline. Juba antiikajast on teada, et kera on sama ruumalaga kujunditest vähima pinnaga, aga selle matemaatilise tõestamiseni jõuti alles 19. sajandil. Matemaatiliselt päris keerukaks osutub pindala küsimus siis, kui mitu mulli kohtuvad. Alles 2000. aastal sai kahe mulli probleem lahenduse, minimaalse pindala reegel kehtib ka sel juhul. Võrdse ruumalaga mullide vaheline seebikile osa on tasase ketta kujuline. Kui mullid ei ole ühesuurused, kumerdub ühine pind suurema mulli poole.
Paljude mullide ühinemisel tekib vaht. Mullide paiknemist vahus kirjeldavad lisaks minimaalse pindala nõudele veel mõned lihtsad reeglid pindade ja nurkade kohta (Plateau seadused).
Siinkohal lõpetame pinnanähtuste teema. Mulliteaduse nüansid ei ole sellega sugugi ammendunud. Kirjeldamata jäid antimullid, omapärane nähtus, kus ühte uurimisobjekti on seotud nii tilga kui ka mulli omadused. Antimulle võib märgata vedelikus hõljuva või pinnal libiseva tilgana, mida eraldab väliskeskkonnast õhuke gaasikiht. Seebimullidele on nad tõesti vastandid. Samuti ei jõudnud rääkida ilma mullideta keemisest. Sellest, kui veetilk kukub kuumale pliidile ja kiiresti ringi kihutades keeb iseendast tekkiva auru padjal ära, ilma et tekiks keemisel iseloomulikku mullide kerkimist. Eraldi kursust vääriksid pinnanähtuste rakendused tehnikas ja tähtsus looduses, sulamine, keemine, tilkumine, mullitamine või vahutamine kaaluta olekus ja palju muud huvitavat.
Nüüd, kui teame juba üsna palju aine erinevatest olekutest ja faaside vahelisest piirpinnast, võib veelkord tagasi tulla faasisiirete juurde, kõigepealt aine agregaatolekute muutumise teemasse.
Ühe konkreetse aine olekuid (laiemalt võttes kõiki faase) võib kujutada arvteljel, nagu külili asetatud termomeetril (joonis 1.9.1.). Sellel arvteljel on kaks olulist punkti, A) sulamis- ja tahkumistemperatuur; B) keemis- ja kondensatsioonitemperatuur. Need temperatuurid on aineti erinevad ja seepärast on igal ainel vedela oleku vahemik erineva pikkusega ja erinevas kohas.
Selline pilt (joonis 1.9.1.) kehtib ainult muutumatu rõhu korral, sest sulamistemperatuur ja eriti keemistemperatuur (joonis 1.2.2.) sõltuvad välisrõhust. Näiteks vee korral on atmosfäärirõhul sulamistemperatuuri ja keemistemperatuuri vahe 100 kraadi. Kõrgemal rõhul on see vahe pikem, madalamal lühem. Et saada täit pilti aine olekute muutustest kõigil rõhkudel, ei piisa ühest arvteljest. Kui aga lisada joonisele 1.9.1. veel sulamise ja keemise andmeid kõrgematel ja madalamatel rõhkudel, saame aine olekute graafilise esituse, mida nimetatakse olekudiagrammiks (joonis 1.9.2.). Olekudiagrammi kõverad kujutavad tingimusi, kus toimub üleminek ühest olekust teise. Tahke ja vedela oleku vahel on sulamiskõver, vedela ja gaasilise piiril on keemiskõver, tahket ja gaasilist olekut eraldab sublimatsioonikõver. Keemiskõveral on keemistemperatuurid erinevatel rõhkudel, sulamiskõveral sulamistemperatuurid erinevatel rõhkudel. Kõverate vahele jäävad alad vastavad tingimustele (rõhk ja temperatuur), mille juures aine on gaasilises, vedelas või tahkes olekus.
Tavaliselt on ainete nii keemis- kui sulamiskõver kaldu kõrgemate temperatuuride poole, aga keemiskõvera kalle on suurem, st et rõhk mõjutab keemist rohkem kui sulamist. Igal diagrammil on üks punkt, kus kõverad kohtuvad. Kuna selles punktis kohtuvad ka aine kolme olekut (gaasilist, vedelat ja tahket) kujutavad diagrammi alad, siis on selle nimi kolmikpunkt.
Kui aine temperatuur ja rõhk on faasidiagrammil sulamiskõveral, võib aine korraga olla tahkes ja vedelas olekus, näiteks jääkuubikud vees. Keemiskõverale vastavatel tingimustel esinevad korraga gaas ja vedelik, näiteks aurumullid keevas vedelikus. Kolmikpunkti tingimused võimaldavad ainel olla korraga kolmes olekus. Keevas vedelikus on siis koos nii aurumullid kui ka tahkise tükid. Igapäevaelus me sellist olukorda ei kohta, sest sellised tingimused on üsna haruldased. Igal ainel on ju ainult üks kolmikpunkt. Me elame atmosfääris, mille rõhk on üsna püsiv, umbes üks atmosfäär (1 atm=101325 Pa). Kui me leiaks aine, mille kolmikpunkt on atmosfäärirõhul ja jääb ka elukeskkonna tavalisse temperatuurivahemikku, oleks tõesti võimalik kolme olekut korraga ühes nõus vaadelda. Lihtsate tehniliste vahenditega võib sellise olukorra saavutada veega, meie lemmikainega (joonis 1.9.3.).
Keemiskõveral on veel üks eripära kõrgel temperatuuril ja suure rõhu all. Gaas ja vedelik erinevad tiheduse poolest, vedelike tihedus on suurem. Vedelikud paisuvad kuumutamisel ja nende tihedus väheneb. Teiselt poolt suureneb gaaside tihedus kokkusurumisel. Nii juhtubki, et keemiskõver katkeb ühes punktis, mida nimetatakse kriitiliseks. Sellest punktist edasi pole enam võimalik kokkusurutud gaasil ja paisunud vedelikul kindlat vahet teha. Vastuseta jääb küsimus, kas tegemist on vedeliku tiheduseni kokku surutud gaasiga või gaasisarnaseks paisunud vedelikuga. Ülekriitilises voolises ei saa olla olekutevahelist piirpinda. Pajude tuntud gaaside kriitiline temperatuur on üsna madal. Näiteks metaani (maagaasi) kriitiline punkt on T= 190,7 K (−82,5 °C), p = 46 bar (45,4 atm). Sellest on näha, et igapäevastel temperatuuridel ei saa muuta maagaasi kokkusurumisega pärisvedelikuks. Küll aga saab seda teha jahutamisega.
On üsna loogiline arvata, et ained, mida me gaasideks nimetame, veelduvad madalal temperatuuril ja lõpuks väga-väga madalal temperatuuril tahkuvad. Sellel arvamusel on tõepõhi all, kuid siingi ei saa mööda rõhu küsimusest. Tõepoolest, paljud gaasid veelduvad atmosfäärirõhul, mõned neist väga madalal temperatuuril. Vesiniku keemistemperatuur on 20,28 K (−252,87°C), heeliumil koguni 4,22 K (−268,93°C). Veeldumise mõttes on erandiks ained, mille kolmikpunkt on tavalisest õhurõhust kõrgemal. Sellistest gaasidest ilma rõhku tõstmata vedelikku ei saa. Tahkumise osas jääb erandiks heelium. Ülimadalatel temperatuuridel ilmutab heelium ootamatuid füüsikalisi omadusi (näiteks ülivoolavus) ja tahkeks ta atmosfäärirõhul ei muutugi. Tahke heeliumi saamiseks on vaja rõhku tõsta.
Süsihappegaasi me tunneme igapäevaelus gaasina, tal on isegi vastav nimi. Olekudiagrammi (joonis 1.9.2.) atmosfäärirõhu horisontaali vaadates märkame, et atmosfäärirõhul süsihappegaas ei veeldu (ei kondenseeru vedelikuks), kuitahes osaval jahutamisel. Võib tunduda, et me just seepärast nimetame teda gaasiks, aga päris nii see siiski ei ole. Paljud ained, mida me ikka ja ainult gaasidena tunneme, veelduvad ja tahkuvad üsna sarnaselt veega, st kolmikpunkt on neil allpool atmosfäärirõhku. Näiteks lämmastik veeldub temperatuuril −195,79°C ja tahkub −210°C juures ilma rõhku muutmata.
Kolmikpunktist allpool, st madalmatel rõhkudel ei ole temperatuuri muutmisega võimalik ainet vedelaks muuta. Süsihappegaas (kolmikpunkt T=216,6 K, p=518kPa) on atmosfäärirõhul ainult gaasiline või tahke. Temperatuuril −78,5°C moodustab süsihappegaas härmatise (süsihappelume), mis samal temperatuuril sublimeerub, kui teda soojendada. Soojendamiseks ei ole muidugi vaja muud kui hoidmist toasoojas õhus. Tegelikult on isegi korralik talvepakane tahkunud süsihappegaasile „liiga soe”. Vedelas olekus võib süsihappegaas olla kõrgemal rõhul, nii teda balloonides hoitaksegi. Väljalaskmisel vedelik aurustub ja sellest tuleneva jahtumise tõttu osa tahkub, moodustades süsihappelume, mille pressimisel saadakse nn kuiv jää.
Oleme jälle mitmel korral võtnud näiteks jää, vee ja veeauru. Vee kolmikpunkt on atmosfäärirõhust madalamal, kõik kolm olekut meile hästi tuttavad ja selles mõttes on vesi hea näide. Kuid sellel, niigi erilisel ainel, on ka olekudiagramm ebatavaline. Sulamiskõver ei kaldu rõhu tõustes kõrgemate temperatuuride poole, vaid tavaliste olekudiagrammidega võrreldes nö vales suunas.
Me teame, et vee tahkumisega (jäätumisega) kaasneb ruumala suurenemine, mille tõttu on jää tihedus väiksem kui vedelal veel. Jää ujub vee peal, mis on oluline elu tekke ja kliima stabiilsuse seisukohalt, sest pinnajää kaitseb veekogusid põhjani külmumise eest. Sarnane füüsikaline omadus on tõesti väga vähestel ainetel, peale vee käituvad nii räni, vismut ja veel mõned metallid. Kuid veel on teisigi tavatuid omadusi. Näiteks väga suur erisoojus ja see, et kõrgel rõhul on sulamistemperatuur veidi madalam, mitte kõrgem nagu tavalistel ainetel. Selle eripäraga on püütud seletada jää libedust. Jäätunud tänaval kõndides avaldame me jääle rõhku ja seega on saapataldade all sulamistemperatuur madalam. Võiks arvata, et just seepärast sulab osa jääst veeks ja muudab pinna libedaks. Olekudiagrammi vaadates on ilmne, et see seletus paika ei pea. Sulamiskõvera kalle on liiga väike. Isegi päris suur rõhk vähendab sulamistemperatuuri mõne kraadi võrra, aga jää on libe ka väga külma ilmaga ja üsna väikese rõhu (suured saapad, suusad) korral. Jää libedust on püütud seletada hõõrdumisest tingitud sulamisega, aga seegi hüpotees pole kinnitust leidnud. Tänapäeval peetakse kõige tõenäolisemaks, et jää lihtsalt ongi libe aine. Jääkristallide väga õhuke pinnakiht on pidevalt vedelikusarnases olekus ja see teebki ta libedaks. On omamoodi hämmastav, et 21. sajandi algul on nii igapäevase aine omadused jätkuvalt tõsiseks uurimisteemaks.
Olekudiagrammilt näeme, millistel rõhkudel ja temperatuuridel on sama aine erinevates olekutes. Ainete omadused on erinevates olekutes teistsugused. Gaasid ja vedelikud on voolavad, tahkised mitte. Gaasid on kokkusurutavad, vedelikud ja tahkised mitte. Paljud teisedki omadused on eri olekutes erinevad. Kuid sama aine võib tahkes olekus (ja mõnel juhul ka vedelikuna) ilmutada erinevaid füüsikalisi omadusi ainuüksi aatomite erineva paigutuse tõttu. Sel juhul räägime aine erinevatest faasidest (ptk Faasid). Muidugi on ka olekud erinevad faasid, sest kindlate omadustega ainekogus on teistsugusest ainekogusest piirpinnaga eraldatud. Nagu saime koostada olekudiagrammi tingimuste kohta, mille juures on aine teatud olekus, nii saame ka koostada faasidiagrammi.
Paljude ainete korral toimub üleminek ühest olekust teise kindlal temperatuuril. Sulamise, tahkumise, keemise ja kondenseerumise nähtusi kirjeldasime []sulamise, tahkumise, gaaside ja vedelike peatükkides[]. Samuti võib üleminek (siirdumine) ühest faasist teise toimuda kindlal temperatuuril, mida nimetatakse siirdetemperatuuriks. Seejuures ei pruugi muutuda aine olek, küll aga muutub mingi füüsikaline omadus. Faasisiirete energeetilist efekti kirjeldavad siirdesoojused, nagu näiteks sulamissoojus kirjeldab sulatamiseks kuluvat või tahkumisel eralduvat soojushulka.
Tahkete faaside üleminekul (faasisiirdel) on olekumuutusega võrreldes üks küllalt oluline erinevus. Vaatame näitena süsiniku faasidiagrammi, joonis 1.9.6. Sulamis-, keemis- ja sublimatsioonikõver on üsna sarnased sellega, mida nägime olekudiagrammil (joonis 1.9.2.). Tahke oleku kohale on märgitud grafiit ja lisaks väga kõrgel, ülisuurte rõhkude piirkonnas on kirjas teemant. Teemandid on täiesti olemas atmosfäärirõhul ja toatemperatuuril, aga faasidiagramm näitab tavatingimustes ainult grafiiti. Siin ilmnebki tahkete faaside eripära. Nimelt „elavad” mõned faasid päris edukalt võõrastes tingimustes. Süsinik ei muutu kuidagi iseenesest teemandiks, aga kui see on kord juba juhtunud kõrge rõhu toimel, säilitab teemant oma piirpinna ja füüsikalised omadused uskumatu visadusega.
Süsinik käitub ühest faasist teise üleminekul eriliselt, säilitab oma faasi (st piirpinna ja füüsikalised omadused) kaugel väljaspool faasidiagrammis „talle eraldatud ala”. Mitte kõik faasid ei ole nii visad püsima. Näiteks on hästi tuntud tina millel on kaks tahket faasi, α- ja β- tina. Hõbevalge läikega metalliline β-tina muutub madalal temperatuuril halliks pulbriliseks α-tinaks. Tina faasisiire valgest tinast halliks on autokatalüütiline (kord juba alanud üleminek areneb üha kiirenevalt) ja on võimeline teisi esemeid „nakatama”. Sellepärast nimetatakse nähtust tinakatkuks.Tina saab kuumutamisel oma metallilised omadused tagasi, aga tinast valmistatud esemed on nende üleminekute käigus pöördumatult kadunud.
Tinakatku kohta räägitakse uskumatuid lugusid, mille tõepära üle vaieldakse tänaseni. Napoleoni sõdurid olevat kaotanud külmas Vene talves mundrite tinanööbid ja nagu teada, lõppes sõjakäik lüüasaamisega. Polaaruurijatega juhtunud äparduste nimekirjas on tinaga joodetud toidu- ja kütusenõude lagunemised. Kõige rohkem on kirjutatud Robert Falcon Scotti juhitud retkest lõunapoolusele, kus väga külmades tingimustes olevat lagunenud tinaga joodetud kütuse- ja toidunõud. Katk kahjustab kergesti puhast tina, paljud tinasulamid (isegi väikese lisandiga) on üsna külmakindlad. Tänapäevased mürgiste metallide (plii, kaadmiumi, antimoni) kasutuspiirangud on puhta tinaga jootmise uuesti ausse tõstnud, kuid see võib tekitata probleeme külma käes töötavas elektroonikas.
Tehisteemantide saamise plaani pidasid teadlased juba 18. sajandi algul, kohe pärast seda, kui sai selgeks, et teemant on lihtaine, puhas süsinik. Muidugi oli kaugem lootus valmistada briljantide lihvimiseks sobivaid suuri kive. Teemandi eriline kõvadus pakkus samas tehnilist huvi ja praktilist kasutust leiavad ka pisemad tükid, isegi teemandipuru kulub ära. Looduslikud leiukohad annavad aimu sellest, et kõrge rõhk ja temperatuur on teemantide tekkimisel olulised olnud. Nii proovitigi grafiiti mitmesugusel viisil kuumutamise, pressimise ja jahutamisega teemandiks muuta. Mitmed katsed kuulutati õnnestunuks, aga korduskatsed äpardusid alati. Praegused teadmised aine ehitusest panevad meid uskuma, et varasemates katsetustes saadi küll huvitavaid kristalle, aga teemandid need siiski ei olnud. Esimeste tehisteemantide valmistamiseni jõuti alles 20. sajandi keskel. See on küll selgelt tagantjärele tarkus, aga faasidiagrammi vaadates on nüüd ilmne, et kui lihtsalt väga suure rõhuga teemandid ei teki, siis võiks oodatud tulemuseni „hiilida” läbi vedela või gaasilise oleku. Tegelikult osutus teemantide tootmine tehniliselt palju keerulisemaks, seostudes näiteks süsiniku lahustumisega vedelates metallides. Tänaseks on mitu oleku muutusega seotud tehnoloogiat osutunud edukaks. Tehnilise teemandipuru tootmine on isegi nii odav, et igaüks võib mõõduka hinna eest osta ehituspoest teemantsae või teemantpuuride komplekti.
1895. aastal avastas Röntgen tundmatud kiired, mis paistsid asjadest läbi, isegi inimesest läbi. Esimest korda ajaloos sai elava inimese sisse piiluda ilma teda lahti lõikamata. Röntgenist sai Nobeli füüsikapreemia esimene laureaat. Tundus, et teadus saadab korda imesid. Teaduse populaarsuse laineharjal kogusid uue sajandi algul kiiresti tuntust ka radioaktiivsus ja raadium. Raadium kujunes müügiargumendiks. Pea kõigesse võis lisada raadiumi, see nägi etiketil välja kaasaegne ja teaduslik. Raadiumvärvid pidid kindlasti olema paremad kui tavalised, kuigi enamasti seal raadiumi polnud, lihtsalt nimi maksis. Väga kasulikuks ja populaarseks osutusid radioluminofoorid, värvid, millesse segatud radioaktiivne aine pani need helendama.
1917. aastal võttis US Radium Corporation erinevatesse ametitesse tööle umbes 70 naist, kellest osa hakkasid tööle nn raadiumvärviga. Helenduva värviga kaeti kellade ja näidikute numbrilaudu ning osuteid. Peene töö jaoks kasutati pisikesi kaamelikarvadest pintsleid. Et pintsli ots oleks täpse joonistamise jaoks terav, niisutasid töötajad seda suus. Umbes samal ajal töötas erinevates USA ja Kanada ettevõtetes sellel tööl ligi 4000 inimest. Radioaktiivsete ainete ohtlikkus oli sel ajal juba teada. Ladudes ja laborites hoiduti hoolega kokkupuutest raadiumiühenditega ja kasutati kaitseriietust. Värvimistöö juures aga veendi töötajaid, enamuses noori naisi, et kõik on ohutu. Esines juhtumeid, kus tüdrukud värvisid helendava seguga küüsi, ehteid, juukseid ja vähemalt ühel juhul isegi hambaid.
Tagajärjed olid kohtavad. Töötajate tervis halvenes kiiresti, neid vaevasid erinevad haigused. Paljud surid, täpset arvu ei ole teada. 1927. aastal pöördusid viis raskesti haiget endist töötajat kohtusse tervisele tekitatud kahju eest kompensatsiooni saamiseks. Kohtuprotsess osutus keerukaks, kestis kaua ja kajastus laialt ajakirjanduses. Kas raadiumitüdrukute kohtuasi muutis teadlaste ja kogu ühiskonna arusaamu aatomifüüsikast ja selle rakendustest?
Eelmises osas oli palju juttu aatomite ja molekulide vahelistest jõududest. Mitmed nähtused osutusid nii päris hästi kirjeldatavaks, ilma et me oleks suuremat tähelepanu pööranud aatomi koostisele ja siseehitusele. Muidugi me teame seda, et aatom koosneb tuumast ja elektronkattest. Ilma selleta poleks kuidagi olnud võimalik hakkama saada põhikooli füüsikatundides ja läbida keemiakursusi. Ka elektromagnetismi, optika ja elektrienergia teemades oli juttu elektronidest. Nüüd ongi aeg küsida, kuidas aatom koos püsib ja kuidas paiknevad seal elektronid? Selgub, et aine ehituse saladused ei ole avanenud loodusteadusele kergelt ja aatomi täpsem kirjeldamine ei ole kuigi lihtne ülesanne.
Aatom on küll nime järgi jagamatu (kreeka keeles atomos - jagamatu), aga hiljemalt 19. sajandi lõpuks oli füüsikutele selge, et tõeliselt jagamatu ta olla ei saa. Üheks vihjeks aatomi siseehitusele oli valguse mõju elektrilaenguga kehadele. 1887. aastal avaldas Heinrich Herz artikli sellest, et elektrisädemete tekkimist soodustab laetud kehadele langev ultravioletne valgus. Järgnevatel aastakümnetel uuriti nähtust (joonis 2.1.1.) väga põhjalikult ja see sai nimeks fotoefekt. Vaatamata kõigile pingutustele õnnestus fotoefekti ainult täpselt kirjeldada, mitte põhjendada.
19. sajandi lõpuaastatel tehti mitu avastust, mis viisid aatomiehituse mõistmisele tublisti lähemale. 1895. aastal avastas Wilhelm Röntgen senitundmatu kiirguse, x-kiired, mida hakati mõnel pool nimetama avastaja nime järgi röntgenikiirteks. Otsides fosforessentsi seotust Röntgeni avastatuga, märkas Henry Becquerel 1896. aastal, et uraaniühendid kiirgavad iseeneslikult veel üht uut kiirgust. Kiirgumine ei sõltu välistingimustest ja sellega ei kaasne keemilisi muutusi. Marie Skłodowska-Curie ja Pierre Curie eraldasid uraanimaagist uued, palju suurema kiirgusvõimega elemendid, polooniumi ja raadiumi. Nähtus sai nimeks radioaktiivsus. 1897. aastal avastas J.J. Thomson esimese aatomist väiksema osakese, mida hiljem hakati nimetama elektroniks. Aastal 1900 esitas Max Planck kvanthüpoteesi ja põhjendas, miks kuumemad kehad kiirgavad keskmiselt lühema lainepikkusega (sinisemat) valgust. Kvanthüpoteesi keskseks ideeks on, et valgus kiirgub ja neeldub väikeste portsjonitena, elementaarsete mõjukvantidena. Ühe kvandi energia on seotud valguslaine sagedusega. Kvandi energia () on väga väike, sagedust () ja energiat seob Plancki konstant:
Kvanthüpotees ühendab valguse lainelist ja korpuskulaarset käsitlust, siiamaani olid need mitu sajandit rivaalitsenud.
Kvantide tegelik olemasolu ei olnud algul kindel, seega oli teooria hüpoteesiks nimetamine põhjendatud. Ometi osutus kvantide idee väga viljakaks. 1905. aastal ilmus Albert Einsteini fotoefekti teooriat elektronide ja kvantide kaudu seletav artikkel.
| Joonis 2.1.1. Fotoefekti on võimalik demonstreerida üsna lihtsate vahenditega. Elektroskoobiga saab vaadata, kuidas negatiivse laenguga tsinkplaat kaotab laengu ultraviolettvalguse toimel. Tavalise lambiga valgustamine ei toimi. Positiivse laenguga plaadile ei mõju ei tavaline ega ultraviolettlamp. | Eriti lihtsate vahenditega läbi viidud fotoefekti katse. Alumiiniumpurgiga katses on vaja UVC-lampi (λ < 280nm). |
Vaatame üht lihtsat fotoefekti näidet (joonis 2.1.1.). Ultravioletse valguse toimel kaotab metallplaat negatiivset laengut, aga positiivset mitte. Teades, et negatiivset laengut kannavad elektronid, võime tänapäevaste teadmiste alusel öelda, et valgus sunnib vabu elektrone ainest väljuma. Kuna positiivse laenguga metallis ei ole vabu negatiivseid ega ammugi mitte vabu positiivseid laengukandjaid, siis sel juhul pole valgusel midagi ainest välja lüüa. See lihtne ja paikapidav seletus jätab vastuseta mitu fotoefekti katseliselt kindlaks tehtud iseärasust:
- Fotoefekt tekib enamasti ultravioletse valguse toimel. Pikemalaineline kiirgus (näiteks punane valgus või soojuskiirgus) ei suuda elektrone ainest välja lüüa. Piiri, millest lühema lainepikkusega kiirgus on võimeline fotoefekti tekitama, nimetatakse punapiiriks. Punapiir on aineti erinev ja ei sõltu pinnale langeva valguse intensiivsusest. Kui nõrk ultravioletne valgus tekitab fotoefekti, siis isegi väga ere punane valgus seda ei tee.
- Ainest valguse poolt väljalöödud fotoelektronide energia on erinev, aga pole kunagi teatud piirväärtusest suurem. Valguse intensiivsuse suurendamine ei suuda kuidagi väljunud elektronide maksimaalset kiirust (st kineetilist energiat) suurendada, küll aga teeb seda lainepikkuse vähendamine.
Kui käsitleda valgust elektromagnetlainena, pole võimalik nimetatud katseandmeid seletada. Näiteks suurem valgustatus (eredam valgus) kannab ainesse rohkem energiat ja peaks seetõttu fotoelektronidele suurema kiiruse andma. Katseandmed näitavad aga, et suurema kiiruse annab hoopis lühem lainepikkus. Einstein rakendas oma 1905. aasta artiklis Plancki kvanthüpoteesi, käsitledes valgust energiakvantidena (saksa keeles - Energiequant. Lichtquant). Tänapäeval räägime valgust osakeste voona käsitledes kvantidest või footonitest. Ühe kvandi energia läheb ühele elektronile. Selline lähenemine lahendas fotoefekti mõistatuse ja ühtlasi veenis füüsikuid, et kvandid ei ole tühipaljas hüpotees.
Tänapäeval esitatakse fotoefekti teooria kokkuvõtlikult ühe töö ja energia valemina:
- Võrdusmärgi ees on aines neelduva valguskvandi energia. kus on Plancki konstant () ja on sagedus. See lihtne valem kirjeldab valgust dualistlikult, ühelt poolt kvandi ehk footonina energia kaudu, teiselt poolt lainena sageduse kaudu. Tasub märkida, et kvantide energiad on väga väikesed. Näiteks ultraviolettvalgus, mille lainepikkus on 273 nm (st sagedus on 1,1·1015 Hz) kiirgub ja neeldub kvantidena, mille energia on 7,26·10-19 J (4,53 eV).
- Teisel pool võrdusmärki on see, mis neeldunud kvandist saab. A tähistab valemis elektroni metallist väljalöömiseks vajalikku tööd, seda nimetataksegi väljumistööks. Kui footonitel on energiat vähem, kui kulub väljumistööks, siis fotoefekti ei teki. Kui footonitel on energiat rohkem, siis saavad elektronid metallist välja ja lisaks veel teatud kineetilise energia. Valemis on elektroni kineetiline energia kus on elektroni mass ja v elektroni suurim võimalik kiirus.
Väljumistöö on aineti erinev. Vase väljumistöö ACu=7,2·10-19J (4,7 eV), sellise energiaga on ultravioletse valguse kvandid. Kaaliumi väljumistöö AK=3,7·10-19J (2,3eV), fotoefekti tekitab isegi nähtav valgus.
Võib öelda, et Einsteini fotoefekti teooria esitab energia jäävuse seaduse mikromaailmas, aatomite ja mingil määral isegi elektronide tasandil.
Vaatame veelkord juba kirjeldatud näidet, fotoefekti tsinkplaadis ultravioletse valguse toimel (joonis 2.1.1.). Iga ultraviolettkiirguse kvant () kannab energiat:
Kvanthüpoteesi iva on selles, et kvandi energia ei saa jaguneda mitmele elektronile, sest kvandid on elementaarsed, neid ei saa vähemateks osadeks jagada.
Väljumistöö sõltub tsingi pinna kristallstruktuurist ja puhtusest. Igal konkreetsel plaadil võib olla veidi erinev väljumistöö, näitena jääme levinud keskmise väärtuse juurde:
Nii palju energiat kulub ühe elektroni ainest väljalöömiseks. Väljunud elektronide kiirendamiseks ehk nende kineetilise energia suurendamiseks jääb:
Sellest pisikesest energiast piisab, et anda elektronile kiirus, mis võib olla kuni:
Fotoefekti avastuslugu ja esimesed rakendused olid seotud välisfotoefektiga, nähtusega, kus elektronid valguse toimel tõesti väljuvad tahkest ainest gaasi või vaakumisse. Ainest väljunud elektronid, kui need elektrivälja abil liikuma panna, moodustavad fotovoolu, mida saab mõõta ja mitmel moel rakendada. Tänapäeval on fotoefektil palju rakendusi, mis põhinevad enamasti sisefotoefektil. Sisefotoefekti korral valgus küll vabastab elektronid, annab neile võimaluse liikuda, aga ei vii neid ainest välja. Neeldunud valguskvantide energia annab võimaluse viia elektronid samas ainetükis teise kohta, tihti teise kihti. Nii töötavad näiteks päikesepaneelid ja fotoaparaatide sensorid.
Õppisime Füüsikalise looduskäsitluse aluste kursuses, et kogu meile teadaolev universum koosneb ainest ja väljast. Ainel ja väljal on väga erinevad omadused. Näiteks mingi osakene asub ruumis kindlas kohas ja tal on kindlad mõõtmed. Aga väljal, mida see osake tekitab, ei ole mõõtmeid, see levib lainetena üle kogu ruumi.
Oleme ka rääkinud, et atomistlik printsiip kehtib ka väljade kohta. Makromaailmas pidevana tunduv väli osutub mikrotasemel samuti koosnevaks jagamatutest osakestest, mida nimetatakse välja kvantideks.
Käesolevas peatükis me uurime elektromagnetlaineid ning sellega seoses tutvume veel ühe looduse fundamentaalse printsiibiga. Selgub nimelt, et ühelt poolt saab loodust kirjeldada ainena (osakestega), mida võib põhimõtteliselt "näha ja katsuda". Teisalt saab neidsamu nähtuseid kirjeldada ka väljadega, mida pole näha, kuid mis vahendavad osakeste vahel mõjuvaid jõude. Sellist omaduste kahesust nimetatakse dualismiks (lad duo – kaks). Looduses vastab igale lainele osake ja iga osakesega kaasneb laine. Näiteks elektrone, mida me oleme joonistel harjunud nägema ümber aatomi tuuma tiirlevate pallikestena, saab kirjeldada ka lainete abil (selliseid laineid nimetatakse ka De Broglie laineteks).
Ka valgust saab kirjeldada kaheti. Siiani oleme rääkinud valgusest kui elektromagnetväljast, mis levib ruumis lainena. Selgub aga, et valgust saab kirjeldada ka osakeste abil, nimelt on olemas valguse osakesed ehk kvandid. Valguse kvanti nimetatakse footoniks (kr phos – valgus).
Footonitest oleme juba rääkinud kursuses Füüsikalise looduskäsitluse alused. Sealt saime teada, et footon on osake, millel seisumass on võrdne nulliga, see tähendab, et paigalolekus footon olla ei saa. Teisiti öelduna: kui footon peatatakse, siis muutub ta millekski muuks, tema energia muutub mõneks teiseks energialiigiks.
Valguse kvantiseloom ilmneb selgemalt valguse kiirgumisel (tekkimisel) ja neeldumisel (kadumisel). Laineline olemus tuleb esile peamiselt valguse levimisel.
Valguse lainelised ja korpuskulaarsed (osakesetaolised) omadused ühendas omavahel M. Planck 1900. aastal, kui ta võttis kasutusele valemi
kus on footoni energia, vastava valguslaine sagedus ja võrdetegur, mida tuntakse Plancki konstandina: TeX parse error: '\cdot' is only supported in math mode. Toodud valem kehtib kõigi elektromagnetlainete korral, mitte ainult valguse puhul.
Ühe footoni energia on nii väike, et seda otseselt mõõta on võimatu. Näiteks sääse ühe tiivalöögi energia on keskmiselt 1012 (miljon miljonit) korda suurem footoni energiast.
Footonite olemasolu tõestati fotoefekti katsetega. Fotoefektiks, täpsemalt välisfotoefektiks nimetatakse elektronide väljalöömist ainest (J.3.8, a). On olemas ka sisefotoefekt, mille korral valgus lööb elektrone välja keemilistest sidemetest aatomite vahel, aga elektronid ainest ei välju. Sisefotoefekt on näiteks päikesepatareide töö aluseks.
Välisfotoefekti uurimiseks kasutame katseseadet, mille skeem on toodud joonisel. 3.8 b.
Katsete tulemused võib kokku võtta järgnevalt:
- Kui elektroskoobiga ühendatud metallplaat laadida negatiivselt, siis selle valgustamisel kaob laeng mõne aja jooksul
- Kui plaat laadida positiivselt, siis laeng valguse toimel ei kao
- Kui me plaati üldse ei lae, siis valguse toimel plaat ei laadu
- Kui asetada valguse teele klaasplaat, siis ei kao ka negatiivselt laetud plaadi laeng
Teeme katsetest järeldused.
Esimene katse näitas, et valguse toimel kadus plaadilt elektrilaeng. Kuna negatiivse laengu kandjad on elektronid, siis võib järeldada, et valgus lõi plaadist välja elektrone.
Viimane katse aga näitas, et kui valguse teel oli klaasplaat, siis ei löödud plaadist elektrone välja. Põhjus on selles, et klaas laseb läbi ainult nähtavat valgust, aga mitte ultravalgust. Järelikult mitte igasugune valgus ei vabasta elektrone, vaid ainult suurema kvandienergiaga valgus ehk ultravalgus. On ju ultravalguse sagedus suurem kui nähtaval valgusel ja seega on ultravalgusel ka suurem kvandienergia. Tuleb märkida, et välisfotoefekt võib esineda üksikute ainete korral ka nähtava valguse toimel.
Kui plaat polnud laetud, siis valguse toimel ei laadunud sellepärast, et väljalöödud elektronid tõmmati plaati tagasi. Põhjus on selles, et enne oli plaadis elektronide negatiivsete laengute ja prootonite positiivsete laengute summa null. Aga elektronide lahkudes jäi ülekaalu prootonite positiivsete laengute summa ja plaat omandas positiivse laengu.
Kui plaat juba on positiivselt laetud, siis tõmmatakse väljalöödud elektrone plaati tagasi veel tugevamini kui laadimata plaadi korral.
Välisfotoefekti avastas 1887. aastal H. Hertz, kui ta uuris elektroodide vahel tekkivat sädelahendust. Ta märkas, et säde tema elektromagnetlainete tekitamiseks loodud katseseadmes tekkis paremini, kui elektroode valgustada. Põhjalikumalt uuris efekti A. Stoletov 1888. aastal. Kuid nemad ei osanud nähtust seletada. Seda tegi A. Einstein footonite abil 1905. aastal ja talle anti selle eest 1921. aastal Nobeli füüsikapreemia. Einsteini teooria sisu võtab kokku valem, mida tuntakse kui Einsteini valemit fotoefekti kohta.
kus on Plancki konstant, – valguse sagedus, – väljumistöö (töö, mida peab valguskvant tegema, et vabastada elektron positiivsete ioonide tõmbejõududest), – elektroni mass ja – vabanenud elektroni kiirus.
Nägime, et valgusnähtusi seletatakse nii lainete kui kvantide abil. Sageli öeldaksegi, et valgus on olemuselt dualistlik ehk kahene. Täpsem oleks öelda, et mitte valguse olemus ei ole dualistlik, vaid dualistlik on meie käsitlus valgusest: mõnede nähtuse juures avaldub valguse laineline olemus, teiste korral kvantolemus.
Valguse laine- ja kvantteooriad ei ole vastandlikud, nad täiendavad teineteist. Mida see tähendab? Aga seda, et kui me käsitleksime valgust kui ainult elektromagnetilist lainet, siis jääks meile mõistetamatuks mitmed valgusega seotud nähtused nagu juba eespool mainitud fotoefekt või valguse rõhk. Siis oleks leiutamata ka laserid ja kõik nendega seotu alates laserite kasutamisest meditsiinis ja lõpetades CD- ja DVD-mängijatega. Ja kui me käsitleksime valgust kui ainult footonite voogu, siis oleks meil keerulisem seletada valguse difraktsiooni ja interferentsiga seotud nähtuseid.
Mida väiksem on elektromagnetlaine sagedus , seda väiksem on ka kvandi energia , sest . Ja ühe kvandi energia võib olla nii väike, et meil ei ole võimalik seda avastada. Näiteks raadiolainetel, sagedusega 100 MHz, on ühe kvandi energia nii väike, et raadios registreeritava signaali tekitamiseks peab antennini jõudma vähemalt 1010 kvanti sekundis. Sellise osakeste arvu puhul on võimatu neid üksteisest eristada ja neid võib käsitleda lainena.
Ka veelaine koosneb ülipaljudest veemolekulidest, aga keegi ei räägi veeosakeste liikumisest, vaid ikka veelainest.
Kuid suure sagedusega elektromagnetlainete, näiteks γ-kiirguse korral on nende lainelisi omadusi raske märgata. Sel juhul käitub kiirgus pigem osakese kui lainena. Näiteks juba ühest γ-kvandist piisab, et esile kutsuda tuumareaktsiooni nagu seda võib teha ka mingi osakene, näiteks neutron.
Valgusel, mis on sageduste poolest raadiolainete ja γ-kiirguse vahepealne, avalduvad nii lainete kui osakeste omadused. See on aga ebatavaline ja harjumatu, sest me ei oska endale midagi taolist ette kujutada. Midagi muud sarnast pole me looduses märganud. Oleme harjunud, et osakene asub ikka mingis kindlas kohas, aga laine täidab mingi osa ruumist. Valguse korral on aga osake ka samal ajal laine ja laine osake. Sellise ebatavalise olukorra põhjuseks on fakt, et inimene ei saa vahetult tajuda valguse olemust.
Isegi tähtsamate fotoefektiga seotud leiutiste veidigi täpsem kirjeldamine vajaks eraldi peatükke, seepärast piirdume ühe lühiseletusega.
2009. aasta Nobeli füüsikapreemia läks jagamisele kahe praktiliste tulemustega teadussaavutuste vahel. Pool preemiast läks jagamisele Willard S. Boyle'i ja George E. Smithi vahel, kes olid leiutanud pooljuhtseadme, mida selleks ajaks tundis juba terve maailm. CCD (charge-coupled device, laengusidestusseadis) lõi digifotograafia ja tegi nähtavaks seni vaatlemata jäänud nähtused mikromaailmas, elusorganismides, Universumi kaugustes jpm.
CCD on kihilise struktuuriga piksliteks jagatud pooljuhtseade, kus fotoelektrone on võimalik koguda augukestesse (joonis 2.1.3.). See kõlab lihtsalt, aga tehniliselt on seade üsna keerukas. Idee pärineb 1960-ndatest, Boyle'i ja Smithi esimesed artiklid ilmusid 1970. Järgnevate aastakümnetega töötati välja sobivad materjalid ja tehnoloogia ülipisikeste pikslite tekitamiseks. Piksli mõõtudest sõltub pildi kvaliteet. Tänapäeval on piksli suurus umbes 10 mikronit (sajandik millimeetrit).
| Joonis 2.1.3. Digipilt tekib pikslitele langevate footonite arvu (valguse intensiivsuse) mõõtmisel väljalöödud elektronide arvuna (kogunenud laenguna) ja tulemuse muutmisel digitaalseks signaaliks. | Joonis 2.1.4. CCD sensoreid armastavad astronoomid, nende seadmetele on välja töötatud maailma kõige suuremad ja kõige tundlikumad CCD-d. Pildil olev teleskoobisensor on toodetud ettevõttes Spectral Instruments (USA). Ruudukujulise 111,5 megapikslise sensori küljepikkus on ligi 10 cm, see töötab temperatuuril 160 K. |
Max Planckile 1918. aasta Nobeli preemia määramise põhjenduseks olid energiakvantide avastamisega füüsika arengule osutatud teened.
Preemia kätteandmisel 1. juunil 1920 peetud kõnes ütles Rootsi Kuningliku Teaduste Akadeemia president muu hulgas: „Plancki kiirgusteooria on tõesti olulisim teenäitaja kaasaegses füüsikas ja tundub kuluvat veel palju aega, enne kui ammenduvad aarded, mille Plancki geniaalsus on päevavalgele toonud.” On tõsi, et kvantmehaanikast on saanud tähtis kivi tänapäevase füüsika alusmüüris, aga vaevalt osati sel ajal aimata, kui palju selles füüsikaharus veel Nobeli preemiaid antakse ja milliste igapäevaste rakendusteni jõutakse.
Kõigele vaatamata oli Planck ise viimaseid, kes loobus mõttest pöörduda tagasi klassikaliste teooriate juurde. Nii tunnebki teadusajalugu teda kui vastutahtsi revolutsioonilist teoreetikut. Samuti jäi Planck kindlalt maailma juhusliku, tõenäosusliku loomuga toimimise idee oponendiks. See ei klappinud kuidagi tema intuitiivse ettekujutusega vaatleja ja füüsilise maailma suhtest.
Kvanthüpoteesi avaldamise ajal oli Planck 42-aastane ja on mõistetav, et nii suuri avastusi ta rohkem ei teinud, kuigi panustas hiljemgi mitmetesse füüsikaharudesse ja füüsikalisesse keemiasse.
Plancki autoriteet saksa füüsikute hulgas oli suur. Ta oli Preisi Teaduste Akadeemia matemaatika ja füüsika alaline sekretär ning Keiser Wilhelmi ühingu (praegu Max Plancki ühing) president. Kui natsid 1933. aastal võimule tulid ja paljud teadlased riigist lahkusid, jäi Planck Saksamaale, et nii palju kui võimalik hoida tagasi saksa füüsikatraditsiooni hävingut.
Vanemas eas pühendus Planck oma kirjutistes enam filosoofiale, esteetikale ja religioonile. Isiklikud tõekspidamised ja kindel iseloom aitasid tal taluda laste õnnetut surma ning Teise maailmasõja koledusi.
Albert Einstein avaldas 1905. aastal neli teoreetilist artiklit, mis on teadusajaloos nii palju kuulsust kogunud, et seda aastat on hakatud lausa imeväärseks (annus mirabilis) nimetama. 2005. aastal, kui sellest tähelepanuväärsest saavutusest möödus sada aastat, tähistati rahvusvahelist füüsika aastat meenutamaks nende kaasaegse füüsika loomisele oluliselt kaasa aidanud tööde ilmumist.
Aastail 1902 – 1909 töötas Einstein Šveitsis Berni patendibüroo ametnikuna. Tal ei olnud sel ajal eriti head võimalust teadusajakirjade lugemiseks ja polnud ka kuigi palju kolleege, kellega oma teaduslikke ideid arutada. Siiski oli tolleaegne füüsika tippajakiri kättesaadav ja mõned lähemad sõbrad käisid Einsteini juures füüsika ja filosoofia probleeme arutamas.
Neli imelise aasta artiklit käsitlesid footoneid, Browni liikumist, massi ja energia seost ning erirelatiivsusteooriat. Tänapäeval kiputakse arvama, et iga töö neist neljast olnuks Nobeli preemiat väärt, relatiivsusteooria eriti. Einstein sai 1921. aasta Nobeli preemia „teenete eest teoreetilise füüsika vallas ja eriti fotoefekti seaduse avastamise eest”. Miks siis ikkagi fotoefekt, mitte relatiivsusteooria või mõni muu eriline teene? Preemia kätteandmisel peetud kõnes mainis Nobeli Komitee esimees lühidalt relatiivsusteooria ümber käivaid filosoofilisi vaidlusi ja Browni liikumise teooria vastu esimestel aastatel tekkinud suurt huvi. Massi ja energia seos jäi üldse mainimata, selle aeg polnud veel kätte jõudnud. Fotoefekti teooria ja footonite teema said palju kiitust kui teedrajavad suunad teaduses. Sel ajal tuli ridamisi esile teadussaavutusi ja avastusi, kus kvantteooria leidis eksperimentaalset kinnitust ja laia rakendust. Võib arvata, et Nobeli komiteel ei olnudki valikut, mida kõige erilisemaks pidada.
Atomismi idee pärineb antiikajast ja pikkadeks sajanditeks jäigi see ainult ideeks. Eksperimentaalsed meetodid arenesid alles 19. sajandil nii kaugele, et sai võimalikuks tõsiselt rääkida aatommassidest ja aatomite mõõtmetest. Samal ajal paranes jõudsalt arusaamine aatomitest, molekulidest ja keemilistest reaktsioonidest seoses keemiateaduse ning keemiatööstuse arenguga. 1870. aastaks sai esialgsel kujul valmis Mendelejevi tabel, aga selles kajastuvat elementide keemiliste omaduste perioodilisuse seadust polnud võimalik kuidagi põhjendada. Aatomite olemasolu ja ka see, et aatomid pole päris jagamatud, sai 20. sajandi algul üha rohkem kinnitust, aga esialgu oli lahtine, kus elektronid aatomis asuvad ja kuidas nad seal püsivad.
Aatomeid on sajandeid modelleeritud pisikeste kehakestena, mis koosnevad tundmatu päritolu, koostise ja ka tundmatute omadustega aatomiainest. Aatomi siseehitus ja kuju jäid saladuseks, sest inimese meeleorganid ei võimalda üksiku aatomi vaatlemist. Mingil moel lepime me praeguseni sellesama lihtsa ettekujutusega, kui kirjeldame näiteks soojusliikumist või difusiooni ja paneme värvilistest kuulikestest kokku molekulide mudeleid. Siiski, mudelikomplektis käib näiteks süsiniku kerakese külge alati neil sidet, aga vesinikule üks. See ei saa olla niisama, miski aatomi sees peab olema selle põhjuseks.
1897. aastal avastas J.J. Thomson katoodkiiri uurides esimese aatomist väiksema aineosakese, elektroni. Katoodkiired tekivad hõrendatud gaasiga täidetud klaastorus asuvate pingestatud elektroodide vahel, st tegemist on elektrivooluga hõredas gaasis või vaakumis. Tol ajal oli elektrivoolu olemus suureks mõistatuseks ja katoodkiired tähtis uurimisobjekt. Thomson näitas, et katoodkiired koosnevad negatiivse laenguga osakestest, mis on vesiniku aatomist üle 1000 korra kergemad. Kiiresti sai selgeks, et nii katoodkiirtes kui ka metalljuhtmetes kannavad elektrivoolu just elektronid. Avastus oli ka aatomiehituse alal läbimurdeks. Kuna elektronid võivad kanda aatomist välja negatiivset laengut, aga väga vähe massi, on loogiline arvata, et aatom koosneb põhiliselt positiivse laenguga raskest „aatomitaignast”. Nii pakkuski Thomson 1904. aastal välja esimese teaduslikult põhjendatud aatomimudeli, mida nimetatakse „ploomipudinguks”. Ploomipuding on traditsiooniline inglise jõulutoit, mis ei ole meie köögitraditsioonis eriti tuntud, seepärast on hakatud eesti keeles kasutama nime „rosinakukli mudel” (joonis 2.2.1.). Elektronid on selles mudelis nagu rosinad saias. Nimi ei ole väga õnnestunud, sest elektronid ei püsi paigal nagu rosinad, nad peavad aatomis tiirlema või võnkuma. Liikuvate elektronide kaudu saab põhjendada laengu ülekannet, elektrivoolu ja ka spektrite (erineva lainepikkusega valguse kiirgumise ja neeldumise) seletamiseks on lootust.
Rosinakukli mudel ei pidanud vastu kuigi kaua. Kohe pakuti välja ideid positiivse laengu asumisest aatomi keskel ja juba viie aasta pärast leiti aatomituum katseliselt. Sai selgeks, et ühtlast positiivse laengu pilve aatomis ei ole, rosinakukli mudelis on küll rosinad, aga saia ei ole. Aatomituumast ja sellega seonduvast tuleb juttu tuumafüüsika peatükkides. Aatomi elektronstruktuuri seisukohalt oli tuuma avastamine järjekordseks murdepunktiks. Aatomituum on aatomimõõtudes nii väike ja raske, et analoogia Päikesesüsteemiga on ilmne. Ka Päike on võrreldes planeetidega väga raske ja võrreldes kogu süsteemiga väga väike. Nii saigi uus mudel nimeks planetaarmudel. Analoogia oli tegelikult üsna kaudne. Polnud mingit põhjust arvata, et elektronid tiirlevad tuuma ümber ühes tasandis nagu planeedid ümber Päikese ja elektronid on kõik täpselt ühesugused, mida planeedid sugugi ei ole. Orbiitide idee sisaldus tegelikult juba Thomsoni mudelis, aga nende kuju ja stabiilset asetust isegi tuumaga aatomimudelis ei õnnestunud kuidagi klassikalise füüsika abil ennustada.
Aatomimudelid arenesid 20. sajandi algul väga kiiresti. Juba 1913. aastal avaldas Niels Bohr artiklite triloogia, kus aatomit on kirjeldatud kui positiivse laenguga tuuma ümber erineval kaugusel, kuid ainult kindlatel orbiitidel ringlevaid elektrone. Elektronid võivad ühelt orbiidilt teisele tõusta või langeda. Orbiidivahetusega kaasneb footoni kiirgumine või neeldumine. Lubatud orbiidil asuvad elektronid ei kiirga ega neela energiat, st energiatasemed aatomis on kvanditud. See viimane postulaat on vastuolus klassikalise elektrodünaamikaga. Kerkib küsimus, kuidas ja miks tiirlevad elektronid just lubatud orbiitidel ilma valgust kiirgamata?
Bohri aatomimudel võimaldas seletada vesiniku aatomi spektrijoonte koondumist seeriatesse ja andis päris hea alguse keemilise sideme ning elementide keemiliste omaduste põhjendamisele (joonis 2.2.3.). Kirjeldatud mudel on mingil moel segu klassikalisest ja kvantmehaanilisest käsitlusest ja selles ilmnesid, nagu kõigis eelmisteski, peagi puudused. Näiteks kirjeldub Bohri mudeliga ainult ühe elektroniga aatomi või iooni (eelkõige vesiniku) spekter, teiste aatomite spektrid paraku mitte.
Bohri aatom on esimene mikromaailma mudel, mis ei kasutata analoogiaid makromaailmast. Seepärast ei ole tal, erinevalt eelnevatest, kujundlikku nime. Mitte miski meie igapäevaste kehade maailmas ei käitu nii nagu elektronid aatomis. Elektron võib asuda näiteks teisel või kolmandal energiatasemel, aga ei saa asuda nende vahel. Me kõik võime elada teisel või kolmandal korrusel, aga kui me läheme teiselt kolmandale, oleme alati kasvõi korraks ka korruste vahel trepil. Intuitiivselt on vastuvõetamatu kujutleda, et mingi keha (näiteks elektron) saab kaduda ühelt orbiidilt ja ilmuda või tekkida teisel.
Praeguseks on teada, et elektronid ei liigu orbiitidel nagu kirjeldas Bohri-Rutherfordi aatomimudel. Ometi on see mudel paljudel juhtudel kasutamiskõlblik aatomitega toimuva kirjeldamiseks energiatasemete kaudu. Kui aatomi elektronkiht neelab kiirguskvante, lähevad elektronid suurema energiaga olekutesse. Bohri järgi läksid nad kõrgemetele (tuumast kaugematele) orbiitidele. Kasutades aatomi või molekuli elektronkatte lihtsustatud skeeme, nimetame suurema energiaga olekuid kõrgemateks energiatasemeteks. Joonistatakse neid tihtipeale siiski Bohri orbiitidena, eriti aatomite korral.
(Bohri aatomimudeli täpsema käsitluse leiad Henn Käämbre õpikust)
Bohri aatomimudel võimaldab küll elektronide orbiitide energiaid arvutada, aga ei näita põhjust, miks just need kindlad orbiidid (ehk energiatasemed) on lubatud. Siin tuleb appi dualismiprintsiip. 1924. aastal esitas Louis de Broglie käsitlusviisi, kus kõigi aineliste objektidega kaasneb laine. De Broglie lainepikkus () sõltub osakese impulsist, st massist ja kiirusest.
kus on Planki konstant, - impulss, - osakese mass ja - osakese kiirus. Valemist ilmneb, miks me makrokehade lainelisi omadusi ei märka. Kuna Plancki konstant on väga väike, on tavaliste kehade de Broglie lained käsitamatult lühikesed.
| Joonis 2.2.5. De Broglie laine mehaaniliseks analoogiks võiks olla kahest otsast kinnitatud keele võnkumine, aga veel parem on vaadata võnkuvat rõngast. Rõngal saab püsiv seisulaine tekkida siis, kui sinna sobitub täisarv lainepikkusi. Bohri mudeli orbiite peeti ringikujulisteks ja oli loogiline arvata, et lubatud orbiidid on need, kuhu mahub täisarv elektroni seisulaine lainepikkusi. Kuigi selle laine iseloomu kohta ei olnud veel midagi teada, sobis de Broglie elektronlaine mudelisse väga hästi. | Kass mängib keelpilli |
Niisiis, juba tuntud footonite lainelis-korpuskulaarne dualism (ptk Aatom) laieneb elektronile ja teistelegi osakestele. Seega ei kihuta Bohri aatomimudeli orbiitidel mitte pisikesed kerakujulised elektronid, vaid võnguvad elektronide seisulained. Lubatuks osutuvad need Bohri orbiidid, kuhu mahub täisarv lainepikkusi. Kuigi elektroni laineomadused sobisid aatomimudelisse hästi ja leidsid ka eksperimentaalset kinnitust (ptk Elektronide difraktsioon), peab ka siin esitama mõned küsimused:
- kas elektroniga kaasnevat lainet saab otseselt siduda mõne füüsikalise protsessiga ehk hästi lihtsalt küsides: mis lainetab?
- kuidas tõlgendada laine amplituudi?
Need küsimused viivad meid tagasi peatüki alguses lahtiseks jäänud küsimuse juurde, kus ja kuidas paiknevad elektronid aatomis? Klassikalises mehaanikas vastaks sellele küsimusele liikumisvõrrand. Meenutame näiteks teadusajaloos tuntud Kuu trajektoori probleemi lahendamist 17. sajandil. Newtoni seadused võimaldavad Kuu tiirlemist ümber Maa matemaatiliselt kirjeldada ja arvutada selle asukohta suvalisel ajahetkel. Kvantmehaanilises käsitluses on liikumisvõrrandi analoogiks Schrödingeri võrrand, mis kirjeldab aatomite, molekulide, aga ka aatomiosakeste kvantolekuid. Erinevalt klassikalisest mehaanikast ei ole võrrandi lahendiks elektroni trajektoor või asukoht mingil ajahetkel, vaid leiulaine (lainefunktsioon) (ptk Elektronide difraktsioon). Tuleb leppida, et elektroni asukoha, trajektoori või orbiidi asemel on tõenäosus leida elektroni aatomi, molekuli või kristalli mingis kohas. Leiulaine suurem amplituud vastab suuremale tõenäosusele.
Kvantmehaanika algust seostatakse enamasti Plancki 1900. aasta kvanthüpoteesiga (ptk Einsteini fotoefekti teooria), mis kvantiseeris ainult kiirguse. Teadusajalugu teeb vahet kaasaegsel kvantmehaanikal ja varastel kvantteooriatel. Viimaste hulka loetakse ka poolklassikalised teooriad nagu näiteks Bohri aatomimudel ja isegi de Broglie lained. Kvantmehaaniliste mudelite ja seega ka kaasaegses mõttes kvantmehaanilise maailmapildi alguseks loetakse 1926. aastat, mil Schrödinger avaldas oma võrrandi (ptk Kopenhaageni tõlgendus) De Broglie teoorias oli arvestatud, et osakesega ongi seotud mingisugune reaalne laine. Tegelikult on aineosakeste laineomadus esitatud Schrödingeri võrrandis leiulainena, mis on matemaatiline, tõenäosuslik tõlgendus. Ei saa öelda, et mingi füüsikaline objekt selles lainetab. Vaatamata sellele, et kvantmehaanilised mudeleid on intuitiivselt hoomamatud ja raskesti visualiseeritavad, on kvantmehaanika tänapäeva füüsika üks põhialustest ja paljud füüsika-, keemia- ja bioloogiaharud oleksid ilma kvantteooriata mõeldamatud.
Jah, aatomit võib tänapäeval päris hästi kirjeldada, aga peab arvestama, et nägemisega pole siin kuigi palju pistmist. Elektronide asukohti aatomis kirjeldatakse kvantarvudega. Õigemini kirjeldatakse neid piirkondi, kus elektrone võib leida, st elektronide leiulainete kujusid. Tõrjutusprintsiipi võib makromaailmas seletada nii, et kaks keha ei saa olla samal ajal samas kohas. Aatomi elektronstruktuuris tähendab see, et samas olekus, st sama kvantarvude komplektiga saab aatomis korraga olla ainult üks elektron. Elektronide kvantarve on neli: peakvantarv (), orbitaalkvantarv (), magnetkvantarv () ja spinn ().
Peakvantarv loeb elektronkihte. Elektroni keskmine kaugus tuumast on väikseim esimeses kihis (). Järgmistes kihtides on elektronid tuumast keskmiselt järjest kaugemal. Leiulaine suuremad amplituudid on tuumast kaugemal, suurema tõenäosusega võib elektrone leida tuumast veidi kaugemal.
Kuna kaugemal on ruumi rohkem, siis mahub sinna rohkem elektrone ja alates teisest kihist () jagunevad elektronid alakihtidesse. Igas järgmises kihis on üks alakiht rohkem (alakihte vastavas elektronkihis loendatakse nullist peakvantarvuni, ). Lõplikult määrab elektroni poolt kasutatava territooriumi magnetkvantarv. Magnetkvantarvu väärtused igas alakihis võivad olla . Magnetkvantarvule lubatud pluss- ja miinusväärtused annavad igas järgmises alakihis ruumi veel kahele elektronile. Tuumast kaugemates kihtides võib olla üha rohkem elektrone, sest alakihte on rohkem ja eriti seepärast, et iga järgmine alakiht mahutab rohkem elektrone.
Lisaks on elektronil veel üks omadus, spinn. Spin tähendab inglise keeles pöörlemist ja tihti kujutataksegi elektroni päri- või vastupäeva pöörleva kerakesena. See on liiga piltlik, et olla täpne, aga aatomi elektronstruktuuri kirjeldades võib küll öelda, et ühele leiulainele vastab kaks elektroni, nende spinnid on vastassuunalised. Kokku on igas kihis kohta elektronile.
Perioodtabeli koostamise aegu järjestati elemendid aatommasside järgi ja nii said nad endale järjenumbrid. Tegelikult kajastab järje- ehk aatomnumber (Z) elektronide arvu aatomis ja ühtlasi tuuma elementaarlaengute arvu. Elektronkatte kihiline ehitus võimaldab kaugemates kihtides hoida rohkem elektrone. Esimese (tuumale lähema, alumise, kõige sügavama, väiksema energiaga) kihi peakvantarv on üks () ja sinna mahub kaks elektroni. Arvestades ka spinni mahub igasse kihti elektroni. Esimeses perioodis ongi kaks elementi, sellega on esimene kiht täis ja täituma hakkab teine. Teise kihi peakvantarv on 2, sinna mahub 8 elektroni. Aatomite keemilisi omadusi määravad väliselektronid. Heeliumil ja neoonil on väliskihid elektrone täis ja nende keemilised omadused on väga sarnased. Pole uudiseks, et kui väliselektrone on vähe, on need nõrgalt seotud ja aatomid kalduvad neid loovutama. Kui aga väliskiht on peaaegu täitunud, täituvad allesjäänud kohad kergesti teistelt aatomitelt saadaolevate elektronidega. Väliselektronid on sidemete moodustumise alus. Keemiliselt kõige põnevamad on nelja väliselektroniga aatomid, nagu süsinik ja räni, mis oma nelja võimaliku sidemega pakuvad võimaluse lõputu arvu ühendite tekkimiseks. Paljude elektronidega aatomites muutub üha olulisemaks elektronide omavaheline mõju ja alates neljandast perioodist läheb kihtide järjestikuse täitumise reegel segamini. Neljandasse kihti läheb esimene elektron enne, kui kolmandas on kõik võimalikud kohad hõivatud.
| Joonis 2.2.7. Elektronide tõenäosuslikku paigutust aatomi sees on võimalik välja arvutada ja katseliselt kinnitada. Kas on võimalik ka tõeliselt elektronkattesse piiluda või vähemalt otse aatomite seest pärinevaid andmeid pildiks muuta? 2013. aastal avaldas rahvusvaheline teadlaste rühm pildid, kus väidetavalt esimest korda paistab ergastatud vesiniku aatomi elektronstruktuur. Kasutatud on uut „kvantmikroskoopi”, kus toimib juba 30 aastat tagasi välja pakutud fotoionisatsioonmikroskoopia meetod. Laseriga ioniseeritavast aatomist erinevates suundades väljuvad elektronid suunatakse elektrivälja abil läbi elektrostaatilise läätse ekraanile. Tekkinud elektronlainete interferentsipilt kannab otsest infot elektronide leiulainetest. | Kass riputab üles perioodilisustabeli |
J. J. Thomson oli tuntud briti füüsik, andekas õpetaja ja hinnatud lektor. Õpetamine ja juhendamine on kindlasti üks tema suuremaid teeneid füüsikateadusele. Tal oli palju õpilasi ja assistente, koguni seitse neist on saanud Nobeli preemia. Aatomimudelite peatükis on juba mainitud Niels Bohri, aatomituumast rääkides tuleb paratamatult alustada Ernest Rutherfordist ja tuumarelva teemas meenutame Robert Oppenheimerit. Kõik nad õppisid ja töötasid Thomsoni laboris ja kes vähegi huvitub aatomifüüsika ajaloost, kohtab seal veel palju teisi tema õpilasi ja kaastöötajaid. Thomson ise sai Nobeli preemia 1906. aastal gaaside elektrijuhtivuse uurimise eest. Gaasi läbiva elektrivoolu eksperimendid olid tõesti olulised, neist koorus lõpuks välja elektron, mis aitas mõista elektrivoolu olemust ja pikapeale hakkas sealt ka aatomi siseehitus hargnema. Hiljem uuris Thomson positiivsete laengukandjatega (ioonidega) elektrivoolu ja teda peetakse stabiilsete elementide isotoopide avastajaks ning ühtlasi mass-spektromeetria leiutajaks. Nobeli preemia sai 1937. aastal ka J. J. Thomsoni poeg George Paget Thomson uurides katseliselt elektronide difraktsiooni kristallides ja tõestades sellega elektroni laineomadusi (ptk Elektronide difraktsioon).
Louis de Broglie, Prantsuse aadliperest pärit noormees, õppis Sorbonne’is ajalugu ja valmistus diplomaadikarjääriks. Ülikooli lõpetamise ajaks tekkinud huvi matemaatika ja füüsika vastu viis teda kõhkluste kiuste edasi õppima loodusteadusi. Esimese maailmasõja ajal teenis de Broglie Eiffeli torni raadiojaamas ja kulutas kogu vaba aja tehnilistele probleemidele. Pärast sõda jätkusid füüsikaõpingud, põhihuvi oli pöördunud kvantide teooriale. 1924. aastal kaitstud dissertatsioonis „Uuringud kvantteoorias” avaldas de Broglie mateerialainete idee, mille järgi teda kõige enam tuntakse. Võib öelda, et kui Planck ja Einstein kvantiseerisid kiirguse, mis nii kindlat tundus olevat laineline, siis de Broglie sai hakkama vastupidisega. Ta omistas laineomaduse aineosakestele, kõigepealt elektronidele. 1927. aastal kinnitasid de Broglie teooriat mitu teaduseksperimenti. 1929. aastal sai ta Nobeli preemia elektronide lainelise olemuse avastamise eest. Selsamal teemal peetud nobelisti loengus ütleb ta: „Kuigi osakesed ja lained ei saa olla sõltumatud, sest Bohri järgi moodustavad nad tegelikkuse kaks üksteist täiendavat jõudu, peab ometi olema võimalik tuvastada teatud paralleelsust osakese liikumise ja sellega seotud laine liikumise vahel.” De Broglie arendas hiljem lainemehaanikat tuumafüüsikas, aga jäi selle juurde, et osakeste laineomadusega kaasneb mingi reaalne, kuigi osakesest lahutamatu lainetus. Ta hindas kõrgelt füüsika üldist filosoofilist pilti ja kirjutas sel teemal mitu populaarset raamatut.
Kaasaegse aatomimudeli üheks aluseks on dualismiprintsiip. Kõigil osakestel on lainelised omadused. Laiemalt võttes on lainelised omadused kõigel, aga ilmnevad need ainult mikromaailmas, näiteks footonite, elektronide ja aatomite juures. Enne elektronide laineliste omaduste käsitlemist tuletame meelde kahte küsimust mehaanika ja elektromagnetismi kursustest:
- millised on lainete omadused?
- mis on valgus?
Laine üks põhiomadusi ilmneb teise lainega kohtumisel. Kehad ei saa kuidagi olla mitmekesi täpselt samas kohas, lained saavad. Mis juhtub lainete kohtumisel, sõltub sellest, kuidas (millises faasis) nad kohtuvad. Samas faasis (maksimum maksimumiga) kohtuvad lained liituvad ja vastandfaasis (maksimum miinimumiga) kohtuvad lained kustutavad üksteist. Esimesel juhul on tegemist tõusuinterferentsiga, teisel juhul mõõnainterferentsiga.
Difraktsioon on lainete tõkete taha levimise nähtus, see on samuti seotud interferentsiga.
Interferentsinähtusi võib märgata mehaaniliste lainete (veepinna lainetus, heli) juures, valguse interferentsiga see nii lihtne pole. Kui suunata kaks valgusvihku seinale, näeme seal ainult valgustatuse suurenemist, mingit mõõnainterferentsi ei ilmne. Valguse interferentsi katset on siiski sobivates tingimustes võimalik teha. Teadusajalugu tunneb Thomas Youngi interferentsieksperimenti ja vastavat valgusteooriat 19. sajandi algusest. Kahte paralleelset pilu või kahte väikest ava läbinud valgus tekitas ekraanile interferentsipildi. Interferents on kindel valguse lainelise olemuse tõend. Valgusosakeste idee, mille laineteooria kõrvale tõrjus, kerkis uuesti esile 20. sajandi algul kuumade kehade kiirguse ja fotoefekti seletamise käigus (ptk Einsteini fotoefekti teooria) ning hiljem veel mitmetes eksperimentides ja teooriates.
Valguse dualistlik (lainelis-korpuskulaarne) käsitlus paistab viitavat sellele, et valgus „oskab esineda” erinevates nähtustes kord lainena, kord footonina. Polariseerumisel on valgus laine, kiirgumisel ja neeldumisel (sh fotoefekti ja fotokeemiliste reaktsioonide juures) on valgus footonite voog. Peegeldumist ja murdumist võib klassikalise optika raames seletada nii laine- kui ka korpuskulaarteooria abil. Sellise „kord üks, kord teine” iseloomuga on igapäevase elukogemuse põhjal raske leppida. Ükski teine nähtus ei toimi nii ja ka meie tavaliste valgusallikate valgus ei ilmuta silmatorkavat dualismi makrokehade maailmas. Siiski on valgusosakesele suhteliselt kerge andestada, et ta meie intuitiivset mõtlemist teaduseksperimentides sedaviisi lollitab. On ju valgus muuski ebatavaline oma absoluutkiiruse ja seisumassi puudumisega. Kuidas on lood pärisosakestega, näiteks elektronidega?
Vaatame katset skeemi (joonis 2.3.2.), kus elektronid läbivad kahte pilu. Iga üksik elektron jätab pilude taga olevale ekraanile jälje. Igaüks võib ette kujutada, kuidas me tulistame aialippide vahelt vastu seina mingite makromaailma väikeste kehakestega, näiteks hernestega, mis jätavad sinna jälje. Määritud seinal näeme lipivahede kujutisi. Kui tulistame kahest pilust, saame seinale kaks triipu. Kuid elektronid on piisavalt väikesed, et sobivatest avadest läbiminekul ilmutada lainelisi omadusi ja näidata ekraanil üksikutest täppidest moodustuvaid interferentsiribasid, mis ilmselgelt kinnitab elektronide laineomadusi. Arvatavasti tekib igaühel joonist 2.3.2.vaadates mõte, et küllap elektronid mõjutavad üksteist teel piludest ekraanini. Sellisel juhul oleks tegemist paljude osakeste üheskoos lainetamisega, millegi veelainetuse sarnasega. Kuid elektrone on võimalik teele saata ükshaaval. Siis võtab katse muidugi kauem aega, aga interferentsipilt tekib ikkagi. Seega peab elektron läbima kahte ava korraga ja seejärel iseendaga interfereeruma.
| Joonis 2.3.3.a Elektronide difraktsioon on oluline kvantmehaanika eksperiment, sellega seoses on arutatud kvantmehaanilise maailmapildi veidruse üle ja pakutud välja mitmeid mõttelisi katseid. Lisaks sellele on elektronide difraktsioon ka hea vaatlusvahend. Näiteks õhuke vase ja tsingi sulfiidi kiht, mida kasutatakse päikesepaneelides paistab elektronmikroskoobis üsna uduselt | Joonis 2.3.3.b Läbivate elektronide difraktsioon ei anna küll kihist otsest pilti, aga sellest saab välja lugeda aine struktuuri, aatomite paigutuse. |
Pilusid läbivate elektronide katsel on meile varuks veel üks üllatus. On võimalik katseseadmele lisada mõõteriist, detektor, mis kontrollib, kummast pilust elektron läbi läheb. Ükshaaval väljalastud ja piludes kontrollitud elektronid ei tekita interferentsipilti. Mingil moel kaotab elektronide piludes „ülelugemine” lainelised omadused. Enamgi veel, sel moel võib vaatleja mõõteriista sisse-välja lülitades otsustada, millal elektronid on osakesed, millal lained.
Kuigi siiani on kogu jutt keerelnud elektronide difraktsiooni ümber, olid esimesed tõestatult dualistlikud osakesed siiski footonid. Üksikute footonite katse kahel pilul tehti 1909. aastal, see toetas valguse dualistlikku käsitlust. Elektronide lainelised omadused leidsid katselise kinnituse pooljuhuslikult 1927. aastal. Ükshaaval teelesaadetud ja pilus määratud elektronide katseni jõuti aastal 1961. Samal moel on nüüdseks demonstreeritud aatomite ja isegi üsna suurte molekulide laineomadusi. Ülalpool näitena nimetatud herneste lainelisust siiski mitte. Kahe pilu katse on kogu aeg olnud ka tuntud mõtteline eksperiment, mis on õhutanud teaduslikku arutelu kvantmehaanika teemal.
Kahe pilu katse mitmed variandid ja mitmed kaasnevad mõttelised eksperimendid panid 20. sajandi esimese poole teoreetikud raske ülesande ette. Mikroosakeste lainelisele käitumisele kuluks ära põhjendus, seletus, tõlgendus või mudel. Aktiivse teadusliku debati käigus kujunenud seletus on matemaatiline ja selle lihtsatesse lausetesse või visuaalsesse mudelisse tõlkimine on küsitav kui üldse võimalik. Mitmed tuntud füüsikud on rõhutanud, et kvantmehaanikas tuleks jõudumööda hoiduda keelele kippuvast küsimusest: „Kuidas see ometi võimalik on?”
Üks formuleering, millest füüsikud enamasti lähtuvad kvantmaailmast rääkides, pärineb suuresti Taani füüsikult Niels Bohrilt, tema kodulinna järgi nimetatakse seda Kopenhaageni tõlgenduseks.
Osakesi väljutav seade (valgusallikas, elektronkahur, radioaktiivne preparaat) tekitab osakese leiulaine. Kopenhaageni tõlgenduse järgi esitab leiulaine osakese leidmise tõenäosust. Teelesaadetud elektroni kohta ei saa küsida, kus ta parasjagu on. Meil on olemas ainult elektroni leidmise tõenäosuse lainetus ruumis, Schrödingeri võrrandi leiulaine. See laine läbibki kahte pilu, interfereerub ja moodustab piludetaguses ruumis elektroni leidmise tõenäosuse interferentsipildi. Üksik elektron võib jõuda ekraanil üsna juhuslikku kohta, praktiliselt igasse punkti, kus ta leidmise tõenäosus on nullist erinev. Kui elektrone saata läbi pilude palju, siis jõuavad nad rohkem sinna, kus interfereerunud leiulainega määratud tõenäosus on suurem.
Hetkel, kui elektron jõuab kahe pilu katses ekraanile ja jätab sinna jälje (tänapäeval jätab see enamasti jälje tundliku ekraaniga ühendatud arvuti mällu), saab selgeks, kus elektron tegelikult on. Elektroni asukoha 100% tõenäosusega teadmine kaotab kogu määramatuse, st mujal ta olla ei saa. Füüsikud ütlevad selle kohta, et leiulaine kollabeerub. Nüüd on ka selge, miks elektronide registreerimine piludes ei võimalda enam interferentsipildi tekkimist. Leides elektroni ühte pilu läbimas, määrame me tema asukoha täpselt. Leiulaine kollabeerub ja ei saa enam interfereeruda. Tegelikult liigub elektron edasi ja pärast pilu läbimist on tegu lihtsalt leiulaine uue kujuga.
Siit paistab veel üks põhjus, miks kvantmehaanika ilmutab end mikromaailmas. Klassikalises mehaanikas toimub kõik alati ühteviisi ja ei sõltu sellest, kas me kehi vaatame või mitte. Muidugi võib juhtuda, et kohmakas eksperimentaator häirib makrokehade liikumist, jätab selle häirimise arvestamata ja saab vigased tulemused. Ometi on suuri kehi võimalik jälgida ilma neid oluliselt mõjutamata. Kahe pilu katses pole võimalust selgelt eristada osakesi (st katseobjekte), mõõtmisseadet ja vaatlejat. Mõõtmine muudab kvantolekut paratamatult.
Veel ühe probleemi tekitab see, et kvantefektid ilmnevad mikromaailmas, aga vaatleja jaoks tuleb mõõtmistulemus paratamatult üle kanda makromaailma. 1935. aastal tõi Erwin Schrödinger artiklis „Praegune olukord kvantmehaanikas” välja hiljem maailmakuulsaks saanud mõttelise eksperimendi, mida tänapäeval kutsutakse „Schrödingeri kass”.
„On võimalik välja mõelda isegi väga veidraid juhtumeid. Teraskambrisse on pandud kass koos järgneva põrgumasinaga (millele kass ise otseselt ligi ei pääse): Geigeri loenduris on väike kogus radioaktiivset ainet, nii vähe, et näiteks tunni jooksul võib-olla laguneb seal üks aatom, aga sama tõenäoline on, et ei lagune ühtegi. Kui laguneb, toimub loenduri torus lahendus ja relee vabastab haamri, mis purustab sinihappe pudelikese. Kui jätta kogu süsteem tunniks ajaks omaette, võib öelda, et kass on elus, kui ükski aatom pole vahepeal lagunenud. Esimene lagunev aatom oleks ta mürgitanud. Kogu süsteemi psiifunktsioon näitab, et seal on (kui lubate nii öelda) elus ja surnud kass võrdsetes osades segunenud või laiali määritud. Sellistel juhtudel on tüüpiline, et algselt vaid aatomimaailmale omane määramatus muutub makromaailma määramatuseks, mida saab lahendada otsese vaatlusega. See hoiab meid „ähmast mudelit” naiivsel moel tegelikkuse kirjelduseks pidamast. Iseenesest selles ei ole midagi segast ega vastuolulist. On vahe, kas foto on tehtud väriseva käega ja teravustamata või on ülesvõttel pilved ja uduvaalud.”
Schrödingeri näide rõhutab läbi kvantmehaanika prisma paistva maailma veidrust. Püüd kirjeldada aatomiosakeste maailma, kus vaatlemine ei ole võimalik vaatlusobjekti olekut (st kvantolekut) muutmata, viib kaugele eemale sellest maailmast, kus on kujunenud meie meeled ja intuitsioon.
Elektronide difraktsiooni (kaldumist sirgjooneliselt teelt tõkke taha) kahe pilu katses võib tagantjärgi pidada kvantmehaanika aluskatseks. Muidugi tekitavad kvantmehaanilised seletused ja Schrödingeri kassi sarnased mõttelised eksperimendid uusi küsimusi.
- Kuidas leiulaine kollabeerub? Milline on täpsemalt see füüsikaline protsess, kui kaua see aega võtab ja kuidas seda kirjeldada?
- Teel elektronkahurist piluni häirib elektron kindlasti mõnda molekuli, iooni või kosmilist osakest, andes seega infot oma asukohast. Kas see ei lähe kirja mõõtmisena paljalt seepärast, et info ei jõua vaatlejani? Millised nõuded esitab loodus mõõtmisele?
- Kas pole olemas mõnda seletust, mis klapiks kõigi katseandmetega ja oleks seejuures ka „mõistlik”?
Kaks esimest küsimust on vastuseta, kuigi nende kallal töötatakse. Kolmanda vastus paistab olevat „ei.” Nii nagu kvantmehaanikat võib matemaatiliselt formaliseerida mitmel, lõppkokkuvõttes siiski samasel viisil, on olemas ka mitu seletust, millest ükski ei mahu meie igapäevase intuitsiooni raamesse ja seega pole „mõistlik”.
Erwin Schrödinger oli Austria füüsik, kaasaegse kvantmehaanika looja. Tema nimega seostuvad Schrödingeri võrrand ja Schrödingeri kass, mille sügavama sisu tundmine jääb kahjuks palju maha nende sõnade kuulsusest. Schrödingeri teaduslik karjäär oli kirju. Ta töötas mitmetes Austria, Šveitsi, Saksamaa, Inglismaa ning Iirimaa teadusasutuses ja ülikoolides, pidas loenguid ka Ameerika Ühendriikides, aga ei jäänud kuhugi pikemalt elama. Põhjuseid oli mitu: Saksamaal ja hiljem ka Austrias võimutsevad natsid, Schrödingeri tervis (ta põdes tuberkuloosi) ja tolle aja kohta ebatavaline ning mitmel pool vastuvõetamatu eraelu korraldus.
Schrödingeri paljude teaduslike huvide hulgas oli aukohal aatomiehituse teooria, uus viis lainemehaanika kaudu lahendada aatomiehituse suuri küsimusi. Selle saavutuse eest sai ta 1933. aastal koos Paul Diraciga Nobeli preemia. Samal aastal anti preemia kätte Werner Heisenbergile, kes oli saanud preemia juba eelmisel aastal, samuti kvantmehaanika loomise eest. Scrödingeri teiste huvide hulka kuulusid värvide nägemise teooria, teoreetiline bioloogia, teadusfilosoofia, antiik- ja idamaade filosoofia, eetika ja religioon. Huvitav on märkida, et mõnedel andmetel ei olnud Schrödinger ise kvantmehaanilisest maailmapildist väga vaimustuses ja otsis midagi enamat, tegeles muu hulgas nagu Einsteingi ühtse välja teooria loomise katsetega.
Niels Bohr oli 20. sajandi teadusrevolutsioonis ehk kõige erakordsema ande ja samavõrd erakordse elukäiguga aatomifüüsika teoreetik. Bohr sündis, elas ja töötas põhiliselt Kopenhaagenis. Mõned aastad õppis ja töötas ta Inglismaal Thomsoni ja Rutherfordi juures Londonis ja Manchesteris. Kopenhaagen jäi siiski linnaks, kus avaldus ta oskus arendada uusi ideid ja samal ajal teadusasutust juhtida. Inglismaalt doktorantuurist naasnud, tegi ta varsti ettepaneku luua ülikoolis teoreetilise füüsika professuur ja oli valmis ise sellele kohale asuma. Asi võttis aega, aga juba mõne aasta pärast asus Bohr suure innuga asutama teoreetilise füüsika instituuti. Ettevõtmist toetasid Taani valitus, Carlsbergi fond, paljud tööstusettevõtted ja eraisikud. 1921. aastal avati instituut ametlikult, töö käis varemgi ja esimesed teadustööd juba ilmusid. Kopenhaagenist sai kvantmehaanika probleemide vaagimise keskus. Teoreetikud hakkasid Kopenhaagenis käima, peeti kirjavahetust. Direktor Niels Bohr osutus andekaks juhiks, tema kui hea võõrustaja ja meeldiva kolleegi kuulsus levis. Füüsikud, sõites Kopenhaagenisse Bohriga nõu pidama, kohtusid omavahel teel läbi Euroopa, peeti ülikoolides loenguid, vaieldi ja arendati uusi teooriaid. Alguse sai Bohri ja Einsteini aastatepikkune debatt, millest kasvas ja arenes kvantmehaanilise maailmapildi Kopenhaageni tõlgendus, arutati läbi paljud uued seisukohad ja tehti üha põnevamaid mõttelisi eksperimente. Füüsikateaduse kuldaeg oli täisõites.
1937. aastal tegi Bohr koos naise ja pojaga maailmareisi, käies Ameerikas, Jaapanis, Hiinas ja Nõukogude Liidus. Teine maailmasõda viis ta mõneks ajaks kodust eemale. Natside võimuletuleku järel pakkus Kopenhaageni instituut ajutist varjupaika paljudele juudisoost teadlastele, aga ka teistele, kes natside ideoloogia suhtes kriitilised olid. Sakslaste poolt 1940. aastal okupeeritud Taanis oli olukord ebakindel ja saanud hoiatuse peatsest arreteerimisest, põgenes Bohr koos perega Rootsi. Seal kohtus ta kuningaga, et rääkida Taani juutidele varjupaiga taotlemisest. Ei ole päris kindlaid tõendeid, kas just Bohri tegevus oli määrav, aga üle 7000 juudi pääseski okupatsioonivõimude eest Rootsi pakku. 1943. lõpul viidi Bohr riskantse lennureisiga Inglismaale ja varsti suundus ta Ameerika Ühendriikidesse, kus valenime all reisides tutvus tuumarelva loomise salajase projektiga. Ei ole täpselt teada, kui suur oli ta panus sellesse, aga mitmetes mälestustes on tema osa siiski mainitud. Pärast sõda võitles Bohr aatomienergia rahumeelse kasutamise eest. Teades, et tuumarelvade loomine muudab rahvusvahelisi suhteid, pooldas Bohr üldist tuumasaladuste avalikustamist. Külma sõja tingimustes osutus kõik palju keerulisemaks, aga siiski õnnestus pärast esimesi Nõukogude Liidu tuumakatsetusi luua Rahvusvaheline Aatomienergia Agentuur. Bohri initsiatiivil loodi Euroopa Tuumauuringute Keskus (CERN) pidurdamaks sõja eel alanud ja üha jätkuvat ajude äravoolu Ameerikasse. Esialgu tundus loogiline olevat asutada keskus Kopenhaagenisse. Euroopa füüsikud suhtusid sellesse kahtlevalt, sest Taanis oleks kogu tegevust varjutanud suurepäraste administraatorivõimetega Bohri vaieldamatu autoriteet. CERN asutati Šveitsis, kuigi teoreetiline osakond töötas algul siiski Kopenhaagenis. Niels Bohr suri 1962. aastal oma armastatud kodulinnas.
Bohri teadussaavutustest tuntakse enam Bohri aatomimudelit koos vesiniku spektri seletusega (Nobeli preemia 1922) ja kvantteooria arendamist. Nende kahe ja oma instituudi pikaajalise juhtimise kõrvale mahtus veel palju märkimisväärset teadust. 1920. aasta paiku esitas Bohr perioodtabeli teoreetilise kirjelduse, mis sisaldab huvitavaid ennustusi. Kolmekümnendatel tegeles ta aatomituuma ehituse teooriatega ja seletas, mis osa on uraani radioaktiivsel lagunemisel isotoobil massiarvuga 235.
Võib teha veel ühe üsna veidra mõttelise eksperimendi, millel on üllatuslik seos kvantmehaanikaga. Kujutleme maanteel kihutavat autot ja politseinikke selle kiirust mõõtmas. Politseinike ja nende aparatuuri jaoks on igal ajahetkel autol kindel koht ja kiirus. Mida parem on aparatuur, seda tõenäosem on täpse tulemuse saamine. Seejuures me (autojuhid, reisijad, politseinikud, mõõteseadmete tootjad, taatlejad jt) eeldame, et kiiruse mõõtmise täpsus ei mõjuta asukoha mõõtmise täpsust. Küllap ongi mõistlik autode kiiruse mõõtmist võtta just nii. Selle mõttelise eksperimendi küsimus on hoopis järgmine: kas võib ette kujutada mingit teist olukorda, mingeid teisi mõõdetavaid objekte, mille korral kiiruse ja asukoha määramise täpsus on omavahel seotud?
Saksa teadlane Werner Heisenberg tõestas 1927. aastal, et on olemas füüsikaliste suuruste paarid, mis ei saa olla samaaegselt kuitahes täpselt määratud. Üheks selliseks paariks on keha asukoht (koordinaat ) ja impulss (, massi ja kiiruse korrutis). Seda tõestatud tõsiasja nimetatakse määramatusseoseks või määramatuse printsiibiks ja väljendatakse matemaatiliselt valemiga:
kus on asukoha ja impulsi mõõtemääramatus ning on taandatud Plancki konstant (h kriipsuga). Plancki konstant ses valemis viitab veelkord sellele, et määramatusseos ilmutab end mikromaailmas ja puudutab kvantolekuid. Autode ja politseinike maailmas, kust me alustasime seda peatükki, jääb määramatusseos arvestamata, aga kiirguskvantide ja elektronide juures saab see otsustavaks.
Teades, et mõõtmine mõjutab mõõdetavat, võib määramatusseost võtta nii, et looduses on olemas põhimõtteline piirang mõõtmiste täpsusele, aga võib vaadata ka nii, et kvantsüsteem ise on teatud piirini määramatu asukoha ja impulsiga. Tegemist pole tehnilise probleemiga, mõõteseadmete täiustamisega ja ettevaatlikuma (st objekti vähem häiriva) mõõtmisega sellest üle ei saa ega saa ka mingil muul moel.
Määramatuse printsiip on üsna universaalne ja ei käi ainult mõõtmise määramatuse kohta. Peale koordinaadi ja impulsi on teisigi füüsikaliste suuruste paare, mida seob määramatusseos. Loodusnähtuste seletamisel ja praktilise rakenduste juures tuleb rääkida seosest:
| Joonis 2.4.1. Ühe pilu katse, laserkiir läheb läbi reguleeritava laiusega pilu ekraanile. Väga kitsa pilu korral moodustub optikakursusest tuttav difraktsioonipilt, külgedel on näha interferentsimaksimumid. Keskmine valguslaik, mis lahtise pilu korral oli ümmargune täpp, venib külgedelt laiemaks. Pilu kitsamaks tehes määrame järjest täpsemalt footonite asukoha pilu läbimisel. Määramatusseose tõttu jääb üha enam määramata, kuhu nad edasi lähevad, st kitsama pilu korral võivad footonid rohkem kõrvale kaduda. | Joonis 2.4.2. Kunstnik võiks tunnelmikroskoobi tööd kujutada nii. Kristalne teravik libiseb üle uuritava pinna, sinise helenduse saatel tunneleeruvad elektronid teravikult proovi aatomitesse. Arvuti reguleerib teraviku asendit ja registreerib selle liigutused nanoskaalas. Ekraanile ilmub pilt... Kujutlus polegi nii väga kunstiline. Võib-olla sinine helendus on liiast, aga nii see aatomite „vaatamine” tänapäeval käib. |
Energia ja aja määramatusseose populaarne seletus pöördub jälle kord mõttelise eksperimendiga autode maailma. Kujutleme ülesmäge kihutavat autot, mille kütus on lõppenud, aga hoog on sees, ja kui kineetilisest energiast piisab tõusu lõpuni, ootab ees pikk laskumine järgmise bensiinijaamani. Kahjuks jääb tipu ületamisest natuke puudu ja auto ähvardab hakata kohe-kohe tagasi veerema. Nüüd võiks väga lühikeseks hetkeks energia jäävuse seadusest mööda hiilides nihutada auto läbi korraks avaneva „tunneli“ mäe teisele küljele. Kui energia jäävus jälle kehtima hakkab, siis bilanss klapib. Auto on ikka samal kõrgusel, aga teiselpool mäge ja teekond võib jätkuda.
Vaevalt, et keegi autosõidul sellist trikki tõsiselt kaalub, aga mikromaailmas on energia ja aja määramatuse seosel tähtis koht looduslikes protsessides, näiteks tuumaenergeetikas, Päikese ja teiste tähtede sisemuses ning radioaktiivsusega seonduvates protsessides.
On olemas tunnelefektil põhinevaid rakendusi, millest tunnevad rõõmu nanotehnoloogid.
Tunnelmikroskoobis (joonis 2.4.2.) liigutatakse „vaadeldava” objekti pinna kohal peene elektroonilise juhtimisega üliteravat teravikku, mille peenimat tippu võib pidada peaaegu üksikaatomiks. Teraviku ja proovi vaheline väike pinge sunnib elektrone rajama endale ainesse üleminekuks määramatuse tunneleid. Tekkinud voolu mõõdetakse ja selle kaudu reguleeritakse teraviku kõrgust. Kõrgusest ja asukohast saab arvutada pinna struktuuri ja kuvada see arvutiekraanile.
Parafraseerides Einsteini: Nagu oleks kogu sellest kvantkarglemisest veel vähe... Energia ja aja määramatusseos lubab mikroosakestel tekkida eimillestki. Tingimuseks on muidugi, et nad oleks kerged (vähe massi, vähe energiat) ja ei kestaks kaua. Nii pole ka vaakum sugugi tühi, sealgi saavad olemise ja olematuse piiril hüpelda virtuaalosakesed.
Werner Heisenberg seostub teadusloos eelkõige määramatusseosega. Nobeli preemia sai ta kvantmehaanika loomise eest, mida praegu on kombeks siduda hoopis Erwin Schrödingeri ja tema võrrandiga. Heisenbergi füüsikani jõudmine oli juhuste rida. Kui juhused oleks võtnud ritta teisiti, räägitaks temast tänapäeval kui silmapaistavast matemaatikust. Tema lähenemine füüsikaprobleemidele oli teistsugune, aga lõpptulemustele pole muidugi miskit ette heita. Heisenberg oli isiklikus elus ja karjääris keeruliste valikute ees nagu enamus 20. sajandi füüsikuid. Tedagi mõjutasid lisaks üldisele murrangule teaduslikus mõtteviisis väga isiklikult ühiskondlikud ja poliitilised sündmused maailmas ning Euroopas eriti. 1935. aastal oleks ta võinud saada Müncheni ülikooli professoriks oma teadusliku juhendaja Arnold Sommerfeldi pensionilesaatmise järel. Kohalemääramine venis aastaid, sest ametlik poliitika suhtus eitavalt sellistesse „juudi teadustesse” nagu relatiivsusteooria ja kvantmehaanika. Heisenberg ei olnud juut, teda süüdistati juudi stiilis tehtud teaduse pärast. Lõpuks õnnestus tal uurimistest siiski auga välja tulla, aga karjäär Münchenis oli siiski läbi. Teise maailmasõja ajal oli Heisenberg edutult kulgenud Saksa tuumarelva loomise programmi juht. 1941. aasta sügisel külastas ta okupeeritud Kopenhaagenit, pidas mõned loengud ja kohtus Niels Bohriga. Heisenberg oli Bohri alati pidanud oma õpetajaks ja Kopenhaagen oli talle kahekümnendatest aastatest kodune koht, aga sundimatust vestlusest asja ei saanud. Kohtumist, mille eesmärk oli arvatavasti tuumaenergia küsimuste arutamine, on hiljem kirjeldatud erinevalt ja täpsemad asjaolud ongi jäänud teadmata. Sõja lõpu eel interneeriti Heisenberg koos teiste saksa teadlastega ja viidi Inglismaale. 1946. aastal jõudis ta tagasi kodumaale, ütles viisakalt ära ettepanekust kolida Nõukogude Liitu ja töötas elu lõpuni mitmetes teadusasutustes, avaldas artikleid füüsikast ja filosoofiast, pidas loenguid nii kodu- kui ka välismaal. Muu hulgas sai temast korraline professor Müncheni ülikoolis.
Röntgenikiirte ja elektroni avastamine 19.sajandi lõpuaastatel oli kahtlemata pöördepunkt teadusliku maailmapildi arengus. Mõnekümne aastaga saadi vastused küsimustele, mida enne ei osatud küsidagi: valguse ja teiste kiirguste olemus, elektrivoolu ja magnetismi toimemehhanism, aatomite elektronstruktuur ja selle seos keemiliste omadustega; kvanthüpoteesist jõuti kvantmehaanikani. Samal ajal avastatud radioaktiivsuse uurimine viis mitte vähem revolutsiooniliste muutusteni teaduses ja ühiskonnas. Nii nagu fotoefekti teooria ei saanud tekkida enne elektroni avastamist ja kvanthüpoteesi, ei saanud ka radioaktiivsuse saladus laheneda enne aatomituuma avastamist.
Tuumafüüsika sünd on seotud Ernest Rutherfordi töödega, eelkõige maailmakuulsa kuldlehe eksperimendi (joonised 2.5.1., 2.5.2.) ja aatomituuma avastamisega. Rutherfordi juhtimisel uuriti Victoria ülikoolis Manchesteris, kuidas raadiumist kiirguvad α-osakesed läbivad erinevaid aineid. Radioaktiivse kiirguse liigid, α- ja β-kiired ning vastavad osakesed oli ta ise varem avastanud ja nimetanud. Otsustava eksperimendi tegid Rutherfordi juhtimisel Hans Geiger ja Ernest Marsden 1910. aastal. Rutherford esitas eksperimendi tulemused ja oma aatomimudeli 1911. aastal. Uue mudeli järgi tiirlesid elektronid suure massiga ülipisikese positiivse kesklaengu ümber. Kaasaegsest mudelist oli veel päris palju puudu, näiteks ei tuntud neutraalset tuumaosakest, neutronit, ka elektronide orbiitidega oli veel paljugi lahtine, aga tuumafüüsika oli sellega sündinud.
| Joonis 2.5.1. Rutherfordi hajumine. Üliõhukest, umbes 400 aatomi paksust kuldlehte läbivad α-osakesed kohtuvad oma teel aatomitega. Thomsoni rosinakukli mudeli [bookx=1610](ptk Aatomimudelite arengust 20. sajandil)[/bookx] järgi pidanuks aatomis hajusalt paiknevad laengud üsna rakseid ja kiireid α-osakesi otseteelt kõrvale kallutama mõne kraadi võrra. Eksperimendi käigus selgus, et α-osakeste hajumine on hoopis suurem, väike osa neist põrkub aatomitelt isegi tagasi. Analüüs näitas, et aatomi mass ja laeng peavad olema väga tihedalt koondunud. Kesklaengu mõõtmeteks arvutati mitte üle 10-13 meetri. | Joonis 2.5.2. Täiustatud seade kuldlehe eksperimendiks. Pisikeses kambris (1) on raadiumitükike (2), millest väljuvad α-osakesed läbivad kitsa ava. Moodustub kiir, mis läbib õhukese kuldlehe (3). Pööratav mikroskoop (5) võimaldab vaadelda erinevate nurkade all hajunud α-osakeste stsintillatsioone (pisikesi valgussähvatusi) tsinksulfiidiga kaetud ekraanil (4). Nõrkade sähvatuste lugemiseks peab eksperimentaatori silm olema pimedusega täielikult harjunud, st vähemalt pool tundi enne mõõtmise algust peab veetma täielikus pimeduses. Minutise vaatluse järel on vaja silmi puhata ja üle 90 osakese minutis ei jõua keegi eraldada. Katsete käigus loeti kümneid tuhandeid osakesi. |
Isotoobid on elemendi teisendid, mis erinevad aatommassi poolest. Aatommassi erinevuse põhjus on neutronite erinev arv tuumas. Tuumade tähistamiseks kasutatakse perioodtabeli sümboleid, mille juurde märgitakse tuuma laenguarv (ühtlasi järjenumber) ja massiarv kujul , kus element on tabelis järjekohal , (st tuumas on prootonit) ja tuumaosakeste koguarv ehk massiarv on (st, neutroneid on A-Z).
Näiteks looduslik uraan koosneb 3 isotoobist:
, uraan-238, tuumas on 92 prootonit ja 146 neutronit (, );
uraan-235, tuumas on 92 prootonit ja 143 neutronit (, );
uraan-234, tuumas on 92 prootonit ja 142 neutronit (, ).
Ühe elemendi isotoopide keemilised omadused on väga sarnased, raksematel tuumadel täiesti ühesugused, seepärast ei saa neid kuigi lihtsalt üksteisest eraldada (ptk Manhattani projekt).
Aatom on väga väike, aga aatomituum tõesti peaaegu kirjeldamatult väike. Aatommassid võib leida igast perioodtabelist või käsiraamatust, aga täpset aatomite ja tuumade mõõtmete tabelit on keeruline koostada. Aatomi raadius on mõiste, mida mitmetes füüsika ja keemia mudelites tõlgendatakse erinevalt. Piltlikult öeldes on see nagu puuvillapallide mõõtmine. Mõõtmistulemus oleneb sellest, kas puuvill on lahtiselt põrandal või pakitud, kas pall on üksikult või laoruumis teiste vahele kiilutud. Kui tõmmata lahtisele puuvillale mõõdulint ümber, tekib kohe tüli sellepärast, kui palju peaks linti pingutama, et saada aus tulemus. Ka aineosakeste mõõtmisel on paratamatu, et nad saavad mõõtmisest häiritud ja tegelikult ei olegi neil selget kõva pinda, mille „ümber mõõdulinti tõmmata”. Kõigist neist probleemidest mööda hiilimiseks räägime vaid suurusjärkudest ja arvestame, et aatomite läbimõõt on umbes 10-10 meetrit. Aatomite, molekulide, keemiliste sidemete, mikrobioloogiliste objektide jms mõõtmiseks kasutatakse tihti spektromeetriast pärinevat aatomimõõdus ühikut ongström: 1 Å =10−10m=0,1nm.
Aatomituumade läbimõõdu suurusjärk on 10-14 meetrit. Tuumaosakeste mõõdud on umbes üks femtomeeter, 1fm=10−15m. Suuremate tuumade läbimõõt on umbes 15fm=1,5⋅10−14m. Femtomeeter kannab juba pool sajandit tuumafüüsikas nime fermi, meenutamaks Itaalia füüsikut Enrico Fermit. Väga üldiselt võttes on tuum aatomist 10 000 korda väiksem. Kuigi mikromaailma tegelikke mõõte on inimesel raske hoomata, võib püüda aatomit kujutleda nii suurena, et ta parasjagu mahuks tuppa ära. Aatomi tuum oleks siis nii suur nagu selle raamatu täpitähtede täpid.
Modelleerides tuuma kui tuumaosakeste tilka ja lugedes kõik aatomid täpselt kerakujuliseks, võime kasutada tuumade raadiuse () arvutamiseks lihtsat, umbes 20% täpsusega valemit:
kus konstant ja on tuuma massiarv (prootonite ja neutronite koguarv). Kulla () tuumade läbimõõt on selle mudeli järgi 14,5 fm.
Rutherfordi mudel ei kirjeldanud kuidagi tuuma siseehitust. Tuuma massi ja laengu klapitamiseks arvati osa elektrone olevat tuuma sees. 1920. aasta paiku levis neutronite hüpotees, nimepanijaks jälle Rutherford. Kõigi tuumaosakeste, ühtviisi nii neutronite kui ka prootonite vahel toimiv tuumajõud pidi kuidagi kompenseerima prootonitevahelist elektrilist tõukejõudu ja muutma tuuma stabiilseks. 1932. aastal tundis James Chadwick neutroni ära eksperimentides, kus berülliumi aatomeid pommitati α-osakestega. Selle avastuse eest sai ta Nobeli preemia.
Tuuma lihtsaimaks kirjeldajaks sobib tilgamudel. Kõik osakesed tuumas on ühesuurused, kerakujulised ja neid hoiab koos tuumajõud, tekitades tuuma pinnal midagi pindpinevuse sarnast. Mudel pärineb 1935. aastast ja kirjeldab tuuma siseehitust klassikalise vedelikuna. Umbes pooltel osakestest on positiivne elementaarlaeng, teistel laengut pole. Vaatamata sellele erinevusele ei ole aatomituuma tilgamudelis ühelgi osakesel mingit eelistatud kohta, nii nagu vedelikutilgas ei ole ühelgi molekulil oma kindlat kohta. Mudel kirjeldab päris hästi mitmeid tuumade omadusi, näiteks kerakujulisust ja seoseenergiaid (ptk Kust pärineb tuumareaktsioonides vabanev energia?).
Tilgamudel haarab osakeste kvantmehaanilist olemust ainult servamisi ja ei seleta täpselt tuumade stabiilsuse erinevusi. Perioodtabeli mõnede tuumade seoseenergia on ebatavaliselt suur, need nn maagiliste järjenumbritega 2, 8, 20, 28, 50, 82 ja võib-olla 126 tuumad on oluliselt stabiilsemad, kui neile vahetult järgnevad. Erinevalt tilgamudelist võtab kihtmudel prootonitelt ja neutronitelt nende vabaduse olla tuumas kus tahes, kirjeldades nende kvantolekut. Mudelis sisaldub analoogia aatomi elektronstruktuuriga. Prootonite ja neutronite kihid on stabiilsemad, kui nad on osakestega täielikult täidetud, nii nagu väärisgaaside erilise inertsuse põhjus on elektronkihtide täidetus.
Aatomituum koosneb nukleonidest, prootonitest ja neutronitest, mis omakorda koosnevad kvarkidest. Prootonite ja neutronite, millest koosnevad meie tavapäraste aatomite tuumad, fundamentaalsed koostisosad on kaks kvarki: u-kvark ja d-kvark. Nimed on tuletatud inglise keelest, up ja down, aga neil ei ole otsest seost sõnade igapäevase tähendusega. See kehtib kogu Standardmudeli terminoloogia kohta. Kvargid on erilised osakesed, nad ei esine kunagi ükshaaval. Prootonis on kaks u-kvarki ja üks d-kvark, neutronis on kaks d-kvarki ja üks u-kvark. Nii ongi kvargid kolmekesi, teatud erilistel juhtudel korraks kahekesi, aga mitte kunagi üksi. See nähtus on saanud nimeks kvarkide vangistus.
Standardmudeli fundamentaaljõude on neli, tugevuse tõusu järjestuses: gravitatsioonijõud, elektromagnetjõud, nõrk jõud ja tugev jõud. Igapäevaelus tunneme kahte esimest, mida on võimalik kirjeldada klassikaliste füüsikamudelitega. Raskusjõud, hõõrdejõud, elastsusjõud – kui nimetada ainult tuntuimad. Nõrk ja tugev jõud on lihtsa vaatluse eest peidetud aatomituumadesse. Tugev jõud vangistab kvargid nukelonidesse. Gluuonid on osakesed, mis vahendavad kvarkide vahel tugevat jõudu, „kleepides” (inglise keeles: glue - liim) nad kokku prootoniteks ja neutroniteks.
Tugev jõud on väga väikese mõjuulatusega, suuremalt jaolt toimib ta nukleonide sees. Prootoneid ja neutroneid hoiab omavahel koos see osa tugevast jõust, mis ulatub nukleonist välja, nn tugeva jõu jääk. Prootonite ja neutronite vahelist jõudu võivad vahendada neutraalsed piionid (), mis on väga lühikese elueaga kvargist ja antikvargist koosnevad osakesed.
Mõnes mõttes on nukleonidevahelised jõud sarnased molekulaarjõududega (ptk Van der Waalsi jõud). Molekulaarjõude võib vaadelda keemilist sidet põhjustava elektromagnetjõu jäägina. Sarnaselt molekulaarjõududele on ka tugeva jõu jääk tõmbejõud, aga väga väikesel kaugusel muutub tõukejõuks, mis püüab osakesed minimaalse energia lõksu (joonis 1.1.3.). See sarnasus ongi põhjuseks, miks tilga mudel nii hästi töötab.
Tuumaosakesi on üsna keeruline pildile saada, sest tuuma üliväikeste mõõtmete juures ei ole mõtet küsida, kuidas see või teine asi „välja näeb”. Osakestefüüsikas, kus protsesse saab kirjeldada vaid üsna keeruka matemaatika abil, kasutatakse interaktsioonide arvutamiseks ja visualiseerimiseks Ameerika füüsikuteoreetiku Richard Feynmani leiutatud diagramme. Joonisel on Feynmani diagramm, mis kujutab prootoni ja neutroni vahelist interaktsiooni. Püstteljel on ruum (kaugus), rõhtteljel aeg. Tegemist on lihtsustatud diagrammiga, kus ei ole näidatud gluuoneid ja piioni tekkimist.
Ernest Rutherford oli pärit Uus-Meremaalt. Teaduskarjääri jaoks polnud Uus-Meremaa tol ajal sobivaim paik, aga Rutherford oli tubli ja edukas üliõpilane, tegeles uurimistööga elektritehnika alal ning sai stipendiumi õpingute jätkamiseks Inglismaal Cambridge’i ülikoolis. J. J. Thomsoni laboris tegeles ta mõnda aega raadiosidealaste töödega, uuris koos juhendajaga gaaside elektrijuhtivust ja röntgenkiiri. Püüdes gaaside elektrijuhtivust mõjutada värskelt avastatud radioaktiivse kiirgusega, kaldus ta huvi 1898. aastal radioaktiivsuse üldisele uurimisele. Töötades Kanadas McGilli ülikooli moodsas laboris ja hiljem Manchesteris Victoria ülikoolis, uuris Rutherford üksteise järel välja radioaktiivsuse saladusi. Ta tõi tuumafüüsikasse mõisted alfa-, beeta- ja gammakiirgus, poolestusaeg, kivimite radioaktiivne dateerimine jpm. 1908. aastal sai Rutherford Nobeli keemiapreemia radioaktiivsete elementide keemia uurimise eest. Ta on ainuke nobelist, kes on preemia saanud enne oma tuntuimat saavutust.
Kanadas töötades oli Rutherford märganud, et alfakiirgus kipub vilgukivi lehekest läbides veidi hajuma. Manchesteri laboris asusid alfaosakeste hajumist aatomites mõõtma tema noored kolleegid Marsden ja Geiger. Kuigi sellest vaevarikkast eksperimendist (joonis 2.5.2.) midagi erilist loota polnud, läks hoopis teisiti. Katse tulemused võttis kokku juhendaja ise. Täpsus polnud väga suur, kuid tulemus oli pöördeline, täiesti uus aatomimudel. Eksperimentaatorina ei olnud Rutherfordile vastast. Ta jätkas koos arvuka noortest teadlastest koosneva meeskonnaga tuumareaktsioonide uurimisega, tõestas, et vesiniku aatomituum on teiste tuumade ehituskivi ja nimetas selle prootoniks.
1912. aastal saabus Manchesteri laborisse vaid mõneks kuuks Niels Bohr, kes oli tulnud Inglismaale J. J. Thomsoni juurde oma õpinguid lõpetama. Vabameelne ja uutest ideedest vaimustuv Bohr sobis hästi Rutherfordiga ja samavõrra planetaarmudeliga. Rutherford-Bohri poolklassikaline aatomimudel on praegugi kooliõpikutes tähtsal kohal, sest kirjeldab piltlikult ja piisavalt mitmeid aatomite omadusi. Bohri ja Rutherfordi sõpruse ja koostöö tulemusena sündis tuuma tegeliku koostise teooria, mis ennustas neutroni ning tuumajõudude olemasolu. Rutherfordi mõju eksperimentaalfüüsika arengule on sama raske üle hinnata, kui Bohri oma teooriale.
Kolmekümnendad aastad tõid Rutherfordi nii isiklikku kui tööellu muutusi. 1930. aastal suri pärast neljandat sünnitust tema ainus laps, tütar Eileen. Rutherford jätkas noorte kaastöötajate juhendamist. 1932. aastal tõestas James Chadwick oma eksperimendiseeriaga neutroni olemasolu. John Cockcroft ja Ernest Walton tekitasid tuumareaktsiooni kiirendatud prootonitega, tõestades, et tuumaosakeste seosed on miljoneid kordi tugevamad keemilistest sidemetest. Olles 1931. aastast parun Rutherford of Nelson ja Lordide Koja liige, pöördus ta üha enam ühiskondlike teemade poole. 1933. aastast oli ta Akadeemilise Abistamise Nõukogu president, toetades natsire?iimi eest pagenud teadlasi, aga keeldus isiklikult abistamast saksa keemikut Fritz Haberit, kes oli Esimese maailmasõja ajal arendanud keemiarelvi. Rutherford suhtus alati ühtviisi nii kuulsustesse kui noortesse algajatesse, samuti toetas ta naistele võrdsete õiguste andmist ühiskonnas, hariduses ja teaduses. Ta ei unustanud oma algset kodumaad, olles Uus-Meremaa ülikoolile heaks nõustajaks ja võttes vastu sealt pärit üliõpilasi.
Rutherford lootis, et tuumaenergia ei ole inimkonnale kättesaadav, vähemalt mitte enne, kui on õpitud naabritega rahus elama. Ta suri 1937, paar aastat enne tuumarelva loomise projektide algust.
Aatomi jagamatuse ja igavese püsivuse idee oli 20. sajandi alguses muutunud ajalooks. Radioaktiivsuse uurimine oli paljastanud tõsiasja, et vähemalt mõne elemendi aatomituumad lagunevad, kiirates - ja -osakesi. -osake on heeliumi tuum, mis tähendab, et üks aatom (näiteks raadium) paiskab välja teise aatomi (heeliumi) tuuma. Seejuures muutub ta ka ise teiseks elemendiks. -osake on kiire (st suure energiaga) elektron. Esimestes oletustes tuuma koostise kohta eeldati tuumaelektronide olemasolu, aga katsed ja arvutused näitasid, et see pole nii. Järelikult peavad elektronid tuumas tekkima, aga kuidas ja millest?
Kuni 1919. aastani oli tuumade muundumisest tuntud ainult iseeneslik - ja -lagunemine. Mitme tuuma või tuuma ja osakese vahelisi interaktsioone, mille käigus tuumad lagunevad või moodustuvad uued, looduses küll toimub, aga neile polnud kuigi kerge jälile saada.
Ernest Rutherford uuris Manchesteris mitu aastat -osakeste mõju gaasidele: vesinikule, lämmastikule jt. Tema viimaseks tööks enne Cambridge'i tagasipöördumist oli tõestus, et -osakesed löövad lämmastiku tuumadest välja prootoneid ja ise ühinevad lämmastikuga. Seda võib lugeda esimeseks kontrollitud tingimustes uuritud tuumareaktsiooniks:
Tuumareaktsiooni võrrandis on siin vasakul poolel levinuim lämmastiku isotoop , mis ühinemisel -osakesega (heeliumi tuumaga ) muutub stabiilseks hapniku isotoobiks , mida looduslikus hapnikus on ainult 0,04%. Eraldub prooton ehk vesiniku tuum, mille tekke järgi reaktsioon tegelikult avastati.
Keemiliste reaktsioonide võrrandites avaldub 18. sajandil avastatud aine massi jäävuse seadus, mis tähendab, et kõik lähteainete aatomid peavad olema ka saaduste poolel ehk võrrand olgu tasakaalus. Tuumareaktsioonide võrrandid tasakaalustuvad teiste jäävusseaduste järgi, millest nimetame kolm:
- Laengu jäävuse seadus. Sümbolite juures on alumise indeksina märgitud tuumalaeng (tuuma positiivsete elementaarlaengute ehk prootonite arv, järjenumber). Laengute summa võrrandi pooltel peab olema tasakaalus.
- Massiarvu jäävuse seadus. Massiarvud (prootonid ja neutronid kokku) peavad samuti olema tasakaalus. Tuumareaktsioonides ei tähenda see massi jäävust samas mõttes kui keemilistes reaktsioonides.
- Energia jäävuse seadus.
Tuumareaktsiooni võrrandi vastavus jäävusseadustele ei tähenda veel, et selline reaktsioon toimub. Tuumad või osakesed peavad ka kokku saama. Rutherfordi teostatud või pigem avastatud tuumareaktsioonis kasutati -osakesi, mis tekkisid iseeneslikul radioaktiivsel lagunemisel. Lämmastiku tuum ja -osake on mõlemad positiivse laenguga, et nad kohtuksid, tuleb ületada elektriline tõukejõud, nn kuloniliste jõudude barjäär. Looduslikel α-osakestel selle barjääri ületamiseks piisavalt energiat pole ja nimetatud reaktsioon saab toimuda ainult tänu tunnelefektile (ptk Määramtusseos). Tuumareaktsioone saab toimuma panna ka kunstlikult osakesi kiirendades. Esimese kiirendatud prootonitega tuumareaktsiooni teostasid 1932. aastal John Cockcroft ja Ernest Walton. Nende saavutust nimetatakse aatomi lõhestamiseks, mis on selles mõttes õige, et saadused (heeliumi tuumad) on väiksemad kui märklauaks olnud liitiumi tuumad. Sisuliselt on tuumereaktsiooni toimumine siiski keerulisem ja lõhestamiseks võib seda ainult kujundlikult nimetada.
Selles üsna kuulsaks saanud tuumareaktsioonis ilmneb huvitav energeetiline efekt. Mõõtmised näitasid, et -osakeste kineetiline energia oli kokku suurem kui prootonite oma (liitium oli paigal). See tähendab, et reaktsioon on eksotermiline, tuumareaktsioonis vabaneb energiat. Energia tootmiseks see siiski ei sobi, sest ei toimu iseenesest. Selleks, et aatomid pidevalt lõhustuksid, on vaja pidevalt prootoneid kiirendades energiat kulutada. Tuumaenergeetika vajab reaktsioone, mis ennast ise käigus hoiaksid, teisisõnu ahelreaktsioone (ptk Tuumaenergeetika). Ahelreaktsioon tekitab ise osakesi, mis põhjustavad uue reaktsiooni. Selliseid protsesse tuntakse nii keemias, füüsikas kui ka majanduses. Tuumafüüsikas osutus järjekordseks pöördepunktiks uraani tuuma lagunemise avastamine 1938. aastal. Just siis said läbi teaduse kuldsed ajad. Euroopa teadlased olid rahvuslikel ja poliitilistel põhjustel üle maailma laiali paisatud, järgmisel aastal algas Teine maailmasõda ja teaduslik saavutus sai ühtlasi pöördeks rahvusvahelistes suhetes (ptkTuumarelv).
Ahelreaktsioonis laguneb uraan-235 tuum (looduslikus uraanis 0,72%) neutronite toimel ja eralduvad uued neutronid:
Reaktsiooni saadusteks on erinevad kildtuumad, millest esimesena avastati keemilise analüüsi abil baarium. Hiljem on selgunud, et neutroni haaramisega ebastabiilseks muutunud uraan-235 tuum laguneb erinevateks baariumi ja krüptooni isotoopideks (seepärast pole võrrandis massiarve) ja ka muud killud ei ole võimatud. Reaktsioon jätkab ennast sobivates tingimustes ise, sest tekitab uusi neutroneid, mis võivad omakorda uraanituumasid lõhkuda. Ahelreaktsioon võib laviinina laienedes kulgeda plahvatuslikult, aga kui uusi neutroneid ei teki piisavalt, võib ka hääbuda.
Maapealsed tingimused ei soosi üldiselt tuumareaktsioonide toimumist. Gabonis, Ekvatoriaal-Aafrikas on leitud uraanimaagis jälg kaks miljardit aastat tagasi toiminud looduslikust tuumareaktorist. Praeguse uraanimaagi koostise ja Maal valitsevate tingimuste juures see enam töötada ei saaks. Mitmeid tuumareaktsioone tekitab kosmiline kiirgus ja tähed säravad just tuumareaktsioonide arvel.
Tähtede tohutu kiirgusvõimsuse taga on heeliumi tuumade süntees:
Tähe suur siserõhk ja kõrge temperatuur võimaldab prootonitel ühineda heeliumiks läbi mitme vaheetapi. Lõpuks tekib väga stabiilne tuum (-osake), mis koosneb kahest prootonist ja kahest neutronist. Osa lähteprootonitest muutuvad neutroniteks ja laengu jäävuse tõttu tekivad positronid (positiivse laenguga elektronid, antielektronid), mis tavaliste elektronidega kohtudes kohe annihileeruvad:
Heeliumi sünteesis vabaneb palju energiat, millest osa eraldub -kiirguse ja neutriinodena ().
Tuumaenergia, mida saab kasutada tuumajaamas või mida me tunneme päikeseenergiana, on osa tuumaosakeste seoseenergiast. Aatomituuma tilgamudel esitab siin hea analoogia. Kui vedelikutilk aurustada (molekulideks laiali jagada), on vaja molekulaarsidemete lõhkumiseks energiat kulutada. Kui aga vedelik kondenseerub piisaks ja sidemed moodustuvad, siis seesama energiahulk eraldub. (ptk Gaas ja vedelik). Kujutledes aatomituuma tekkimas üksikutest prootonitest ja neutronitest, on selge, et ka tuuma „kondenseerumisel” eraldub energiat ja kui tuuma saaks üksikuteks nukleonideks jagada, siis oleks selleks vaja samavõrra tööd teha.
Tuumade seoseenergiad on erinevad, sest tuumad on erineva suurusega. Kui jagada kogu tuuma seoseenergia nukleonide arvuga, saame eriseoseenergia – seoseenergia ühe tuumaosakese kohta, mis on samuti tuumati erinev (joonis 2.6.2.). Tavalise vesiniku tuumas on üks prooton, sellel tuumal seoseenergiat pole. Vesiniku rasketel isotoopidel, deuteeriumil , triitiumil ja heeliumi kergel isotoobil on tuumas mitu osakest ja nende eriseoseenergiad on juba suuremad. Ootamatult suure seoseenergiaga on tavaline heeliumi tuum.
Aatomituuma kihtmudel seletab seda analoogselt heeliumi keemiliste omadustega. Tuumaosakeste kihi täitumine põhjustab aatomi erilise stabiilsuse samamoodi nagu elektronkihi täitumine põhjustab keemilise inertsuse. Alates kolmandast perioodist kasvab eriseoseenergia tasapisi suuremate tuumade suunas kuni koobalti, raua ja niklini. Veel suuremad tuumad on justkui üleliia suured, et hästi koos püsida, ja perioodtabeli lõpuosas on eriseoseenergiad veidi väiksemad.
Vaatame veelkord tähtedes toimuvat tuumareaktsiooni, kus vesinik „põleb” heeliumiks. Algul on neli prootonit, lõpuks on üks -osake ja suur hulk energiat on kiirguse ning osakeste kineetilise energiana vabanenud (joonis 2.6.1.). Vabanev energia tuleb lähtetuumade ja lõppsaaduse seoseenergiate erinevusest.
Keemilistest reaktsioonidest võiks võrdluseks tuua maagaasi tõelise põlemise. Algul on metaani molekul ja kaks hapniku molekuli, lõpuks on süsihappegaasi molekul ja kaks vee molekuli ning vabanenud energia. Lähteainete ja saaduste keemiliste sidemete energia erinevusest tulevadki soojus, valgus ning mehaaniline töö, mida me maagaasi põletamisest ootasime.
Kirjeldet tuumareaktsioonis vabanev energia on keemiliste reaktsioonide omast võrratult suurem, seepärast ilmutab end siin maailmakuulus Einsteini massi ja energia seose valem . Reaktsiooni lihtsustatud massiarvestus:
- Kahe prootoni seisumass on kokku
- Kahe neutroni seisumass on kokku
- Eraldiseisvate osakeste mass kokku on
- -osakese seisumass on
- Masside vahe ehk -osakese massidefekt on Δm(α)=0,03037u=5,04306⋅10−29kg
-osakese mass on umbes kolme sajandiku aatommassi ühiku võrra väiksem, kui seda moodustavate nukleonide oma. Massi ja energia seose järgi on massidefekt ka seoseenergia. Kui süsteemist lahkub energia, siis väheneb ka mass.
Džaulides kirjutatuna tundub energia tühiselt väike, aga arvestagem, et see käib ühe osakese kohta. Tuumade seoseenergiad on mitu miljonit korda suuremad kui aatomite ionisatsioonienergiad. Näiteks metaani põlemisel
eraldub ühe molekuli kohta soojusena umbes 1,35·10-18 J.
Massi ja energia seos toimib muidugi ka keemilistes reaktsioonides, kuigi on otseseks mõõtmiseks liiga väike. Kui tulirelvas püssirohu põlemisel tekkinud gaasid saaks kokku koguda, jahutada ja ära kaaluda, ilmneks imetilluke massidefekt, mille põhjuseks on hajunud soojus, kiirgunud valgus ja kuuli minemalennutamiseks tehtud mehaaniline töö.
Tuumajõud ja seoseenergia
Aatomituumi hoiab koos tuumajõud. Tuuma osakesteks jagamiseks oleks vaja kulutada teatud energiakogus – seda nimetatakse seoseenergiaks. Kui tuum saaks üksikutest osakestest moodustuda, siis eralduks sama energia. Ühe tuumaosakese kohta arvutatud seoseenergia (eriseoseenerg
Otto Hahn, Lise Meitner ja Fritz Strassmann uurisid 1938. aastal Berliinis uraani töötlemist neutronitega. See tundus huvitav ja sama teemaga tegeldi Prantsusmaal ning Itaalias. Selleks ajaks oli palju teadlasi Saksamaalt lahkunud ja juulis ei jäänud ka Austria juudisoost Meitneril enam valikut. Ta põgenes Madalmaade kaudu Rootsi. Hahn kirjutas talle Berliinist, et uraani neutronitega pommitamise üks saadus on baarium. Teade oli nii uskumatu, et tekitas algul isegi analüüside ja katsetehnika suhtes kahtlusi. Kuni selle ajani ei olnud üheski tuumaprotsessis leitud aatomist eraldumas suuremaid kilde kui prootonid ja α-osakesed. Baariumi leidmine tähendas seda, et uraani tuum jaguneb mitmeks suureks tükiks. Eksperimendi tulemuste avaldamine üheskoos oli poliitilistel põhjustel võimatu, Hahn ja Strassmann saatsid oma artikli ära 1938. aasta detsembris.
Lise Meitner kohtus Kopenhaagenis töötava füüsiku Otto Frischiga ja arutas uraaniprobleemi. Nende tuumalõhustumise käsitlus ilmus 1939. aasta jaanuaris ja sisaldab viidet Einsteini valemile E=mc2. Samal ajal esitas Frisch ka teooria katselise kinnituse. Avastatud tuumareaktsioonis vabanev energia annab aimu tuumade seoseenergia suurusest, mis väljendub massidefektis (ptk Tuumareaktsioon). See ongi põhjuseks, miks uraani lõhustamise avastamist loetakse tuumarelva loomise eelduseks ja Einsteini valemit nimetatakse isegi aatompommi valemiks.
Uraan on viimane perioodtabeli looduslik element, tema tuum on väga suur, suure laenguga ja looduslikult radioaktiivne. Tilgamudelis (ptk Aatomituum), millest Meitner ja Frisch lähtusid, hoiab tuuma koos tuumajõududest põhjustatud „pindpinevus”. Positiivse laenguga prootonite tõukumine töötab väikese mõjuulatusega tuumajõududele vastu. Suur tuum on prootonite tõukumise tõttu viimasel püsivuse piiril ja valmis vähimagi häirimise (üksiku neutroni lisamise) peale lagunema. Neutroni haaramine muudab tuuma täiesti ebastabiilseks, see venib pikerguseks ja jaguneb kaheks enam-vähem võrdseks osaks. Tekkinud kildtuumad lendavad laengutevahelise tõukejõu mõjul laiali, aga nende kineetiline energia on nii suur, et ei seletu lihtsalt laengutevahelise tõukumisega. Selle suure energia allikas on lähtetuuma ja kildude seoseenergiate erinevus (ptk Tuumareaktsioon), st tuumaosakeste-vahelist seoste potentsiaalne energia. Raskete tuumade lõhustumise uudis levis teadlaste hulgas kiiresti. Ameerikasse viis teate konverentsile kiirustav Niels Bohr. Tuumaenergia kasutusvõimalused paistsid olevat käeulatuses, aga teoreetilised ja tehnilised probleemid olid endiselt suured. Lisaks sellele oli kohe algamas maailmasõda.
Ahelreaktsiooni võimalust tuumafüüsikas oli juba 1933. aastal ennustanud Ungari päritolu füüsik Leo Szilárd, aga ta ei leidnud aineid, millega see toimuda võiks. Kui selgus, et neutronite toimel lagunevas uraani tuumas tekivad uued neutronid, tundis Szilárd selles peituva võimaluse kohe ära. Koos teiste Ameerikasse põgenenud Ungari füüsikutega arutati võimalust, et Saksamaal on alustatud või kohe algamas tuumaenergia sõjalise rakendamise projekt ja otsustati juhtida sellele võimalusele Ameerika Ühendriikide valitsuse tähelepanu. Einsteini-Szilárdi kiri presidendile viis kokkuvõttes Manhattani projekti ja tuumarelva loomiseni. Einsteini veendi allkirja andma tema suure tuntuse tõttu ja see muutis kirja tõepoolest kaalukamaks.
Selleks, et kasutada tuumaenergiat, oli vaja lahendada mitmeid teoreetilisi ja tehnilisi probleeme. Looduslik uraan koosneb põhiliselt kahest isotoobist, üle 99,27% on uraan-238 ja 0,72% on uraan-235. Plahvatusliku ahelreaktsiooni annab uraan-235, mille omadused olid 1939. veel üsna tundmata. Isotoopidel on samad keemilised omadused, st tavalised ainete eraldamise meetodid uraan-235 kontsentratsiooni tõstmiseks ei sobi. Füüsikalistest rikastusmeetoditest katsetati algul gaasilise uraanheksafluoriidi () tsentrifuugimist, aga see osutus tehniliselt liiga keeruliseks ja kalliks. Kahe gaasi difusioonil põhineva ja ühe elektromagnetilise meetodi järjestikune rakendamine võimaldas tõsta uraan-235 kontsentratsiooni 89%-ni. 1945. aasta juulikuuks oli nii saadud umbes 50 kg pommi valmistamiseks sobivat materjali.
Tuumarelva arendamise teine suund keskendus plutooniumile. Plutoonium-239 leidub looduses nii vähe, et selle eraldamine maakidest ei tule kõne alla. Suure koguse plutooniumi tootmine on võimalik tuumareaktorites (ptk Tuumaenergeetika), kus uraan-238 muutub neutronite toimel läbi mitme beetalagunemise (ptk Radioaktiivsus ja kiirgus) plutoonium-239-ks.
Plutooniumi tekib üsna vähe ja see tuleb pärast reaktorist väljavõtmist eraldada. Erinevalt uraani rikastamisest saab siin kasutada keemilisi meetodeid, aga ka see oli algul lahendamist ootav probleem, sest plutooniumi omadusi polnud veel jõutud uurida. Tuumarelva loomise projekti kõige kulukamaks osaks saigi uraani rikastamine ja plutooniumi tootmine.
Ahelreaktsioon (ptk Tuuamreaktsioon ei arene plahvatuslikult väikeses uraani- või plutooniumitükis, sest palju tekkinud neutroneid pääseb ainest välja enne, kui nad kohtuvad järgmiste lõhustumisvalmis aatomitega. Ahelreaktsiooni kestmiseks piisavat aine kogust nimetatakse kriitiliseks massiks. Uraan-235 ja plutoonium-239 kriitilised massid on ideaaljuhul vastavalt 50 kg ja 10 kg. Reaalselt sõltub kriitiline mass aine puhtusest ja tihedusest, mõju avaldavad välistingimused nagu temperatuur ja neutronite tagasipeegeldamine. Tehniliselt on oluline ainetüki kuju. Näiteks kerakujulisena kriitilist massi ületav kogus on alakriitiline varrastena või rõngastena. Esimeste aatompommide loomiseks korraldati mõned lihtsad, kuid võrdlemisi riskantsed kriitilise massi eksperimendid, millest saadud andmed võimaldasid teadlastel asuda relva konstruktsiooni välja töötama (joonis 2.7.1.).
Esimeste aatompommide loomise teaduslike ja tehniliste probleemide kõrval tuli tegelda taktikaliste küsimustega. Pommide lõplik monteerimine ja kohaletoimetamise viisid vajasid läbitöötamist. Projekt pidi olema hoolega salastatud ja seegi polnud lihtne ülesanne. Teadlased osutusid tihtipeale isepäisteks ja probleemseteks isiksusteks. Rikastustehaste, laborite ja instituutide kümnetesse tuhandetesse ulatuvat tehnilist ja abipersonali püüti hoida teadmatuses saladusest, mille heaks töö käis. Administreerimine, logistika ja salastamine läks üldiselt hästi, aga sellele vaatamata õnnestus nõukogude agentidel info plutooniumipommi kohta välja viia. Nõukogude Liidu tuumaprogrammil oli kättesaadud dokumentidest palju abi. Praeguseks avalikustatud andmed viitavad, et Ameerika saladuste väljanuhkimine kiirendas nõukogude tuumaprogrammi mitme aasta võrra.
Manhattani projekti esimesed tuumapommid said valmis 1945. aastal. Esimene tuumakatsetus toimus New Mexico osariigis Almogordo polügoonil 16. juulil. Enne Teise maailmasõja lõppu otsustati lõhata kaks pommi (joonis 2.7.) Jaapani linnade kohal. Tuumarünnakuid Hirošimale ja Nagasakile on möödunud aastakümnete jooksul hinnatud erinevalt. Linnade hävitamist on õigustatud sõja kiire lõpetamise vajadusega. On tõsi, et Jaapan kapituleerus kohe pärast tuumarünnakuid. Samas ei ole kuidagi võimalik teada, milline oleks olnud sõja lõpp ilma tuumarelvadeta, mis oleks saanud edasi rahvusvahelistest suhetest ja kas aatompommid oleksidki jäänud lõhkema ainult katsepolügoonidel. Nõukogude tuumaprogramm arenes Los Alamosest lekkinud andmete tõttu kiiresti ja juba 1949. aastal jõuti esimese tuumakatsetuseni Semipalatinski tuumapolügoonil Kasahstanis.
| Joonis 2.7.2. Esimeste tuumarelvade hulka kuuluv "Väikemees" heideti 6. augustil 1945. aastal Jaapani linnale Hiroshima. Pommi kuju on funktsionaalne, tegemist on uraanitükkide kokkutulistamise kahuriga. | Tuumarelva "Paksuke" kuju on funktsionaalne, ümar kest mahutab kerakujuliselt paigaldatud lõhkelaenguid, mille kontrollitud plahvatus surub keskele tihedalt kokku plutooniumist tuuma. Pomm heideti 9. augustil 1945. aastal Jaapani linnale Nagasaki. |
Saksamaal alustati 1939. aasta aprillis tuumaenergia projektiga, mida tuntakse Uraaniühingu (Uranverein) nime all. Erinevate ametite alluvuses, vahepeal teadlaste sõjaväkke võtmise tõttu tööd katkestades ja jaotudes mitmete ülikoolide ning instituutide vahel, töötas projekt kuni sõja lõpuni. Arendati tuumareaktorit, toodeti uraani ja tegeldi uraani isotoopide eraldamise meetoditega. Projekt ei olnud edukas.
Polegi lõplikult selge, miks Werner Heisenbergi (ptk Määramatusseos) juhitud Saksa tuumaenergia programmil tuumarelv loomata jäi. Arvatavasti segunesid siin kolm olulist põhjust:
- Suhtumine füüsikutesse oli vastuoluline. Ühelt poolt tunnistati riiklikult teadusliku ja tehnilise arengu olulisust, teistpidi kahtlustati kõiki juudilikes teooriates ja juurutati puhast„saksa füüsikat”.
- Tuumaprogrammis kulub palju raha (materjale, energiat) ja see vajab palju tööjõudu. Mõlemaga oli sõdival Saksamaal kitsas käes.
- Teadlased, kes töötasid Heisenbergi juhtimisel, kõhklesid, kas see on ikka õige asi, milles nad osalevad ja kas üldse on võimalik saadaolevate vahenditega midagi saavutada.
Sõja lõpu eel uurisid Manhattani projekti erioperatsioonid Euroopas põhjalikult kõike tuumateadusega seonduvat. Sõjaline operatsioon Alsos korraldati otsimaks seadmeid, materjale ja dokumente. Üheksa Saksa tuumateadlast viidi mitmeks kuuks Inglismaale ülekuulamisele. Oranienburgi tuumareaktor hävitati. Selgus, et võrreldes Manhattani projektiga oli Saksamaa panustanud pommi loomisse väga vähe. Toimus ka nõukogude „Alsos”. Keiser Wilhelmi instituut ja Berliini tehnikakõrgkool olid linnast põhiosas ära kolitud ja tehnilist või teaduslikku teavet nõukogude poole kätte kuigi palju ei sattunud. Siiski oli pärast sõda palju Saksa teadlasi kaasatud nõukogude tuumaprogrammi.
Enne esimest tuumakatsetust analüüsiti võimalust, et plahvatuskeskmes väga kõrgele tõusev temperatuur võiks panna vesiniku aatomid (näiteks vees) ühinema heeliumiks (ptk Tuumareaktsioon), mis käivitaks nn superpommi ehk vesinikupommi. Arvutused näitasid, et seda ei juhtu. Lisaks kõrgele temperatuurile vajab „Päikese süütamine Maal” ka kõrget rõhku. Vesinikupommi väljatöötamine osutus väga mahukaks füüsikateooria ja matemaatika probleemiks, mille lahendamisele aitas palju kaasa esimeste elektrooniliste arvutite, ENIAC ja MANIAC kasutamine. Teise maailmasõja järgne võidurelvastumine viiski kergete tuumade sünteesil põhineva termotuumarelva väljatöötamiseni 1950-ndate keskel. Tavalist vesinikku või vesinikku vee molekulides ei saa maapealsetes tingimustes niimoodi ühinema panna, nagu see toimub tähtedes. Termotuumapommi lõhkeaineks on vesinik-2, deuteerium. Deuteeriumi tuumas on üks prooton ja üks neutron, massiarv kaks. Loodusliku vesiniku hulgas on deuteeriumi 0,01%. Siiski on puhta deuteeriumi või selle ühendite eraldamine mõnevõrra lihtsam, kui oli uraani isotoopide eraldamine, ja vastavaid tehaseid ehitati juba alates 1930-ndatest mitmel pool maailmas.
Kuigi veeldatud deuteeriumi plahvatamapanek tavalise aatompommi toimel osutus võimalikuks (esimene katsetus 1953), polnud reaalne sellist pommi sõjaliselt kasutatavaks, st kohaletoimetatavaks teha. Hiljem katsetatud väiksemates ja kergemates seadmetes kasutati liitiumi ja raske vesiniku ühendit, liitiumdeuteriidi. Sütikuna kasutati kaheastmelist plutooniumpommi. Plahvatuses vabanenud neutronid tabavad liitiumi tuumi, tekib palju triitiumi (vesinik-3, üliraske vesinik). Triitiumi ja deuteeriumi ühinemise saaduseks on heelium-4 tuumad ja neutronid, vabaneb väga palju energiat.
Tuumaplahvatus on lõhkeaine plahvatusest erinev. Kõrge temperatuur ja lööklaine tekivad mõlemal juhul, aga just plahvatuse võimsus on erinev. Tuumarelvas vabaneb väga palju energiat mõne millisekundi jooksul. Osa energiast tekitab hävitava kiirgusimpulsi, temperatuur plahvatuse keskmes tõuseb mitme miljoni kraadini ja sellega kaasneb ülitugev lööklaine. Tuumapommide plahvatusi hinnatakse võrdluses tavalise lõhkeaine, trotüüli ehk trinitrotolueeni (TNT) plahvatusega. Kuigi tuumaplahvatuse iseloom on tavalõhkeainete omast erinev, saab trotüüliekvivalendi kaudu plahvatustel vabanevat energiat võrrelda. Esimese tuumakatsetuse eel lõhati jälgimisseadmete ja mõõteriistade kontrollimiseks polügoonil 100 t trotüüli. Tuumaplahvatus osutus võrdseks 20 000 t lõhkeaine plahvatusega. Trinity oli niisiis 20 kt (kilotonnine) pomm, energiat vabanes 8,4·1013 J=84 TJ. Hirošimale ja Nagasakile heidetud pommid olid vastavalt 13 kt ja 21 kt. Megatonniste plahvatuste piir ületati vesinikupommidega. Nõukogude Liidus projekteeriti 100 Mt Tsaar Pomm, mis ehitati katsetuse jaoks poole võrra vähendatud variandis ja plahvatas Novaja Zemlja polügoonil 1961. aastal. See on suurim plahvatus, mille inimesed on korraldanud. Kõige suurem teadaolev plahvatus enne aatomiajastut arvatakse olevat 1917. aasta õnnetus lõhekaineid vedanud Prantsuse kaubalaevaga. Arvestuslik trotüüliekvilaent oli 2,9 kilotonni.
Tuumaplahvatusega seostatud seenekujuline pilv tekib tegelikult teistegi suurte plahvatuste, nt vulkaanipursete ja metsatulekahjude korral. Tuumaseen kerkib plahvatustel, mis toimuvad maapinnal, maa või vee kohal. Udust, suitsust, pinnasetolmust, purustatud ja osaliselt aurustunud kivimitest ning pommi enda jäänustest koosneva pilve kõrgus sõltub pommi tüübist ja plahvatusel vabanevast energiast. Vesinikpommide katsetused on näidanud, et alates 1 Mt plahvatusest võib tuumaseen tõusta 20 km kõrgusele ja viia stratosfääri suurel hulgal gaase ning tolmu, sh radioaktiivseid aineid (ptk Radioaktiivsus ja kiirgus).
Tuumarelvade valmistamise saladus oli 1950-ndate alguseks avalikuks saanud ja võidurelvastumise hoos kasvasid nii tuumaarsenalid kui ka tuumariikide nimekiri. Tuumarelvade arvu loetakse kasutusvalmis ja kiiresti valmisseatavate lõhkepeadena. Arvesse ei lähe lahtivõetud ja hävitamist ootavad lõhkepeade osad ja pooleliolevad seadmed. Mahakantud ja poolelijäänud tuumapommid on potentsiaalselt ohtlik materjal, sest nende üle peetav arvestus on katkendlik. Tuumarelvade laoseisu maksimum oli 1986. aasta paiku, koguarv ületas siis 65 000 lõhkepead. USA maksimum oli 1966. aastal, Nõukogude Liidu maksimum oli 1986. või 1987. aastal. Teistel tuumariikidel on arvatavasti kunagi olnud kokku umbes tuhat lõhkepead. Kui kõik maksimumid oleks kokku langenud, võinuks olla korraga umbes 73 000 lõhkepead. Ei ole teada, kui palju lõhkepäid on üldse toodetud, hinnatakse, et üle 130 000. Neist veidi üle 2000 on lõhatud tuumakatsetuste tarvis. Pärast külma sõja lõppu on palju tuumarelvi hävitatud või hävitamiseks ette valmistatud ja 2013. laoseisuks arvatakse umbes 17 300 lõhkepead. Põhiosa sellest on endiselt vanade tuumariikide, enamalt USA ja Venemaa käsutuses.
Tuumariike on üheksa: Ameerika Ühendriigid (esimene katsetus 1945), Venemaa (1949), Ühendkuningriik (1952), Prantsusmaa (1960), Hiina (1964), India (1974), Pakistan (1998), Põhja-Korea (2006). Iisraeli peetakse kindlalt tuumariigiks, aga ametlikku kinnitust sellel pole. On võimalik, et Iisrael tegi koostööd Lõuna-Aafrika vabariigiga ja korraldas tuumakatsetuse 1979. aastal India Ookeanis, aga ka seda varjab ametlik vaikimispoliitika. Lõuna-Aafrika Vabariik on oma 1980-ndatel valmistatud tuumarelvadest täielikult loobunud. Nõukogude Liidu lagunemisega iseseisvunud riikide territooriumil olnud lõhkepead viidi Venemaale. Nii jäid tuumariikide nimekirjast välja Ukraina, Valgevene ja Kasahstan. Iraani tuumprogrammi eesmärk on 2013. aasta seisuga lahtine.
20. sajandi teisel poolel sai tuumaohutusest oluline rahvusvaheliste suhete ja koostöö teema. Probleem on mitmetahuline: tuumarelvade tootmine, hoidmine ja lõpuks ka hävitamine, tootmisjääkide käitlemine ja ladustamine, tuumakatsetuste mõju ookeanile, atmosfäärile ja inimeste tervisele, tuumareaktorite töökindlus, jäätmete töötlemine ja pikaajaline säilitamine, radioaktiivsete ainete kasutamine meditsiinis ja tehnikas jpm. Suurriikide ladudesse kogunesid tuhanded lõhkepead, mis kergitas küsimuse suuremahulise tuumasõja puhkemisest ja selle võimalikest tagajärgedest. Nõukogude Liidus, Ameerika Ühendriikides ja teisteski riikides püüti näidata tuumasõda kaunis kergesti üleelatavana ja elanikkonda selleks ette valmistada. Kindralid kippusid uskuma, et tuumasõda on võidetav, isegi mõistlik, koguni paratamatu. Samal ajal suurenes tuumakatsetuste ja vulkaanipursete uurimise andmestik, atmosfääri- ja kliimamudelid arenesid arvutustehnika täiustumise toel üha edasi. Tuumasõja tagajärgede mudelid näitavad, et tuumaseentega ülestõstetud tolmust ja tulekahjude suitsust muutuvad päevad pimedaks (tuumaöö) ja suved jäävad ära (tuumatalv). Stratosfääri ulatuvad pilved rikuvad osoonitasakaalu aastakümneteks. Sajab musta radioaktiivset vihma. Võib-olla ei ole see kõik nii hull, need on ikkagi ainult mudelid ja tagajärjed sõltuvad plahvatuste arvust ning kohast, aastaajast jpm. Diskussioon tuumatalve teemal on olemuslikult sarnane vaidlusega üldise kliimasoojenemise üle. Majanduslikel ja poliitilistel põhjustel hinnatakse mudelite järeldusi ja puudusi oma mätta otsast ning halvustatakse vastasleeri. Praegu on siiski üsna selge, et Hiina kommunistlik juht Mao Zedong eksis rängalt, kui ta 1957. aastal ütles:
„Kujutleme, kui palju inimesi sureb sõja puhkemise korral. Maailmas on 2,7 miljardit inimest ja kolmandik hukkub. Või natuke rohkem, võib-olla pool. Ma ütlen, et kui juhtub halvim ja pool sureb, siis pool jääb ikkagi alles. Aga imperialism on maatasa tehtud ja kogu maailm saab sotsialistlikuks. Mõne aasta pärast on inimesi jälle 2,7 miljardit.”
J. Robert Oppenheimer oli Manhattani projekti teadusdirektor. Tehniliselt ja sõjaliselt poolelt juhatas kindral Leslie Groves. Oppie, aatompommi isa, nagu teada tunti 20. sajandi keskel, on paljudele teadlase isiklike tõekspidamiste ja riiklike huvide kokkupõrke sümbol.
Oppenheimer õppis nooruses võrdse vaimustusega loodusteadusi, matemaatikat ja keeli. Hea mälu ja keeletaju võimaldas tal korraga tegelda kreeka, ladina, prantsuse ja saksa keelega, ajendiks tihti soov lugeda huvitavaid autoreid originaalkeeles. Kogu elu huvitus ta klassikalisest ja idamaade filosoofiast.
Pärast õppimist Harvardis ja Cambridge’i ülikoolis Rutherfordi juures sai ta doktorikraadi Saksamaal ning pöördus Ameerikasse tagasi 1929. aastal. Oppenheimer oli erakordselt andekas õppejõud ja suurepärane teoreetik. California ülikoolis Berkeleys ja California tehnoloogiainstituudis töötades avaldas ta mitmeid ennustuslikke ideid, mis puudutasid neutroneid, positrone, neutrontähti – kui nimetada ainult tuntumaid. Pikka kasvu, kõhn, energiline, intensiivne, kaasahaarav, särav – need on sõnad, millega õpilased ja kolleegid teda iseloomustasid.
Teoreetilise füüsika uuringud haarasid teda sedavõrd, et ta elas tihti justkui omas maailmas, lugemata uudiseid ja kuulamata raadiot. 1930-ndate poliitilised sündmused maailmas köitsid siiski ta tähelepanu ja ta võttis väga selge fašismivastase seisukoha. 1942. aasta juunist asus Oppenheimer Manhattani projekti juhtima. Parimate teadlaste koondamine Los Alamose teaduskeskusesse on kindlasti Oppenheimeri energia ja suhtlemisoskuse teene. Lõpuks juhtis ta üle kolme tuhande töötajaga keskust, lahendades samas pidevalt teoreetilisi ja tehnilisi probleeme. Ometi ei tunnistatud tema sobivust direktori kohale alguses kuigi kergelt. Juhtimiskogemusi tal eriti polnud, tema lähedased olid seotud kommunistliku parteiga, ta polnud isegi, erinevalt teistest kandidaatidest, Nobeli preemia laureaat. Vaatamata võimude pidevatele kahtlustele ja arvatavale turvariskile oli kindral Groves siiski kindel, et paremat meest projekti juhtima pole olemas. Tagantjärele on kõik tunnistanud, et tal oli õigus.
Esimese tuumakatsetuse jälgimist meenutas Oppenheimer aastaid hiljem kahe tsitaadiga hinduismi pühast tekstist Bhagavadgītāst: „Kui tuhande Päikese helendus sööstaks korraga taevasse, oleks see nagu kõigevägevama hiilgus.” ja „Nüüd on minust saanud Surm, maailmade hävitaja.”
Pärast sõda juhatas Oppenheimer USA Aatomienergia Komisjoni. Vesinikupommi loomist ta algul ei toetanud, aga vaatamata kõhklustele loobus siiski otsesest vastuseisust. Kommunismihirmu laineharjal tuletati nüüd jälle meelde tema vasakpoolseid vaateid ja lähedasi suhteid kommunistidega enne sõda. Uurimine viis selleni, et Oppenheimeri luba töötada riigisaladustega tühistati, tema töö Aatomienergia Komisjonis ja vesinikupommi projektis lõppes.
Kaotanud võimaluse mõjutada teaduspoliitikat, jäi Oppenheimer ometi Princetoni Instituudi direktoriks, pidas loenguid Euroopas ja Jaapanis, ta valiti paljude ülikoolide audoktoriks ja teadusseltside liikmeks. Teda tunnustasid nii teadlased kui ka poliitikud. Praegu, kui isegi Venemaal avanevad veidi tuumasaladuste arhiivid, on üsna kindel, et kuigi Oppenheimer oli 1930-ndatel lähedalt seotud kommunistide ja kommunistliku parteiga, ei saanud nõukogude luure tema kaudu mingit informatsiooni, kuigi proovis.
1950-ndate keskpaigast alates veetis ta pikki kuid oma väikeses rannamajas Neitsisaartel, kus purjetas koos naise ja tütrega merel ning kirjutas raamatuid eetika ning moraali teemadel. Oppenheimer oli noorusest saadik ahelsuitsetaja. 1966. aastal diagnoositi tal kõrivähk ja ta suri Princetonis veebruaris 1967.
Aatomituumade siseenergia muutmine elektrienergiaks on alates 20. sajandi keskpaigast saanud tavaliseks. Tuumaenergeetika on suur teadus- ja tööstusharu. Kasutuses on palju erineva tuumkütusega reaktoritüüpe, neutronite voogu aeglustatakse ja kontrollitakse mitmel moel ja konstruktsioonilisi lahendusi on samuti palju. Kõige üldisemalt (joonis 2.8.1.) on tegemist soojuselektrijaamaga, kus generaatorite pööritamiseks kasutatav kuum aur saadakse reaktoris tuumareaktsioonil vabaneva soojusega vett keetes.
Reaktor on seade, milles toimub tuumareaktsioon, kus seda kontrollitakse ja kust vabanenud soojus viiakse soojuskandjaga välja. Reaktori konstruktsioon, materjalid, kaitsekest ja turvasüsteemid võivad neil harvadel juhtudel, kui midagi valesti läheb, tuumaõnnetuse tagajärgi leevendada või isegi päris ära hoida.
Tuumkütuseks on aineid, mis aatomituumadega toimuvate protsesside, olgu lagunemise või liitumise tulemusena võimaldavad tuumade siseenergiat teisteks energialiikideks muuta. Tihti nimetatakse tuumkütuseks ka valmismaterjale (koos kesta, täiteainete, aeglustajate jm-ga), mis on toodetud tuumareaktorisse paigutamiseks. Kõige tavalisemad tuumkütused on uraan-235 ja plutoonium-239, milles tekib aeglaste neutronite toimel ahelreaktsioon. Uraan-238, mida on looduslikus uraanis kõige rohkem, laguneb kiirete neutronite toimel, ahelreaktsiooni ei teki. Uraan-238 tuumad haaravad neutroneid ja neist saab pärast kahte beetalagunemist (ptk Radioaktiivsus ja kiirgus ja Manhattani projekt)
tuumkütus plutoonium-239. Kütus pannakse reaktorisse enamasti varrastena, mis olenevalt reaktori tüübist sisaldavad veel struktuurseid materjale, neutronite aeglustajaid või neutronite peegeldajat.
Neutronite aeglustamiseks on reaktoris tuumkütuse hulka või vahele lisatud aineid, mille tuumadega põrkudes kaotavad neutronid kineetilist energiat. Aeglustamine on vajalik, sest kütuse tuumad haaravad ainult aeglasi neutroneid piisavalt suure tõenäosusega, et ahelreaktsioon saaks püsida. Aeglustiks sobivad ained on näiteks süsinik (grafiit), vesi, raske vesi, berüllium. Hea aeglusti ei neela neutroneid ega sisalda neutroneid neelavaid lisandeid. Tuumareaktorite väljatöötamise algusaegadel oli probleeme puhta süsiniku tootmisega, näiteks boorilisandiga grafiit ei sobi reaktorites kasutamiseks. Saksamaa tuumaprogrammi luhtumise üheks põhjuseks Teise maailmasõja ajal oli saadaoleva grafiidi liiga suur boorisisaldus.
Ahelreaktsiooni juhtimiseks kasutatakse kontrollvardaid, mis valmistatakse neutroneid neelavast ainest, põhiliselt kaadmiumist, indiumist ja hõbedast, aga ka paljudest teistest metallidest või ühenditest. Kontrollvardaid reaktoris kütuse vahele pistes või neid sealt välja tõmmates reguleeritakse neutronite arvu ja seekaudu reaktsiooni kulgu. Reaktsiooni saab kontrollida ka reaktorist läbi voolava soojuskandja kaudu, selleks lisatakse sinna booriühendeid.
SCRAM on ahelreaktsiooni peatamine avariiolukorras või teatud sorti avariikahtluse korral. Näiteks Jaapanis on SCRAM-i käivitamine kohustuslik kõigis tuumajaamades maavärina korral ja toimub tavaliselt automaatselt. Nimi pärineb esimeste tuumareaktorite katsetamise aegadest, kui varraste reaktorisse viimist nimetati skrämmimiseks. Hiljem mõeldi välja, et SCRAM-i tähendus võiks olla julgestuse kontrollvarda kirvemees (safety control rod axe man). Kõige esimese tuumareaktori käivitamisel olevat tõesti ühe mehe ülesandeks jäetud hädaolukorrasläbi raiuda köis, millega oli üles riputatud üks lisavarras. See varras oleks kukkunud reaktorisse ja peatanud kontrolli alt väljuva ahelreaktsiooni. Esimest SCRAM-i ei läinud vaja.
Aastakümnetega on projekteeritud ja läbi proovitud väga palju erineva konstruktsiooni ja mitmete soojuskandjatega reaktoreid. Kõiki variante ei jõua nimetadagi, aga märkimist väärivad järgmised:
- Survevee reaktorid (PWR - pressurized water reactors), kus tavaline vesi kõrgel rõhul ja temperatuuril kannab soojuse boilerisse. Boilerist saadud aur suunatakse turbiinile. Vesi toimib ka neutronite aeglustajana.
- Keeva vee reaktorid (BWR - boiling water reactors), kus vesi keeb reaktori sees, tuumkütuse varraste vahel, ja aur suunatakse sealt otse turbiinile. Vesi (täpsemalt iga vesiniku tuum vee molekulis) on neutronite aeglustaja, aga kahjuks ka üsna hea neutronite neelaja. Veega jahutatavas reaktori tuumas peab kasutama rikastatud uraani.
- Suure võimsusega kanalreaktor (RBMK - pеактор bольшой mощности kанальный - РБМК), Nõukogude Liidus välja töötatud üsna ebatavaline grafiitaeglustiga reaktoritüüp, mida praegu enam ei ehitata. Kolm veel töötavat jaama peaksid reaktorid sulgema 2030. aastaks. Pärast õnnetust Tšernobõlis on käiku lastud ainult üks selline reaktor.
- Raske vee reaktorid, mis kasutavad neutronite aeglustajana ja osaliselt ka soojuskandjana rasket vett (D2O). Deuteerium on hea aeglustaja ja ei neela neutroneid, seepärast saab raske vee reaktorites kasutada rikastamata uraani. Kanadas on kõigis tuumajaamades CANDU (CANada Deuterium Uranium) raske vee reaktorid, neid on projekteeritud ka teistesse maadesse.
- Gaasjahutusega reaktorite variandid, mis kõlbavad hästi nii jõujaamadeks kui plutooniumi tootmiseks, töötati välja Ühendkuningriigis ja Ameerika Ühendriikides. Grafiitaeglustaja ja gaasilise soojuskandjaga jaamu arendatakse edasi ja peetakse perspektiivikaks.
- Sulatatud soolad ja metallid on soojuskandjatena suhteliselt ohutud, neid kasutatakse muuhulgas aatomiallveelaevadel. Sulatatud sooladega reaktoris on võimalik, et soojuskandja on ühtlasi ka kütus.
Tuumareaktorite tehnilist täiustumist, turvalisuse nõudeid, vastavat seadustikku ja rahvusvahelist kontrolli kirjeldatakse reaktorite põlvkondadega:
- I põlvkonda kuuluvad katseseadmed, prototüübid ja mõned proovireaktorid, mida ärilistel eesmärkidel käiku ei lastudki. Praeguseks on need kõik suletud, mitmeid hoitakse alles tehnikaajaloo mälestistena.
- II põlvkonnaks on põhiosa praegu töötavaist reaktoreist, mis said valmis aastatel 1965 kuni 1996. Nende jaamade tööeaks oli arvestatud 30 kuni 40 aastat, aga mõned neist on juba ümber ehitatud toimima 50 või 60 aastat ja arvatakse, et osa jaamu võib parandamise ja täiustamisega vastu pidada 80 aastat. Mõned II põlvkonna jaamad on ehitatud isegi pärast 2000. aastat, neis on parandatud turvalisust ja planeeritud, et ilma suurema ümberehituseta töötavad 60 aastat. Neid jaamu loetakse mõnikord põlvkonda II+.
- III põlvkonna jaamade projekteerimise põhimõtted kujunesid välja 1990-ndateks. Neis uutes jaamades on parandatud kütusetehnoloogiat, on rohkem tähelepanu pööratud passiivturvalisuse meetmetele, vähendatud hooldevajadust ja tõstetud efektiivsust. Ühtlasi on neid jaamu odavam ehitada ja kasulikum pidada. Paljud praegu töötavad ja ehitatavad jaamad kannavad tähiseid III+ ja III++.
- IV põlvkonna jaamu pole veel ehitatud ja kuigi uurimine käib, pole lootust nendega turule tulla enne 2030. aastat.
- V põlvkonna tuumajaamade põhimõttelist võimalikkust on arutatud. Kuigi uurimisteemasid oleks, pidurdavad esialgu konkreetsemaid plaane majanduslikud ja turvakaalutlused.
Esimene tuumareaktor käivitati 1942. aastal Chicago ülikoolis Enrico Fermi juhitud töörühma poolt. Algul oli selliste reaktorite loomise eesmärgiks uurida ahelreaktsiooni toimumise tingimusi, juhtimise võimalusi ja toota plutooniumi. 1950-ndate jooksul arendati välja elektrienergia tootmiseks sobivad seadmed ja tuumajaamade arv kasvas kiiresti. 2013. aastaks oli maailmas umbes 435 töötavat tuumelektrijaama, planeeritud koguvõimusega üle 370 GW. Läbi tuumaenergeetika poolsajandi on kõige rohkem jaamu ehitatud Ameerika Ühendriikides, Prantsusmaal, Jaapanis ja Nõukogude Liidus. Ehitamine käib umbes 70 tuumajaamas, mis peaksid lähematel aastatel lisama 65 GW võimsust. Uusi jaamu ehitatakse ja projekteeritakse suuremalt jaolt Venemaal, Hiinas, Indias ja Lõuna-Koreas. Paljud riigid on loobunud uute tuumajaamade planeerimisest ja asunud vanu sulgema.
Tuumaelektrijaamade sulgemise ja ehitamisplaanidest loobumise põhjused on osaliselt majanduslikud. Uraani hind on tõusnud ja ehitusnormid karmistunud, mis teeb kallimaks nii jaamade püstitamise kui ka igapäevase käigushoidmise. Teiselt poolt on igasuguse tuumatehnoloogia kasutamine ühiskondlik ja psühholoogiline probleem, mis tuleneb kahest ohust:
- On hea, et tuumajaamal ei ole tossavaid korstnaid ja suuri tuhavälju (joonis 2.8.1.). Arvestades jaamade pikka iga, on jäätmeid silmapaistvalt vähe. Vastukaaluna on tuumajäätmete käitlemine, transport ja säilitamine keerukas ning kallis. Jäätmeid ei saa peaaegu üldse uuskasutusse võtta, nad ei muutu ohutuks ka väga pika aja jooksul. Hoidlaid peab kontrollima, valvama ja ümber korraldama sadu, osaliselt isegi tuhandeid aastaid. Mitte keegi ei taha oma maale tuumajäätmete hoiupaika.
- Elektrijaam on suur ettevõte, mis toimib paljude keerukate seadmete koostöös. Seal töötab palju erinevate väljaõpete ja ülesannetega inimesi. On praktiliselt võimatu, et nii suures süsteemis ei lähe midagi rikki, ei kulu üle piiri, keegi ei tee valeotsust. Nii on see kõigis suurtes tööstusettevõtetes ja tuumajaam ei ole siin erandiks. Eripära on see, et kui mitu õnnetut juhust kokku satuvad, võivad tagajärjed inimestele, jaamale ja kahjuks ka väga laiale ümbrusele olla katastroofilised.
1957. aastal asutatud Rahvusvaheline Aatomienergia Agentuur (IAEA) on praeguseks seadnud kolm suurt eesmärki:
- aatomienergia rahumeelse kasutamise edendamine;
- kontroll tuumatehnoloogiate, -materjalide ja -seadmete kasutamise üle nii palju kui see võimalik on, et vältida edaspidi igasugust sõjalist kasutust;
- tuumajaamade ohutuse parandamine.
IAEA registreerib ja klassifitseerib tuumajaamades juhtunud õnnetusi. Vastav juhtumite skaala INES, (joonis 2.8.2.) koostati 1989. aastal. Juhtumite kirjeldamine ja hindamine ei ole lihtne, arvesse võetakse juhtumi tulemusel tekkinud radioaktiivse saastumise ulatust, surmajuhtumite arvu, tagajärgede likvideerimise kulusid ja arvatavate keskkonnamõjude ajalist ulatust. INES ei ole täpne teaduslik mõõdupuu, pigem on see vahend juhtumite ja õnnetuste kõige üldisemaks kirjeldamiseks, näiteks suhtlemisel ajakirjandusega. Selle järgi on kirjeldatud ka vanemaid õnnetusjuhtumeid. Kõike kokku võttes on tuumaajastu jooksul (veidi üle poole sajandi) juhtunud umbes 25 raskemat õnnetust. Märgiliste, väga suure ühiskondliku mõjuga sündmustena nimetatakse tavaliselt kolme:
1) Three Mile Islandi (USA) jaama teise reaktori jahutussüsteemi häire ja vee temperatuuri tõusu peale käivitus automaatne väljalülitamine (SCRAM), täpselt nii nagu see on ette nähtud. Üks väljalülitamisel 10 sekundiks avatud kaitseventiilidest ei sulgunud, kuigi kontrollseadmed näitasid, et on sulgunud. Ajaga, mis kulus tekkinud probleemide lahendamiseks, jõudis välja voolata nii palju jahutusvett, et reaktori tuum sulas osaliselt üles. Vigastatud ja endiselt väga kuuma reaktori jahutamine osutus tehniliselt keerukaks. Reaktori konstruktsioon pidi igal juhul vältima radioaktiivsete ainete kaitsekestast välja pääsemist, aga mitme õnnetu juhuse kokkulangemise tõttu jõudis reostunud jahutusvesi siiski abihoones asunud mahutisse ja väike kogus radioaktiivset ainet (põhiliselt gaasilised ksenoon ja krüptoon) lekkis keskkonda. Gaaside keemilise inertsuse ja väikese koguse tõttu ei olnud jaama ümbrusele mõõdetavat mõju, inimesed viga ei saanud. Kaitsekest pidas vastu, sulanud ained välja ei voolanud. Kuu ajaga suudeti reaktori temperatuur viia alla 100 kraadi ja rõhk atmosfääri rõhuga võrdsustada. Juhtumi tagajärgede likvideerimine algas augustis 1979, reaktori kaas avati juba juulis 1984 ja detsembris 1993 loeti tööd ametlikult lõppenuks. Teine reaktor on siiski arvel ajutise tuumajäätmete hoidlana, mida säilitakse ja jälgitakse samas kohas vähemalt kogu jaama sulgemiseni aastal 2034.
Vaatamata sellele, et õnnetus lõppes nö õnnelikult, tekitas see ühiskonnas erakordselt laia vastukaja. Esimest korda tuli ilmsiks, et paari aastakümnega harjumuspäraseks muutunud tuumaenergeetika võib tehniliste rikete, inimlike eksimuste, unustamise ning kommunikatsiooniraskuste tagajärjel muutuda ootamatult ohtlikuks. Üle maailma toimus tuumaenergia kasutamise vastaseid meeleavaldusi, korraldati koosolekuid ja kontserte, kirjutati artikleid ja raamatuid. Protestid olid suunatud jaama omaniku, uurimiskomisjoni, riigi ja ka teadlaste ning inseneride vastu. Paljud inimesed nõudsid ja ka said kompensatsiooni neile tekitatud kahjude, rikutud karjääri ja tervise eest. Sündmus võttis tuumaenergeetika arengul tublisti hoogu maha.
2) Tšernobõlis töötas Nõukogude Liidus projekteeritud RBMK tüüpi reaktor, mis oli ebatavaline nii põhimõttelt, konstruktsioonilt kui ka ehitustehniliselt. Selliseid esitati kui nõukogude tuumateaduse ja energeetika suursaavutusi, aga töökindluse, ahelreaktsiooni juhtimise ja avariiolukordade lahendamise probleemid ei olnud tegelikult kuigi kindlalt lahendatud. Suurõnnetus Tšernobõlis sai alguse planeeritud elektrisüsteemi avariilahenduse katse ajal, millega alustati 25. aprillil 1986. Kohaliku elektrivõrgu dispetšeri nõudel lükati katse edasi ja hilisem aeg langes kokku öövahetuse tööletulekuga. Uus vahetus ei olnud elektriinseneride planeeritud katse käiguga kuigi täpselt kursis ja tegi reaktori juhtimisel mitu valeotsust. Päris täpselt ei ole vigade kuhjumise käik ja põhjused teada, sest mitu kontrollruumi töötajat suri kiirituse tagajärjel juba mõne nädala pärast. Katseplaanis ettenähtud reaktori võimsuse vähendamisel tekkis reaktoris lühikese poolestusajaga (ptk Radioaktiivsus ja kiirgus) ksenoon-135, mis on neelab neutroneid ja pärsib sellega ahelreaktsiooni veelgi. Sellist ebastabiilset olukorda nimetavad tuumainsenerid reaktori mürgitumiseks. Võimsus langes väga madalale, aga seda õnnestus käsitsijuhtimisega siiski veidi tõsta ja enam-vähem stabiliseerida. Vaatamata reaktori kahtlasele käitumisele ja liiga väiksele võimsusele jätkati ettevalmistusi katseks. Tervelt kümne minuti jooksul ei tehtud välja mitmetest juhtimissüsteemi alarmidest. 26. aprillil kell 1.23.04 katse algaski. Mürgitunud reaktor, mis töötas madalamal võimsusel, kui katsetingimused ette kirjutasid, käitus ebatavaliselt ja juhtimisarvuti jätkas alarmeerimist.
Kell 1.23.40 vajutas keegi avariisulgemise nuppu ja käivitas SCRAM-i, mis ei olnud kohane ja läks täiesti valesti. Reaktori võimsus tõusis kiiresti kümme korda suuremaks maksimaalsest projekteeritud võimsusest. Tekkis väga palju ülikuuma auru, mis sai esimese plahvatuse põhjuseks. Teine, palju võimsam plahvatus toimus kolme sekundi pärast. Teise plahvatuse põhjus ei ole teada. Võimalik, et ka siin oli tegemist auruga. Kütusevarraste tsirkooniumkatte, grafiidi, kuuma veeauru ja õhuhapniku reageerimisel võis tekkida vesiniku ja vingugaasi segu, mis on samuti väga plahvatusohtlik. Radioaktiivse reostuse uurimise järgi on arvutatud, et mingi osa sulanud reaktori tuumast võis plahvatada nagu ebaõnnestunud tuumapomm, umbes 10-tonnise trotüüliekvivalendiga. Igal juhul oli just teine plahvatus see, mis purustas reaktori ja seda ümbritsenud hoone. Kütuse ja aeglusti laialipaiskamine peatas ahelreaktsiooni, aga süütas ümbruses mitu tulekahju. Reaktori varemed hõõgusid punaselt, grafiit ja ehitusmaterjalid põlesid lahtise leegiga. Õhku tõusis enneolematu radioaktiivse tolmu ja gaasi pilv, mis saastas ümbruskonda ja levis üle paljude Euroopa riikide. Hilisemad mõõtmised on näidanud, et kõige hävitavama reostuse osaliseks said reaktori lähima ümbruse kõrval mõned Valgevene piirkonnad.
Katastroofi sügavamad põhjused on jäänud igikestva vaidluse teemaks. Nõukogude Liidu juhtkond viivitas õnnetusest teatamisega ja püüdis mitmeti tulemusi pisemana näidata. Algul suunati kõik põhimõttelised süüdistused tuumajaama töötajate vastu. Ei saa eitada, et juhtimisruumis tehti vigu ja tagantjärele võiks operaatoritele õpetada, kuidas õnnetust ära hoida. Hiljem on siiski selgunud, et RBMK tüüpi seadmetel oli olulisi puudusi, reaktor oli halvasti projekteeritud ja ehitatud ning mitu muude riikide tuumareaktorites täiesti tavalist turvalahendust oli üldse rakendamata. Tuumatehnoloogia salastamine ja energeetika juhtimine ideoloogilisel alusel tegi võimatuks vigadest õppimise.
Tšernobõli katastroofi tagajärgede likvideerimisele kaasati sõjavägi, suure töö tegi ära kordusõppuste ettekäändel kogutud reserv. Päästetöödeks ei oldud valmis ja kõik osutus väga keeruliseks. Teha oli palju: ümbruskonnast pidi elanikud teadmata ajaks evakueerima (üritades seejuures paanikat vältida), tulekahju tuli summutada, reaktori varemed oli vaja kinni katta ja pikaajaliseks säilitamiseks ette valmistada, sulanud reaktorituumast tekkinud „laava” pinnasesse jõudmist pidi iga hinna eest vältima (seejuures ei olnud teada, mis reaktorihoone alumistes ruumides toimub), ümber plahvatanud reaktori vedelev surmavalt radioaktiivne praht (kütuse, aeglusti ja reaktori tükid) oli vaja kokku korjata, saastunud alad, tehnika, seadmed jm vajasid puhastamist, valvamist ning kontrollimist, suur inimvägi tuli majutada ja toita jpm. Pingelises olukorras oli palju segadust, infosulgu ja probleeme, aga suures osas olid tehtud otsused siiski õiged.
Kolm terveksjäänud reaktorit pandi mõneks ajaks seisma, aga kuna elektrienergiat oli hädasti vaja, käivitati juba samal aastal uuesti. Lõplikult suleti Tšernobõli elektrijaam 2000. aastal. Õnnetuse tekitatud kahjud ja päästetööde kulud on kokku liidetud, aga täit selgust neis siiski ei ole. Jaama lahtivõtmine ja suletud tsooni valvamine tekitab Ukraina riigile jätkuvalt (tõenäoliselt vähemalt 300 aasta jooksul) suuri kulusid.
3) Fukushima tuumajaamas on kuus erineva vanusega ja mitmelt tootjalt pärit keeva vee reaktorit. 2011. aasta ülitugeva maavärina ajal olid neist kolm erinevatel põhjustel suletud. Kolm töötavat reaktorit lülitusid maavärina peale automaatselt välja, nagu Jaapani seadused nõuavad. SCRAM-i alustamisega samal ajal käivitusid avariigeneraatorid, varustamaks energiaga juhtimisseadmeid ja jahutussüsteeme. Sarnase varugeneraatorite süsteemi katsetamine toimus ühel õnnetul ööl umbes 25 aastat varem Tšernobõlis. Fukushima jaamas läks kõik plaanipäraselt, kuni maavärina tekitatud hiidlaine 50 minuti pärast rannikule jõudis. Elektrijaam oli kaitstud 5,7-meetrise veetõusu eest, aga seekordne tsunami tõusis ligi 14 meetri kõrgusele. Elektrivarustus katkes, peaaegu kõik diiselgeneraatorid jäid seisma, kütusepaagid uhuti minema, elektrooniliselt juhitav ülerõhu kontroll lülitus välja. Osa seadmetest jäi siiski töökorda. Jahutussüsteemis oli võimalik kasutada aurupumpi ja lülitada elektroonikat patareitoitele. Hiljem on selgunud, et pingelistes oludes ei jätkunud jaama töötajatel piisavalt tähelepanu kõigi oluliste kohtade jaoks. Vaja oli korraga tegeleda nii elektrivarustuse taastamise, reaktorite jahutamise kui ka kasutatud kütusevarraste jahutusbasseinidega. Probleemid hakkasid kuhjuma ja kui akutoitel lisapumbad seisma jäid, tõusis temperatuur nii kõrgele, et kütusevarraste tsirkooniumkate reageeris kuuma veega ning tekkinud vesinik plahvatas mitmes kohas.
Õnnetusjuhtumi tulemusena pääses keskkonda suur kogus radioaktiivseid aineid, mille täpne kogus ei ole teada. 2013. aasta lõpuks ei ole selge, millal radioaktiivse vee leke Vaiksesse ookeani lõpeb. Juhtumi uurimine tuletas meelde mitmeid Fukushimaga seotud muresid varasemast ajast. Päevavalgele tuli fakte 60-ndate ja 70-ndate aastate turvalisuse kontrolliga seotud dokumentide võltsimisest. Selgus, et jahutussüsteemi katsetamistes oli vahet peetud 11 ja mõnes kohas isegi 40 aastat. 2008. aastal nõuti kontrolli tulemusena kohest tsunamitõkke täiustamist, arvestades veetaseme tõusuga 10,2 meetrit. Kompanii juhtkond ei pidanud soovitust tõsiseks, sest nii kõrge laine tundus ebareaalne.
Seekord reageeris maailm tuumaõnnetusele üsna tagasihoidliku protestiga, aga siiski võeti valitsuste tasandil vastu otsuseid vähendada tuumaenergeetika osatähtsust. Saksamaal on otsustatud kõik tuumajaamad sulgeda aastaks 2022. Itaalias, Šveitsis ja Belgias on toimunud referendumid, väga suur protsent elanikkonnast pooldab tuumaenergeetikast loobumist. Prantsusmaal on otsustatud töötavate jaamade arvu oluliselt vähendada. Mitmetes Aasia riikides on uute jaamade projekteerimine lõpetatud.
Itaalia füüsik Enrico Fermi oli samavõrra tugev nii teoreetiku kui eksperimentaatorina. Tema juhtimisel tehti rida ahelreaktsiooni uurimise katseid, arvutati ja planeeriti esimene töötav tuumareaktor.
Fermi oli pärit Roomast. Ta asus pärast kooli lõpetamist õppima Pisa ülikooli, lõpetas selle hiilgavalt, reisis Euroopas, kus kohtus paljude oma aja füüsikateoreetikutega. Juba 24-aastaselt sai ta Sapienza ülikooli professoriks Roomas. See oli üks esimesi teoreetilise füüsika professuure Itaalias. Fermi juhitud noorte teadlaste rühm sai peagi kuulsaks kui Via Panisperna poisid. Need poisid avastasidki aeglaste neutronite toime, avastus, mis viis lõpuks tuumareaktorite ja aatompommide ehitamiseni.
1938. aastal otsustas diktaator Mussolini Hitleri Saksamaad järgides alustada juudivastase kampaaniaga. Fermi oli Mussolini juures heas kirjas, ta nimetati teaduste akadeemia liikmeks ja kuulus isegi parteisse. Fermi ei olnud juut, aga tema naine oli ja see tegi kogu perekonna elu Roomas keeruliseks. Samal aastal sai ta Nobeli preemia uute, neutronkiirguse toimel tekkivate elementide ja aeglaste neutronite toimel toimuvate tuumareaktsioonide avastamise eest. Pärast preemia kättesaamist Stockholmis sõitis Fermi kohe koos perega Ameerika Ühendriikidesse. Ta oli juba varem salajase kirjavahetusega otsinud töökohta Ameerikas ja valis nüüd viiest pakkumisest Kolumbia ülikooli. Sel ajal oli ta ilmselt neutronite alal maailma parim spetsialist ja seepärast oli väikeseks pettumuseks, et uraani tuumade lagunemise tõestus ja seletus tuli hoopis Saksamaalt. Teise maailmasõja ajal ei olnud itaallastel Ameerikas kuigi kerge, aga Fermi isikuomadused ja eriline anne võimaldasid tal ometi kaasa lüüa olulistes teadusprojektides. 1944. aastal sai ta USA kodakondsuse.
Fermi oli arvatavasti esimene teadlane, kes juhtis tähelepanu Einsteini valemis E = mc2 peituvale tuumade siseenergia vihjele. 1923. aastal kirjutas ta: „Vähemalt lähemas tulevikus ei tundu võimalik, et leitakse tee selle kohutava energiakoguse vabastamiseks ja nii ongi hea. Selle hirmuäratava energiaga plahvatuse esimene tulemus oleks teha pihuks ja põrmuks füüsik, kellel on piisavalt ebaõnne see tee leida.”
2. detsembril 1942. aastal oli Fermi juhitud töörühm Chicago ülikooli vana staadioni tribüünialuses ruumis valmis käivitama tuumareaktorit Chicago Pile-1. Reaktori kütus oli uraanitablettides, neutroneid aeglustas grafiit, kontrollvardad tehti kaadmiumist, indiumist ja hõbedast. Kogu seade meenutas puidust ja mustadest tellistest kuhjatud hunnikut (inglise keeles: pile - kuhi). Kiirguskaitset ja jahutust ei olnud. Reaktor pidi tulema umbes kerakujuline, aga Fermi arvutas ehituse ajal välja, et ahelreaktsiooni käivitamiseks pole vaja kogu materjali kokku laduda. Erakordne läbimõeldus, põhjalikkus ja piinlikult täpsed arvutused olid omased paljudele tema katsetele. See oli ka üheks põhjuseks, et reaktoriga julgeti katsetada rahvarohkes südalinnas. Iseeneslik ahelreaktsioon saavutati kell 15.25 ja reaktor töötas esimesel korral 28 minutit. Hiljem võeti kogu seade koost lahti ja viidi linnast välja. Praegu on see maetud koos mõne teise Manhattani projekti reaktori varemetega Red Gate Woodsi, Chicago linnalähedasse metsa.
Pärast sõja lõppu pöördus Fermi tagasi õppetöö ja teadusliku uurimise juurde. Ta tegeles osakestefüüsika ja kosmilise kiirgusega. Vesinikupommi projekti suhtes oli ta kriitiline, aga nagu paljud teadlased, osales selles siiski konsultandina, tehes mitmeid olulisi arvutusi.
Fermi suri 54. eluaastal pärast maovähi operatsiooni. Kahjuks ei jõudnud ta kirjutada planeeritud tuumafüüsika õpikut.
Prantsuse teadlane Henri Becquerel uuris 1896. aastal fosforestsentsi – mõnede ainete võimet pärast tugevat valgustamist ühevärviliselt helendada. Esialgu paistis, et uraanisoolad kiirgavad päikesekiirte mõjul lisaks valgusele ka röntgenikiiri, mis läbivad katses kasutatud tihedat musta paberit, aga metalli mitte. Peagi selgus, et valgustamine polegi vajalik, uraanisoolad kiirgavad täiesti iseenesest. Radioaktiivsuse uurimisele aitas tublisti kaasa uute, palju võimsamalt kiirgavate elementide avastamine. Marie ja Pierre Curie, eraldasid maakidest polooniumi ja raadiumi. Raadiumi kaudu kinnistus kogu nähtuse nimena radioaktiivsus.
Radioaktiivsus oli alguses teadlastele suur mõistatus, selle lahendamine on seotud Ernest Rutherfordi töödega. Juba aastatel 1898 kuni 1901 selgitas ta välja, et Becquereli kiired koosnevad mitmest erineva läbimisvõimega komponendist, mis said nimeks alfa- ja beetakiired. Elektri- ja magnetväljaga oli võimalik need kiirgused üksteisest eraldada ja siis sai kolmas komponent, millel laengut pole, nimeks gammakiirgus (joonis 2.9.1.). Samal ajal sai selgeks ka see, et gammakiired on sarnased röntgenikiirtega, st tegu on lühilainelise elektromagnetkiirgusega, suure energiaga kvantidega.
Alfalagunemise korral eraldub tuumast α-osake, heeliumi tuum
Tuumad ise muutuvad seeläbi teise elemendi tuumadeks, justkui nihkudes perioodtabelis kahe koha võrra ettepoole. Tekkinud tuuma massiarv on lähtetuuma omast nelja võrra väiksem. Uraan-238 on alfaradioaktiivne, lagunemisel eraldub -osake ja järele jääb tooriumi tuum, mis on samuti radioaktiivne ja laguneb edasi:
Tuumafüüsika ajaloos on -osakestel tähtis koht. Aatomituum avastati kulla aatomeid vaakumis -osakestega pommitades ja nende hajumist mõõtes (ptk Aatomituum). Rutherfordi hajumist kasutati hiljem palju tuumauuringutes. Esimesed avastused tuumareaktsioonide alal tehti samuti aineid -osakestega mõjutades.
Tuntud rakendustest on kõige laiema levikuga ionisatsioonikambriga suitsuandurid. Alfaradioaktiivne ainetükike ioniseerib pisikeses kambris gaasimolekule ja teeb võimalikuks sealt läbi lasta nõrka elektrivoolu. Kui kambrisse tungivad suitsuosakesed, muutub voolutugevus ja alarmsignaal rakendub.
Aatomimaailma mõõtudes on -osakesed üsna suured, suure massiga ja laetud, mispärast ei jõua nad radioaktiivsest preparaadist kuigi kaugele. Õhus levib alfakiirgus mõne sentimeetri, ei läbi õhukest metallikihti ega tungi läbi isegi paksemast paberist. Seepärast ei ohusta alfakiirgus organisme välispidiselt.
| Joonis 2.9.2. Suitsuanduri ionisatsioonikambrisse on peidetud pisike tükk alfaradioaktiivset ameeriitsium(IV)oksiidi. Kiirgusohtu ei ole, kuni kamber on terve, sest α-osakesed ei läbi metalli ega levi ka õhus kuigi kaugele. | Joonis 2.9.3. Satelliitide elektrivarustuse jaoks plutoonium(IV)oksiidist (238Pu02) pressitud silindri paneb punaselt hõõguma radioaktiivsel lagunemisel vabanev energia. |
Kõige levinum tuumaenergia elektrienergiaks muundamine käib tuumajaamades soojusenergia ja vee keetmise kaudu (ptk Tuumaenergeetika). Radioaktiivsel lagunemisel vabanevat energiat saab elektrienergiaks muuta veel mitmel moel. Üks enamkasutatud lahendusi on termoelektriline radioisotooppatarei. Vooluallikaks on neis seadmetes termopaarid. Pinge saavutatakse temperatuurierinevusega, mis paneb laengukandjad liikuma kuumalt poolelt külmale. Kõrge temperatuur saadakse erinevatest, eelistatult -radioaktiivsetest ainetest. Kõige enam on kasutatud plutoonium-238 (joonis 2.9.3.), aga ka strontsiumi, polooniumi, küüriumi ja ameriitsiumi isotoobid on kasutust leidnud. Termoelekrilised radioisotooppatareid teenivad kohtades, kus patareid peavad kaua vastu pidama ja hooldamine või vahetamine on keeruline, kallis või võimatu. Seepärast kasutatakse neid satelliitidel, automaatsetes polaaralade vaatlusjaamades või tuletornides. Mõnda aega paigutati neid isegi südamestimulaatoritesse.
Beetalagunemisel eraldub tuumast suure kiirusega -osake. Henry Becquerel tegi juba 1900. aastal kindlaks -osakese massi ja laengu suhte, mis näitas, et tegemist on elektroniga (). Kuna tuumas ei ole elektrone, mis saaksid sealt väljuda, siis peavad elektronid tekkima. Ebastabiilsed tuumad lähevad iseenesest vähema energiaga seisundisse, misjuures muutub üks neutron prootoniks. Täpsemalt, üks d-kvark muutub u-kvargiks:
ehk
Lisaks sellele tekib igal lagunemisel üks antielektronneutriino. Selles protsessis massiarv ei muutu, küll aga muutub ühe võrra suuremaks laenguarv ja -lagunemisel tekkinud tuum on perioodtabelis lähtetuumast järgmine.
Tuumast eralduvate -osakese energiad on erinevad. Kiirus võib ulatuda üle 270 000 km/s, st beetakiirguse energia on väga suur. Õhus jõuab β-osake mõne meetri kaugusele, tungib rakkudesse või läbib õhukese alumiiniumlehe, aga ei läbi raskeid metalle ega kiviseinu. Kui -osakese kiirus on aineosakestega kohtumise tõttu vähenenud, siis on ta täiesti tavaline elektron. Kahjuks jõuab ta kiirust kaotades ioniseerida molekule ja lõhkuda keemilisi sidemeid, millest tuleb beetakiirguse ohtlikkus elusolendeile.
Beetalagunemisel tekivad koos kiirete elektronidega ka neutriinod, mille jälile jõutigi -osakeste energia mõõtmisel. Beetalagunemise esialgsetes teooriates tekkisid probleemid energia jäävuse ja spinniga, kalduti isegi arvama, et energia jäävuse seadus ei pruugi osakeste maailmas kehtida. 1930. aastal kirjutas Austria füüsikateoreetik Wolfgang Pauli kolleegidele kirja, kus esitas beetalagunemise uue teooria ja kutsus üles planeerima eksperimente selle tõestuseks. Teooria eeldas, et elektroniga koos tekib veel üks väga kerge laenguta osake, mille ta nimetas neutroniks. 1932. aastal avastas James Chadwick eksperimentaalselt neutraalse tuumaosakese, mille nimetas ka neutroniks. Kahe samanimelise osakese eksitava vea parandas Enrico Fermi, kui ta, võttes Pauli kerge osakese oma beetalagunemise teooriasse, nimetas selle neutriinoks. Itaalia keeles on neutron neutrone (suur neutraalne asi) ja neutrino on pisike neutron, neutronike. Veidi utreerides võib öelda, et neutriinoteooria päästis energia jäävuse seaduse.
Pauli tellis oma kirjas „headelt radioaktiivsetelt daamidelt ja härradelt” neutriinode avastamise eksperimendi, mis tegelikult sai teoks alles paarkümmned aastat hiljem. 1956. aastal tõestasid Clyde L. Cowan ja Frederick Reines katseliselt neutriinode olemasolu. Katsed tegi ja teeb keeruliseks see, et neutriinod on laenguta, ja peaaegu massita. Elektromagnetjõudu nad ei tunne ja aineosakestega on vastastikmõjus ainult väikese mõjuraadiusega nõrga tuumajõu kaudu. See tähendab, et neutriinod lähevad peaaegu puutumatult läbi igasugusest ainest. On välja arvutatud, et Päikesel toimuva tuumasünteesi tõttu läbib Maal iga päikesekiirguse poole suunatud ruutsentimeetrit umbes 70 miljardit neutriinot sekundis. Aatomituumadega kohtuvad neist väga üksikud. Cowan ja Reines katsetasid tuumareaktorite juures, kust saadi ruutsentimeetrile umbes 50 triljonit antielektronneutriinot sekundis. 200-liitristes veemahutites, mis olid kosmilise kiirguse mõju vähendamiseks sügaval maa all, kohtusid neutriinod vee koostises olevate prootonitega. Tekivad neutron ja positron (antielektron):
Positron kohtub kohe mõne elektroniga ja annihileerub, andes kaks -kvanti. Saamaks kindlalt äratuntavat signaali, oli vees lahustatud kaadmiumkloriidi. Kaadmiumi tuumad neelavad neutroni, tekib ergastatud tuum, mis kiirgab viie mikrosekundi pärast ühe -kvandi:
Just neist kvantidest pärinevate väikeste valgussähvatuste järgi (kaks korraga ja üks hilinemisega) tunti neutriinod ära. Kuude kaupa andmeid kogudes tehti kindlaks, et keskmiselt neeldub seadmes kolm neutriinot tunnis. Täiendavaks kontrolliks peatati reaktsioon tuumareaktoris, neutriinode neeldumine vähenes, nagu oli ennustatud. 1995. aasta Nobeli füüsikapreemia üks osa anti Frederick Reinesile neutriino katselise avastamise eest, Clyde L. Cowan suri juba 1974. aastal.
Kui selgus, et neutriino kohtumist tuumaosakesega on võimalik registreerida, hakati sobivaid seadmeid ehitama ja arendama terves maailmas. Neutriinoteleskoopideks ja neutriinoobservatooriumiteks nimetatud seadmed on oma mõõtudelt ja tehnoloogialt üsna muljetavaldavad.
Neutriinod on ka edaspidi püsinud teaduslike probleemide esirinnas. 1960-ndatel avastati mitmes katses, et Päikeselt maale saabuvaid elektronneutriinosid on umbes kolmandik sellest, mida ennustasid Päikese toimimist kirjeldavad matemaatilised mudelid. Kahtlustati vigu mudelis ja isegi tundmatuid muutusi Päikese termotuumareaktsioonis. Tõenäolisem paistis siiski mingi neutriinodega seotud põhjus. Neutriinosid on kolme sorti: elektronneutriinod, müüneutriinod ja tauneutriinod. 2001. aastaks tõestati veenvalt, et neutriinod ostsilleeruvad ühest tüübist teise. Umbes 35% Päikeselt saabuvaist neutriinodest on elektronneutriinod. Algul määrati ainult neid. Ülejäänud on müü- või tauneutriinod. Koguarv klapib üsna hästi Päikese teoreetilise mudeliga. Veel järeldub neutriinode ostsillatsioonist, et nad pole seisumassita, alluvad tõrjutusprintsiibile ja ei liigu valguse kiirusega. Sedasama väitis Wolfgang Pauli juba 1930. aastal, kui ta uut osakest esimest korda nimetas. 2013. aastaks on neutriinode massid siiski määramata. On teada piir, millest mass on väiksem ja et see pole null.
2011. aasta septembris avaldas Itaalia Gran Sasso laboratooriumi ja CERNi koostööprojekt OPERA teate, et nende andmed viitavad neutriinode liikumisele valgusest kiiremini. Tegu oli pigem üleskutsega leida viga, sest ka OPERA teadlased ise ei uskunud tegelikku „kosmilise kiiruspiirangu ületamist”. Uudis levis kiiresti, jõudis ajalehtede esikülgedele ja pakkus huvi kõige laiemale publikule. Tekkis ja taaselustus mitmeid teooriaid, mõned neist üsna fantastilised. 2012. aasta juulis tehti teatavaks, et viga on leitud, st neutriinod ei ületa absoluutkiirust. Kui olla päris täpne, siis algsed andmed paistsid näitavat, et neutriinod jõuavad umbes 730-kilomeetrisel teel läbi mägede kohale 60,7 ±6,9(A) ±7,4(B) nanosekundit varem, kui valgus oleks sama tee läbinud vaakumis. Parandatud andmetel jõuavad neutriinod varem 6,5 ±7,4(A) (+8,3)(-8,0)(B) nanosekundit. Mõõtemääramatus on üle kahe korra mõõtmistulemusest suurem, aga küllap võib neutriinodel üllatusi varuks olla.
Radioaktiivsuse uurimise algusaastatel eraldati kiirgusliigid ( ja ) eelkõige läbimisvõime järgi. Aastatel 1899 kuni 1903 tehti radioaktiivsuse uurimisel suuri edusamme ja selgus, et on olemas veel üks põhimõtteliselt erinev, väga suure läbimisvõimega kiirgusliik. Rutherford, kes oli nimetanud eelmised ja näidanud, et sel uuel kiirgusel pole laengut, nimetas selle -kiirguseks. Kui kümne aasta pärast selgus, et -kiired peegelduvad kristallidelt, määrati lainepikkus ja sai selgeks, et tegu on röntgenikiirgusega sarnase, aga suurema sageduse ja suurema kvandi energiaga elektromagnetlainega.
Piir röntgenikiirguse ja -kiirguse vahel on kokkuleppeline ja lähtub enamasti kvandi energiast, mis peaks olema vähemalt 100 keV (sagedus 1019 Hz, lainepikkus 10 pikomeetrit, suurusjärgulise täpsusega). See kokkulepe ei ole väga kindel. Tihti nimetatakse -kvantideks või -footoniteks ka väiksema sagedusega kiirgust, kui see pärineb radioaktiivsusest. Kui kiirgus pärineb aatomi elektronkattest, mitte tuumast, nimetatakse seda röntgenikiirguseks, kuigi kvandi energia võib olla kokkuleppelisest piirist suurem. Maapealseks -kiirguse allikaks on põhiliselt radioaktiivsus. Mõnel juhul tekivad gammasähvatused ägedates äikesetormides, selle protsessi mehhanism ei ole täpsemalt teada. Kosmiline ruum saadab meile samuti mitmesuguse päritolu ja energiaga -kiirgust.
Suur kvandi energia ja hea ainest läbitungimise võime annavad mitmeid võimalusi γ-kiirguse praktiliseks rakendamiseks. On välja töötatud palju meetodeid materjalide ja esemete „läbivalgustamiseks” -kiirtega. Ameerika Ühendriikides on alates 2002. aastast üha enam rakendatud kaubakonteinerite automaatset kontrolli -kiirgusseadmete abil. -kiirgus on laialt levinud meditsiiniseadmete ja -materjalide steriliseerimiseks autoklaavimise asemel.
Vaatamata sellele, et kiirgus on inimeste tervisele mitmes mõttes ohtlik, kasutatakse -kiiri kasvajarakkude hävitamiseks. Tuntuim meditsiiniseadmete gammaallikas on Co-60. Beetalagunemisel annab selle tuum ühe -kvandi. Tekkinud Ni-60 tuum on ergastatud ja kiirgab põhiolekusse üleminekul ühe veelgi suurema energiaga -kvandi:
Radioaktiivne lagunemine on tõenäosuslik protsess (ptk Elektronide difraktsioon ja ptk Määramtusseos). Ei saa kuidagi määrata, millal laguneb konkreetne tuum või millise aatomi tuum järgmisena laguneb. Küll aga on kõigile radioaktiivsetele isotoopidele määratud poolestusaeg (). Selle aja jooksul lagunevad pooled olemasolevatest tuumadest. Algsest radioaktiivsete aatomite hulgast jääb aja möödudes alles aatomit:
on algne radioaktiivsete aatomite arv, on poolestusaeg, on kulunud aeg ja aja pärast allesjäänud osakeste arv.
Näiteks uraani looduslike isotoopide poolestusajad on:
- uraan-234, 2,45·105 aastat;
- uraan-235, 7,04·108 aastat;
- uraan-238, 4,46·109 aastat.
Uraani poolestusaeg on väga pikk. Mitmetel radioaktiivse lagunemise produktidel on see üsna lühike. Näiteks jood-131, mis tekib tuumaplahvatustel ja –reaktorites ja mille poolestusaeg on 8 päeva. Tšernobõli katastroofi järel oli radioaktiivne jood saastunud aladel viibijaile eriti ohtlik esimestel nädalatel, hiljem selle kontsentratsioon langes kiiresti. Eriti kiiresti lagunevad perioodtabeli viimases reas asuvate uute elementide tuumad. Livermooriumi, mis on tabelis 116 kohal, kõigi isotoopide poolestusaegu mõõdetakse millisekundites. Kõige stabiilsemal neist, Lv-294 on poolestusaeg 53 ms.
α- ja β-lagunemisel tekkivad uued tuumad, mille asetust perioodtabelis võrreldes lähtetuumaga kirjeldab nihkereegel:
- α-lagunemisel muutub laenguarv kahe võrra väiksemaks ja massiarv nelja võrra väiksemaks. Tuum nihkub perioodtabelis kahe koha võrra ettepoole.
- β-lagunemisel suureneb tuuma laenguarv ühe võrra, massiarv ei muutu ja tuum nihkub perioodtabelis ühe koha võrra tahapoole.
Tihti on tekkinud uued isotoobid samuti radioaktiivsed ja lagunevad edasi. Nii moodustub lagunemiste seeria, mis viib lõpuks välja mõne stabiilse isotoobi tekkimiseni (joonis 2.9.7.). Paljud lagunemisseeriad annavad võimalusi kivimite vanuse määramiseks. Üks vanemaid ja paremini läbitöötatud meetodeid põhineb kahes lagunemisseerias tekkinud plii-isotoopide koguse määramisel. Uraani-raadiumi seerias muutub uraan-238 stabiilseks isotoobiks plii-206. Uraani-aktiiniumi seerias muutub uraan-235 stabiilseks isotoobiks plii-207. Mõnedes mineraalides, näiteks tsirkoonis (ZrSiO4), esineb teatud määral uraani isotoope, aga tekkimise ajal ei saanud seal kindlasti olla pliid. Tähendab, et kogu analüüsil leitud plii on tekkinud kahe nimetatud lagunemisseeria kaudu. Teades radioaktiivse lagunemise seadust ja tundes kõik vaheetappe (poolestusaegu), on võimalik kivimi tekkimise aeg välja arvutada. Dateerimine uraani ja plii kaudu kõlbab kivimitele, mille vanus on üks miljon kuni 4,5 miljardit aastat. Selle tänapäevaseks täpsuseks loetakse 0,1-1%. Meetodit on arendatud alates Rutherfordi esimestest töödest sel alal 1905. aastal ja praegu on see põhiline viis kivimite vanuse määramiseks. Muu hulgas on nii määratud ka Maa vanus.
Looduslik süsinik koosneb kahest stabiilsest isotoobist (ptk Isotoobid), (98,9%) ja (1,1%). Õhu süsihappegaasis on lisaks stabiilsetele süsiniku isotoopidele väga väike kogus (umbes triljondik) radioaktiivset süsiniku isotoopi , mida nimetatakse ka C-14, süsinik-14 ja radiosüsinik. Põhiline radiosüsiniku allikas on kosmiline kiirgus. Ülisuure energiaga prootonid ja muud aatomituumad tungivad kosmosest atmosfääri ja kohtudes õhu molekulidega, tekitavad laviinina uusi osakesi. Muu hulgas tekib neutroneid, mis võivad lämmastiku muuta radioaktiivseks süsiniku isotoobiks (C-14). Tekkinud süsinik reageerib kiiresti õhuhapnikuga. Moodustunud süsihappegaas levib ühtlaselt atmosfääris ja lahustub veekogudes:
Radioaktiivne süsinik laguneb pidevalt, muutudes taas stabiilseks lämmastiku isotoobiks ja eraldades -osakesi:
Samas selle kontsentratsioon atmosfääri ülakihtides püsib muutumatuna, sest kosmilised osakesed tekitavad radiosüsinikku juurde. Kõigi süsinikuringes osalevate organismide rakkude süsinik koosneb neist samadest isotoopidest, millest õhu süsihappegaas, sest sellest algab kogu toiduahel. Nii saab ka C-14 rakkude koostisse. Surnud orgaaniline aine keskkonnaga enam süsinikku ei vaheta. Radioaktiivne süsinikuisotoop laguneb tasapisi ja selle sisaldus väheneb järjest. Teades radioaktiivse lagunemise seadust, on võimalik allesjäänud C-14 hulga järgi arvutada, kui ammu on uuritav orgaaniline aine lõpetanud süsiniku omastamise. Mida vähem on proovi jäänud radioaktiivset süsinikku, seda vähem kiirgub sellest -osakesi ja seda vanema orgaanilise ainega on tegu.
| Joonis 2.9.8. 1949. aastal saatis Willard Libby arheoloogidele, kes temaga varem koostööd olid teinud, esimese teoreetilise lagunemiskõvera võrdluse teadaoleva vanusega proovide analüüsiandmetega. Kahe aasta pärast ilmus tema raamat „Dateerimine radiosüsiniku järgi”, sellest alates on radiosüsiniku aastate skaalat üha täpsemalt kalibreeritud ja ka meetod on palju täienenud. C-14 poolestusajaks loetakse tänapäeval 5730±40 aastat. 1960. aastal sai Libby Nobeli keemiapreemia. |
Radiosüsiniku meetodi töötas 1949. aastaks välja Willard Libby juhitud töörühm Chicago ülikoolis. Uus meetod põhjustas murrangu arheoloogias. Muudest allikatest määratud leidude vanused klappisid päris hästi radiosüsiniku abil määratutega (joonis 2.9.8.) ja meetod levis kiiresti. Orgaanilist päritolu leidude vanus määratakse radiosüsiniku aastates enne tänapäeva. Tänapäevaks loetakse kokkuleppeliselt aastat 1950, sest just siis rikkusid õhus tehtud tuumakatsetused C-14 tasakaalu. Nii määratud aastaid ei saa päriselt kalendriaastatena võtta. Põhjuseid on mitu. Süsihappegaas ei jaotu atmosfääris ega lahustu ookeanides päris ühtlaselt. Vulkaanipursked ja inimtegevus segavad aeg-ajalt õhku kivimitest või väga vanast orgaanikast pärinevat süsihappegaasi, mis radiosüsinikku ei sisalda. Atmosfääri koostise ja Maa magnetvälja muutused nihutavad paigast C-14/C-12 tasakaalu, st kunagi võis organismidesse ladestuda hoopis teistsugune kogus radiosüsinikku. Arvutatud radiosüsiniku aastaid korrigeeritakse nii palju kui võimalik kalibreerimisega ja arvutatakse seekaudu kalendriaastatesse. Selleks kasutatakse muudest allikatest teadaoleva vanusega proove. Lähemas ajaloos sobivad kirjalikud allikad, vanematel aegadel tulevad appi puidu aastarõngad ja koobastes esinevad lubjakivimoodustised. Radiosüsiniku meetod ei vii meid kaugemale ajalukku kui umbes 50 000 aastat. Selle ajaga on C-14 juba nii palju vähenenud, et määramine osutub praktiliselt võimatuks.
Radioaktiivsus avastati ja seda uuriti aastaid looduslikel radioaktiivsetel isotoopidel. Kunstliku radioaktiivsuse avastamise ja uute radioaktiivsete isotoopide sünteesimise eest pälvisid 1935. aastal Nobeli keemiapreemia Frederic ja Irene Joliot-Curie. Nad pommitasid polooniumist pärinevate α-osakestega mitmeid kergemaid elemente ja said uusi radioaktiivseid aineid. Näiteks alumiinium muutus fosfori isotoobiks massiarvuga 30, mida looduses ei esine. Seda kiiresti lagunevat uut ainet kutsuti radiofosforiks. Paljusid tänapäeval tuntud ja kasutatavaid isotoope looduses ei esine ja neid toodetakse. Meditsiinis tarvitatav Co-60 on samuti kunstlik isotoop, mis tekib Co-59 neutronaktivatsiooni teel.
Uute isotoopidega asi ei piirdu, praeguseks on sünteesitud pikk rida uusi elemente. Perioodtabeli viimane looduslik element on uraan, laenguarv 92. Kõik järgmised ruudud, mida nimetatakse transuraanideks, on täidetud kunstlike elementidega. 1936. aastal täideti lõpuks perioodtabeli 43. ruut sünteetilise tehneetsiumiga. Puuduvat elementi oli sinna otsitud alates tabeli loomisest. Tehneetsium on kergeim element, millel ei ole ühtegi stabiilset isotoopi. Tc-90 hulk maakides on nii väike, et seda ei ole peaaegu võimalik ja muidugi mitte kasulik loodusest toota. Transuraanide sünteesimine oli 20. sajandi keskel mõnda aega teaduslaborite ja suurriikide teadusliku võidujooksu teema. Viimased sünteesitud elemendid on äärmiselt ebastabiilsed, poolestusaegu arvestatakse millisekundites. Teoreetilised mudelid viitavad sellele, et mõned veelgi suuremad tuumad (järjenumbritega üle 120) võiksid olla veidi püsivamad ja moodustada tabelis nn stabiilse saare. Nende poolestusajad arvatakse tulevat üle minuti, mõne teooria järgi isegi aastaid.
Radioaktiivse kiirguse ja röntgenikiirguse otsene ohtlikkus elusorganismidele oli teada peaaegu avastamisest saadik. Geneetiline oht ja kantserogeensus said üldiselt teatavaks 1930-ndate aastate jooksul. Kaasaegse teaduse sajand on lisanud radiatsiooniohtude kohta rohkelt andmeid. Tuumakatsetused, kaks sõjalist tuumaplahvatust, õnnetusjuhtumid tuumajaamades ja ohtlike jäätmete hoidlates, kiirgusseadmetega töötamine - radioaktiivsus on saanud igapäevaseks ja samas muutnud meid ettevaatlikuks. Kiirgust on õpitud mõõtma ja kiirgusallikaid tundma.
Inimesed elavad tegelikult pidevas kiirgusvoos. Elektromagnetlainetest ohustavad meid eelkõige röntgenikiired ja -kiired. Siiski tuntakse tänapäeval ka UV-kiirgusega seotud ohte ja uuritakse hoolega, kas mobiilsides kasutatav raadiolaine ei või olla ohtlik pikaajalise toime korral ja näiteks lastele. Teame ka ohtlikke osakestevooge: - ja -osakesed ning neutronid.
Ohtlikke kiirgusliike, mis võivad otseselt surmata rakke, tekitada neis kahjustusi või muuta DNA-d, nimetatakse ioniseerivateks kiirgusteks. Ioniseeriva kiirguse dooside mõõtmiseks kasutatakse spetsiaalseid SI kiirgusühikuid:
Materjalides või kudedes neeldunud kiirgusdoosi ühik on grei (Gy). Doos on üks grei, kui ühes kilogrammis neeldub üks džaul kiirgusenergiat:
Grei on ühik, mis ei võta arvesse kiirgusliikide erinevat mõju ja seda, milliseid organeid kiirgus mõjutab. Ameerika ühendriikides kasutatakse neeldunud doosi ühikut rad. 1 rad= 0,01 Gy.
Kiirguse mõju organismile kirjeldab paremini ekvivalentdoos, mille ühik on siivert (Sv). Ka siivert väljendab ühes kilogrammis neeldunud energiat džaulides, aga seda korrigeeritakse faktoriga Wr, mis arvestab kiirguse liikide eripära ja muid üksikasju. Ameerikas kasutatakse selle analoogi rem. 1 rem=0,01 Sv.
Mitmetest allikatest pärineb looduslik ja tänapäeval ka osaliselt kunstlik kiirgusfoon (joonis 2.9.9.). Elusolendid on tavalise kiirgusfooniga kohanenud, ohtlikuks saab see siis, kui mingi allikas annab ebatavaliselt suuri kiirgusdoose. Inimeste keskmine ekvivalentdoos looduslikest allikatest on 2,2 mSv aastas. Sellele lisandub umbes 20% kunstlikest allikatest, peamiselt meditsiiniuuringutest. Rahvusvahelised normid määravad, kui suur doos tohib kutsetööst või kohalikest tingimustest lisanduda keskmisele kiirgusfoonile. Näiteks täiskasvanud inimese kogu keha maksimaalne lubatud ekvivalentdoos töökohal ei toi ületada 100 mSv viie järjestikuse aasta jooksul või 50 mSv aastas. Surmavaks ühekordseks kiirgusdoosiks loetakse 3-5 Sv, kiiritushaiguse tekib 1-3 Sv.
Madame Curie, nagu teda tundis teaduskogukond, Marie Skłodowska-Curie, nagu ta ise oma nime kirjutas, oli Poola teadlane, kes töötas põhiliselt Prantsusmaal.
Maria Salomea Skłodowska oli pärit Varssavist, mis kuulus sellel ajal Vene impeeriumi alade hulka. Õpetajate pere, kus Maria oli noorim laps, elas poliitilistel ja majanduslikel põhjustel üsna keerulistes tingimustes. Maria lõpetas siiski gümnaasiumi kuldmedaliga, töötas koduõpetajana, õppis ise raamatute ja kirjavahetuse abil, osales põrandaaluse rahvusliku ülikooli õppetöös ja katsetas keemialaboratooriumis. Poolas oli sel ajal naistele kõrgharidus peaaegu kättesaamatu ja teaduskraadini jõudmine täiesti välistatud. 1891. aastal sõitis Maria (Prantsusmaal Marie) vanema õe eeskujul ja toetusel Pariisi, kus ta kitsaste olude kiuste õppides ja õpetades jõudis kiiresti kahe teadusliku kraadini. Samal ajal kohtus ta Pierre Curie’ga. Neid lähendas ühine teadushuvi ja maailmavaateline kooskõla. Marie oli siiski kindel, et ta pöördub kodumaale tagasi. 1894. aastal sõitis ta Varssavisse, et kohtuda perega ja leida seal tööd. Pierre oli samuti valmis Poolasse sõitma, oli valmis isegi loobuma oma õppetööst Pariisis. Kahjuks ei olnud Poolas midagi muutunud, Krakowi ülikool keeldus naisteadlast tööle võtmast ja Marie pöördus Pierre’i kutsel Pariisi tagasi. 1895. aastal registreeriti nende ilmalik abielu ja neist sai üks maailmakuulsamaid teadusperekondi. Tuntud teadlaseks kasvas ka nende 1897. aastal sündinud tütar Irène.
Pierre ja Marie Curie ühised teadushuvid keskendusid kiirgusele. Sajandivahetuse eel avastatud röntgenikiired ja radioaktiivsus pakkusid huvi paljudele teadlastele ja avastusi tuli ridamisi. Tugeva rahvusvahelise konkurentsi tingimustes avaldasid Curie’d mitukümmend teaduslikku artiklit nii koos kui ka eraldi. Paljud avastused tehti erinevates ülikoolides ja instituutides praktiliselt samal ajal ja kiire avaldamine hakkas muutuma üha tähtsamaks. Curie’d õppisid omavalmistatud seadmetega radiatsiooni mõõtma ja saanud aru, et uraanimaakides sisaldub teisigi radioaktiivseid elemente, eraldasid kahe uue elemendi ühendid. Elemendid nimetati polooniumiks ja raadiumiks. Hiljem õnnestus saada ka puhast metallilist raadiumi. 1903. aasta Nobeli preemia jagati erakordse panuse eest radiatsiooninähtuse uurimisse Pierre Curie, Marie Curie ja Henri Becquereli vahel. Marie on esimene naine, kes Nobeli preemia sai. Tegelikult lisati Marie nimi nominatsioonile Pierre’i otsese nõudmise peale hiljem.
Kuigi rahvusvaheline tunnustus oli suur, ei olnud töö Pariisis kuigi lihtne. Curie’del puudus korralik laboratoorium ja kuigi Pariisi ülikool oli lubanud sisustada sobivad ruumid, ei toimunud mitme aasta jooksul midagi. Stockholmi Nobeli preemiat vastu võtma jõudsid nad alles 1905. aastal. Põhjuseks toodi töökohustused, aga tegelikult sai üha selgemaks, et mõlema teadlase, eriti Pierre’i tervis on väga halb. Preemiaraha võimaldas neil esimest korda laborisse abilist palgata. Vahepeal sündis teine tütar, Ève. Marie jagas end teadustöö ja kodumurede vahel. Muu hulgas õpetas ta lastele poola keelt, saatis ja viis neid oma kodumaale igal võimalusel. Pidevaks probleemiks kujunesid Prantsuse ühiskonnas valitsevad meeleolud, see et Marie Curie oli välismaalane ja naine. Kui Curie’d Londonis Kuninglikku ühingut külastasid, esines ainult Pierre, naise ettekanne oleks olnud liiga järsk traditsioonide murdmine.
1906. aastal hukkus Pierre liiklusõnnetuses. Marie võttis vastu Pierre’i jaoks loodud füüsika õppetooli ja sai Pariisi ülikooli esimeseks naisprofessoriks. Lõpuks õnnestus tal luua korralik laboratoorium. Enamgi, Pariisi ülikooli ja Pasteuri instituudi koostöös sündis kuulus Raadiumi instituut, nüüdseks Curie instituut. Ometi ei valitud Marie Curie’d Prantsuse Teaduste Akadeemia liikmeks. Esimese naisena sai Prantsusmaal akadeemikuks üks tema doktorantidest alles 1962. aastal.
1911. aastal sai Marie Curie teise Nobeli preemia, seekord keemias, radioaktiivsete elementide avastamise ja nende ühendite ning omaduste uurimise eest. Isiklikus elus kujunes see aasta kohutavaks. Ajalehtede tormiliste süüdistuste hulka kuulusid juudi päritolule viitav neiupõlvenimi, Pierre’i teadussaavutuste enda nimele kirjutamine, romantilised suhted abielus kolleegiga, Prantsuse teadusmaine rikkumine jm. Paisuva ühiskondliku hüsteeria toel jõuti lausa isiklike rünnakuteni. Pärast Nobeli preemia vastuvõtmisel peetud kõnet ütles Marie tervis täiesti üles. Ta langes depressiooni ja viibis mõnda aega salastatud asukohaga haiglas. Veidi kosunud, veetis ta terve aasta Inglismaal hoolitseva sõbra juures, kes hoolega ajakirjanikke tõrjus. Laborisse ei pääsenud ta terve 1912. aasta jooksul. Samal ajal pakuti töökohta Varssavis, aga ta otsustas siiski pühenduda oma instituudile Pariisis. Kahjuks ei kestnud see pühendumine kaua, puhkes Esimene maailmasõda ja instituudi töö katkes pea täielikult 1919. aastani.
Sõja algul saatis Curie tütred Inglismaale ja asus ise õppima anatoomiat, radioloogiat ja automehaanikat. Eesmärk oli luua mobiilsed sõjaoludesse sobivad radioloogiaseadmed. Ta aitas sõjaväearstidel ehitada umbes 20 mobiilset röntgenaparaati ja paigaldada välihaiglatesse 200 radioloogiaseadet. Sõja ajal ei tegelenud ta teadustööga, aga kirjutas oma kogemustest sõjaolukorra radioloogiat käsitleva raamatu.
Pärast sõja lõppu töötas ta oma instituudis. Kuigi kuulsus ja kutsed paljudest ülikoolidest üldiselt häirisid ja pahandasid teda, reisis ta päris palju. Ameerikas sai koos tütardega reisiv Madame Curie väga populaarseks. Teisel Ameerika sõidul õnnestus tal hankida raadiumi Poolas asutatava instituudi jaoks. Varssavi Raadiumi instituut avati 1932. aastal. Seda asus juhtima Marie õde Bronisława, seesama, kelle juurde Pariisi ta sõitis 1891. aastal.
Marie Curie suri 66. eluaastal kiirgusest põhjustatud haigustesse. Selleks ajaks teati ioniseerivate kiirguste mõjust organismidele juba päris palju, kahju tervisele oli sündinud pikkade aastate jooksul, kui põnev uurimisteema kaalus üles alles aimatavad ohud. Tänapäeva arusaamade järgi töötati röntgenseadmete ja radioaktiivsete ainetega väga hooletult. Tema laboripäevikud ja isiklikud esemed on praegugi sel määral radioaktiivsed, et neid hoitakse arhiivis pliikattega karpides ja võetakse välja kaitseriietust kandes.
Raadiumühendeist helenduv värv oli 20. sajandi algul populaarne, nagu ka paljud muud raadiumi nimega kaubad. Esialgu ei aimanud ohtu keegi. Üks Rutherfordi kaastöötajatest avastas, et kui ta on pikemat aega radioaktiivsete ainetega töötanud, suudab ta pealehingamisega elektroskoobi maha laadida. See lõbustas ja rõõmustas laboris kõiki, sest tõestas radioaktiivsete gaaside olemasolu. Pierre ja Marie Curie kandsid uuritavaid preparaate taskus, hoidsid lauasahtlis ja öökapil. Raadiumi- ja röntgenikaupade populaarsuse haripunktis oli kiirguse toimest juba üht-teist teada. Oli juhuslikke avastusi, aga ka katsetulemusi ja päris selget statistikat.
Raadiumivärvidega töötanud naistest pöördus tervisekahjude hüvitamise nõudega kohtusse ainult viis. Paljud olid selleks ajaks surnud või lootusetult haiged. Siiski oli ka neid, kes töötasid ohtliku värviga lühemat aega ja nende tervis pidas kuidagi vastu, aga suure ettevõtte vastu kohut käia kardeti või peeti lootusetuks. Ajakirjanduse tähelepanu saatel kulgenud protsess näitas, et US Radium Corporation ei kavatsenud tõesti kergelt alla anda.
1928. aastal kaevati lahti 25. eluaastal surnud Amelia Maggia haud. Neli aastat oli ta raadiumvärviga kelladele helendavaid numbreid maalinud. Viimasel aastal jäi ta väga kõhnaks, väsis kiiresti ja liigesed valutasid. Ta kurtis arstidele, et liikudes tunneb end nagu väsinud vanainimene. Hambaarst avastas, et mitte ainul hambad ei lange välja, vaid ka lõualuu on muutunud pudedaks ja suu limaskest veritseb, väga palju surnud luukudet tuli eemaldada. 1923. aastal naine suri.
Hauast võetud luud puhastati ja töödeldi. Luudest lõigatud tükke ja pehmete kudede tuhka uuriti fotograafilisel meetodil, väga sarnaselt sellele, kuidas Henri Becquerel üle kolmekümne aasta varem radioaktiivsuse avastas. Röntgenipiltide tegemiseks kasutatav film pakiti musta paberisse. Proovid (ja võrdlusproovid laipadest, mis kuidagi ei saanud raadiumiga kokku puutuda) asetati paberile ja hoiti pimedas kümme päeva. Ilmutatud filmidelt oli näha, et mitu aastat tagasi lahkunud neiu luud on ikka veel tugevalt radioaktiivsed. See tõestas, et US Radium Corporationi juristide argumendid, nagu oleks raadiumimürgituse juhtum aegunud, mürgitamist enam ei toimu ja naised ei töötagi juba mitu aastat sel mürgisel tööl, ei pea vett. Raadium jääb organismi püsima ja kahjustab ohvrit seestpoolt pikki aastaid, isegi sadu aastaid. Raadiumi-226 poolestusaeg on 1600 aastat. Kohtuvaidluse ajal suri veel kolmteist raadiumvärviga töötanud naist ja ka kõigi elusolevate tervis halvenes järjest.
Raadiumitüdrukute kohtuasi lõppes kokkuleppega. Ettevõte soostus maksma kõigile tervisekahjude eest kompensatsiooni, määras iga-aastase toetuse ja lubas maksta kõik tervise- ja õiguskulud. Seda oli vähem kui raadiumivärvi ohvrid lootsid. Kuigi sellega ei olnud vaidlused ja kohtuasjad veel läbi, tuleb tunnistada, et teadusuuringud kiirguse biotoime alal said hoogu ja töötervishoid ning tööõigus muutusid tasapisi terves maailmas.
Radioaktiivsus
Radioaktiivsus on mõnede aatomituumade iseenesliku lagunemise protsess. Lagunemisel eralduvad α-oskesed (heeliumi aatomituumas) ja β-osakesed (kiired elektronid) ja algne tuum muutub teise elemendi tuumaks. Radioaktiivne lagunemine on tõenäosusliku iseloomuga, ü
Poolestusaeg
Radioaktiivse lagunemise kiirust iseloomustab poolestusaeg. Ühe poolestusajaga laguneb pool algsetest tuumadest. Järgmise poolestusajaga laguneb pool allesjäänutest, mitte allesjäänud pool.
Radiosüsiniku meetod materjalide vanuse määramiseks
Uurides looduslikes materjalides radioaktiivse lagunemise produktide sisaldust, saab teha järeldusi nende vanuse kohta. Näiteks uraani lagunemisel tekkivate plii isotoopide järgi võib arvutada kivimite moodustumise aega. Orgaaniliste materjalide (puidu, luude jm) vanust saab
Kiirguse mõju inimesele
Inimesed elavad pidevas kiirgusvoos, mis tuleb maakoorest, kosmosest ja tehismaterjalidest. Üks osa kiirgusest kannab ioniseeriva kiirguse nime. Ioniseeriva kiirguse toime tuleneb sellest, et kiirguskvandi või osakese energia on piisav aatomite ioniseerimiseks ja keemiliste sidemete l
Senegali legend, mille on meieni Uuest Maailmast toonud tänapäevane meediakeeris, räägib iidse loo.
Vanaisa leidis teelt Surnud Mehe. Ta kutsus kokku kõik loomad ja küsis, kes viib korraga üle jõe Kuu ja Surnud Mehe? Keegi ei julgenud lubada, aga lõpuks arvasid kilpkonnad, et nad võiksid kahekesi koos siiski proovida. Suur Kilpkonn võttis Kuu ja läkski sellega üle jõe. Väikesel Kilpkonnal olid aga käpad liiga lühikesed ja poolel teel libises Surnud Mees jõkke. Sellepärast on nii, et Kuu kaob ja tuleb jälle tagasi, aga Surnud Mees mitte kunagi.
Kuhu kaob Kuu ja millal ta jälle tagasi tuleb?
Ajaloolises vaatepunktis paistab vaatlejate looduskäsitluses tuhandeid aastaid laiunud ületamatu lõhe. Ühel pool makromaailma kehad, maapealsed nähtused, liikumised ja muutused. Teisel pool täiesti teistsugune maailm, mis paistab taevast, eriti see, mis paistab öisest taevast. Kuigi nende kahe seostamine oli raske, viisid vaatlemise kogemused ja andmete kogumine, matemaatika tugi ning tehniliste vahendite areng astronoomia kui teaduse väljakujunemiseni. Tänapäeva astronoomia uurib kosmilist ainet, taevakehi ja nende süsteeme.
Astronoomia on läbi aegade ausalt täheteaduse (kreeka keeles astron - täht) nime kandnud, aga nüüd on tal mitmeid kaasteadusi. Taevamehaanika kirjeldab matemaatiliselt üksikute kehade liikumist gravitatsiooniväljas. Astrofüüsika peab oma alaks kosmilise aine omadusi ja tähtedes toimuvaid protsesse. Kosmoloogia, kõige noorem, aga kõige vägevam vend, võtab kokku kogu Universumi toimimise, tekkimisest mõõtmatusse tulevikku.
| Joonis 3.1.1. Tartu Tähetorn on tüüpiline 19. sajandi linnaobservatoorium. Kõrgemale lagedale kohale rajatud vaatlustorniga hoones ja selle ümber asusid astronoomide töö- ning eluruumid. Pööratava ja avatava tornikupli all asub tavaliselt teleskoop. Tartus Toomemäel töötas peaaegu pooleteise sajandi jooksul mitmeid tuntud astronoome, kõige kuulsam neist Friedrich Georg Wilhelm Struve. Tema teadussaavutuste hulka kuuluvad esimene Vega kauguse määramine ja kaksiktähtede uue kataloogi koostamine. Struve juhitud Maa meridiaani mõõtmise geodeetiline alguspunkti asub tähetornis. Seetõttu kuulub Tartu Tähetorn 2005. aastast UNESCO maailma kultuuripärandi nimekirja. 200. sünnipäeva aastal avati põhjalikult renoveeritud Tähetorn uuesti muusemi ja külastuskeskusena. Tartu Observatooriumi teadlased töötavad juba alates 1960-ndatest Tõraveres. | Joonis 3.1.2. Galilei sai 1609. aastal teada, et torust ja kahest läätsest on võimalik valmistada „seade, mis näitab kaugel eemal asuvaid esemeid nii, nagu nad asuksid ligidal”. Kuigi ta ühtegi sellist näinud ei olnud, valmistas ta oma aja kohta väga hea teleskoobi ja avas teleskoobiastronoomia ajastu. Valmisosadest Galilei pikksilma kokkupanek on lihtne ja mänguline, tänapäeval pakutakse seda võimalust teaduse populariseerimise üritustel. Kui tahaks ka läätsed ise lihvida, nagu Galilei tegi, poleks ülesanne kaugeltki igaühele jõukohane. |
Astronoomia ajaloo kõige olulisemad murdepunktid on seotud vaatlusvahendite ja tehnika arenguga.
- Teleskoop leiutati 17. sajandi algul ja tõusis tänu Galileo Galilei 1609. aasta taevavaatlustele ning raamatule „Täheteataja” kohe tähtsaks vaatlusvahendiks.
- 19. sajandi esimesel poolel leiutati spektromeeter, kiireid edusamme tegi fotograafia. Tähevaatlustele lisandus tähevalguse analüüs. Spektraalriistad said teleskoopides tavaliseks. Tähtede ja muu kosmilise aine koostis hakkas selguma.
- 20. sajand laiendas vaatluseks sobiva kiirguse vahemikku. Nähtavas valguses vaatamise ja fotografeerimise kõrval arenesid uued teleskoobid. Alates 1930-ndatest võeti järk-järgult kasutusele kogu elektromagnetkiirguse spekter, raadiolainetest gammakiirguseni.(joonis 2.2.4.)
- 1950-ndate lõpus algas kosmoseajastu. Esimest korda paistis maailmaruum ilma paksu õhukihi segava toimeta. Kosmos oli käeulatuses ja astronoomia tegi esimese pisikese sammu puhtast vaatlemisest kosmosekatsete poole.
| Joonis 3.1.3. Esimene päikesevarjutus pärast spektraalanalüüsi meetodi väljatöötamist oli 1868. aastal. Selleks ajaks oli märgatud, et mitmed tumedad neeldumisjooned Päikese pidevspektris (Fraunhoferi jooned) sobivad tuntud elementide laboris saadud kiirgusspektrite joontega. Varjutuse ajal sai analüüsida Päikese ümber helenduvaid kromosfääri ja krooni gaase. Avastati uus erekollane spektrijoon, mida Maal tuntud elementidaga siduda ei saanud. Sel moel leitud aine sai nimeks heelium, kreeka päikesejumala Heliose järgi. 1999. aasta päikesevarjutuse ajal pildistatud Päikese kromosfääri joonspekter näitab vesiniku jooni (valge kriipsuga märgitud lainepikkused 656, 486, 434 ja 410 nm). Heeliumi kõige eredam joon on lainepikkusel 587 nm, kerge on leida ka lainepikkused 502 ja 447 nm. Nõrgemad jooned kuuluvad osaliselt muudele elementidele, mida on Päikese koostises vaid kaks protsenti. Nende hulgas on ka hästituntud naatriumi kollane joon lainepikkusel 589 nm, mis jääb heeliumiga võrreldes üsna varju, sest naatriumi on Päikesel väga vähe. | Joonis 3.1.4. Atmosfääri läbivad väga hästi raadiolained, mida saab vastu võtta raadioteleskoopidega. Raaditeleskoobid on astronoomide aparatuuri hulgas kõige suuremad, õieti on suured nende antennid. 1963. aastast töötab suurima ühes tükis antenniga Arecibo teleskoop Puerto Ricol, taldriku läbimõõt 300 m. Suuremat, 500-meetrist (FAST - Five-hundred-meter Aperture Spherical Telescope), ehitatakse Hiinas samuti maapinna looduslikku lohku, aga tehnoloogia on seal täiesti uus ja antenn ei töötagi ühe jäiga taldrikuna. Veelgi paremat vastuvõttu püütakse liitteleskoopidega, pannes arvutis kokku paljude väiksemate antennide signaalid. |
Inimesi on alati köitnud juhuslikud nähtused, milles ometi on või tundub olevat mingit korda. Usutavasti saab nende järgi tulevikku ennustada ja raskeid otsuseid langetada – mängukaartide pakist välja ladumine, täringute lauale viskamine, kohvipaksu valgumine tühjaksjoodud tassis jpm. Taevakehade näivad liikumised ilmakaarte suhtes, omavaheline asend, kõrgus horisondist mingil tähtsal ajahetkel on teatud määral juhuslik, mis juba mitutuhat aastat sünnitab lootusi ettearvamatu äraarvamiseks. Taevakehade asukohtade järgi otsuste ja ennustuste tegemise kunsti nimetatakse astroloogiaks.
Astronoomia ja astroloogia olid kuni 16. sajandini üks taevaste liikumiste kirjeldamise ja seletamise teadus. Kui taevamehaanika arenes üha täpsemaks ja jõudis taevaste liikumiste põhjuste küsimiseni, jäi astroloogia osaks tõlgenduste koostamise loominguline koorem. Astroloogia kasutab mõningast teaduslikku terminoloogiat, aga loodusteadusliku meetodiga sel seost ei ole.
Horoskoopide koostamine on tänapäeval lihtne, piisab kalendri ja kella tundmisest. Arvutiprogramm joonistab välja sodiaagiringi, jagab selle valitud süsteemi järgi majadeks, märgib taevakehade asendid ja arvutab nende asukohtade suhted (aspektid). Mõni astroloogiatarkvara võib ka lihtsas keeles tõlgenduse kokku panna, aga muidugi on põnevam jätta see töö astroloogi hooleks.
Horoskoobi võib koostada inimese sünnihetkele, aga ka kõigile teistele sündmustele, mida oluliseks peetakse: ettevõtte asutamine, esimene koolipäev, matemaatika eksam, teadusliku eksperimendi algus. Suure Hadronite Põrguti (CERN) esimene kiir tegi täisringi 27 km pikkuses vaakumtorus 10. septembril 2008 kell 10.28. Sellelegi sündmusele on horoskoop koostatud. Merkuur, Marss ja Veenus on Kaaludes.
Galileo Galilei lõi loodusteadusliku meetodi. Võib-olla on see veidi liialdatud, kindlasti ei saanud ta sellega hakkama eelkäijateta ja muidugi ei teinud ta üksi kõike lõpuni ära, aga tema osa teadusloos tõesti raske üle hinnata. Galilei tõi astronoomiasse teleskoobi. Selleks ajaks oli juba algeliste pikksilmadega Kuud vaadatud, aga järeldused ja avastused jäid Galilei teha. Palju abi oli tema kunstiandest ja -oskustest. Teleskoobivaatlused algasid 1609. aastal ja juba märtsis 1610 ilmus „Täheteataja” (Sidereus Nuncius).
- Raamat esitab erinevates faasides Kuu joonistusi. Galilei avastas, et Kuu valgustatud ja pimedat poolt eraldav joon (terminaator) ei ole sugugi sirge. Kuu tumedatel aladel on terminaator sirge, aga heledatel korrapäratult sakiline. Sellest järeldas ta, et heledad alad on mäed ja kraatrid, tumedad aga tasased mered.
- Jupiteri kaaslaste avastamine andis kindla märgi sellest, et kõigi taevaste liikumiste keskpunkt ei ole Maa ega isegi mitte Päike. Galilei jätkas Jupiteri kuude jälgimist ja määras nende perioodid.
- Teleskoobist paistab kordades rohkem tähti, kui tolleaegsed taevaatlased näitasid. Galilei täiendas tuntud tähtkujude jooniseid uute tähtedega, mida palja silmaga üldse nähe ei ole. Linnutees (ptk Galaktikad ja Universum), mida peeti taevaseks uduks, näitas teleskoop lugematu arvu tähti, mis silmaga vaadates ühte sulavad ja uduse vööna paistavad.
- Tähed ja planeedid paistavad taevas ühesuguste valgustäppidena, mõned eredamad, teised tuhmimad. Galilei märkas, et teleskoobiga vaadates paistavad planeedid pisikeste ketastena, tähed jäävad ikka valgustäppideks.
Galilei jätkas taevavaatlusi ja avastas, et Veenus ilmutab faase nagu Kuu ning Päikesel on plekid. Avastuste tulvas tuli ette ka keerulisi nähtusi, mille seletamine ei õnnestunud. Tänapäeval teame, et Kuu tasased alad ei ole mered. Saturn (ptk Päikesesüsteem) hämmastas Galileid mitmel korral. Saturni rõngad paistsid teleskoobis üsna uduselt ja Galilei oletas, et tegu on kolme keha süsteemiga. Hiljem, kui rõngad pöörasid Maa poole serviti, kadusid need vaateväljast hoopis, nagu oleks Saturn oma kaaslased neelanud. Et segadus oleks täielik, ilmusid need 1613. aastal uuesti välja. Galilei püüdis määrata tähtede läbimõõtu, teadmata, et teleskoobis paistvate täppide suurus on tingitud õhu ja teleskoobi enda omadustest.
Igapäevakeelt kõneldes ütleme, et taevas on pilved, sademed langevad taevast, lennukid, õhupallid ja linnud tõusevad taevasse. Astronoomide taevas on siiski palju kõrgemal, kuigi määramata kaugusega, on ta kindlasti väljaspool atmosfääri. See, mida me taevasse vaadates näeme ühtlase, öösel musta, päeval sinise, pinnana, on taevaskera. Võib öelda ka taevakera, taevasfäär, taevavõlv, taevalaotus, taevakuppel, taevakumm, taevatelk. Taevaskera on määramata raadiusega vaatlejat ümbritsev kerapind, millele projitseerub taevakehade näiv liikumine.
Päike tõuseb ja libiseb üle taeva, tehes suvel kõrgema, talvel madalama kaare. Noor Kuu tõuseb ja läheb Päikese järel, tihti märkame teda õhtuti pärast loojangut. Vana Kuu tõuseb enne Päikest ja läheb ka looja enne Päikest. Öösel, kui taevavõlv on must, säravad seal tähed. Tähed liiguvad kõik koos, jääb mulje, nagu oleks nad kinnitatud pöörleva taevaskera külge. Planeedid (varemalt rändtähed) liiguvad kinnistähtede hulgas. Palja silmaga on liikuvatest taevakehadest peale Kuu ja Päikese näha viis planeeti. Kaks neist, Merkuur ja Veenus, hoiduvad Päikese ligi ja neid tuleb tihti eha- või koiduvalgusest otsida. Marss, Jupiter ja Saturn võivad ka südaööl kõrgel taevas särada. Mõnel ööl „langevad tähed”, meteooride kosmiline kineetiline energia muutub atmosfääri sukeldumisel soojuseks ja valguseks
Tähtkujude nimetamine on nii vana tava, et selle algust ja juuri ei tea keegi. Arvatavasti algas kõik heledamatele tähtedele nimede panemisest. Küllap pandi nimed tähtsamate maapealsete kohtade, nähtuste, inimeste ja uskumuste järgi. Linnuteest sai taevane jõgi, tähed seal sees pidid olema kalad või paadid. Kahel pool Linnutee jõge elasid ja toimetasid inimesed või loomad. Algne pärimus kumab üsna veidi läbi hilisemast taevapildi kirjanduslikust, hariduslikust ja teaduslikust käsitlusest. Igal rahval ja maanurgal on olnud oma taevased nimed ja tähtkujud, mida on aastatuhandetega muudetud, segatud naabrite uskumustega ja praeguseks ka klassikalise kreeka-rooma mütoloogiaga. Taevalaotuse võiks kaasaegse täheteaduse huvides jagada lihtsalt ruutudeks, nii kui nii on kõigil kosmilistel vaatlusobjektidel koordinaadid juba kirjas. Tegelikult ei pruugi naabertähed ruumis üldse lähestikku olla, tähtkujusid moodustavad nende projektsioonid taevaskeral. Siiski säilitatakse taeva jagamist tähtkujudeks kui kultuuriajaloolist väärtust. Tähistaevas on vaatamist väärt ning legende on tore ikka ja jälle jutustada.
Taevaskera näiva ümber maailmatelje pöördumise (tähtkujude tõusu ja loojumise) põhjus on muidugi Maa pöörlemine. Päikese ja Kuu päevaseid teekondi üle taevavõlvi võib samuti lihtsa mudeli raames vaadelda Maa pöörlemise peegeldusena. Täpsem ja pikaajalisem vaatlus tekitab siiski küsimusi taevakehade tegelikest trajektooridest ja liikumise põhjustest, siin jääb näiva liikumise mudel hätta.
Antiikajast pärineb Ptolemaiose maailmasüsteem, mis pidas vastu sajandeid. Maa oli liikumatu, taevaskera oli reaalne tähtedega kaetud kera ja seitse astroloogilist planeeti (Päike, Kuu, Marss, Merkuur, Jupiter, Veenus, Saturn) liikusid selle sees üsna keerukaid mitmetest ringjoontest koosnevaid orbiite mööda. 16. sajandiks kogunes planeetide kohta üha enam ja üha täpsemaid vaatlusandmeid ja taevaste liikumiste mudel kippus minema juba ülearu keerukaks. Kuigi idee sellest, et Maa võib tiirelda ümber Päikese, oli välja öeldud juba Antiik-Kreekas, ei pööratud sellele eriti tähelepanu enne, kui Mikołaj Kopernik oma heliotsentrilise süsteemi avaldas. Koperniku järgi on maailma keskpunkt Päike. Maa on gravitatsiooni ja Kuu orbiidi keskpunkt. Planeetide orbiidid koosnevad ringidest või sfääridest. Koperniku süsteem meeldis astronoomidele, sest klappis vaatlusandmetega Ptolemaiose omast lihtsamalt, kuigi mitte täpsemalt. Tänapäeval lausa revolutsiooniliseks peetavat Päikese keskpunkti seadmist ja Maa liikumapanemist ei võetud siiski väga kiiresti omaks. Nagu teadusloos juhtub, tuli oodata uut põlvkonda ja vaatluslikke kinnitusi. Kõik see jõudiski 17. sajandil.
Kerakujuliste taevakehade ja ringorbiitide aksioomi autoriks peetakse Platonit ja selles ei kahelnud keegi enne, kui Saksa astronoom Johannes Kepler pikkade arvutuste ja korduva ebaõnnestumise järel pani kirja orbiitide kuju ja planeetide liikumise iseärasusi kirjeldavad reeglid, mida nüüd tuntakse kolme Kepleri seadusena. Arvutuste aluseks olid Taani astronoomi Tycho Brahe vaatlusandmed. Brahe ja Kepler olid korduvalt tülis nii andmete kasutamise kui ka maailmasüsteemi üldiste põhimõtete pärast. Mõlemad mõistsid ometi, et koostöö võib olla viljakas. Surivoodil pärandaski Brahe oma teleskoobieelse aja kohta erakordselt täpsed vaatluspäevikud Keplerile. Analüüs ja arvutused kestsid aastaid ja kuna ükski variant ei sobinud, loobus Kepler sfääridest, geomeetriliste kujunditega sobitamisest ja ka ringikujulistest orbiitidest. Ta oli päris lähedal gravitatsiooni mõistmisele, eeldades, et planeetide teekonda kujundav jõud tuleneb Päikesest ja väheneb kaugusega.
Hiljem tõestas Newton, et Kepleri seadused on tuletatavad gravitatsiooniseadusest ja üldistest liikumisseadustest (Newtoni seadustest) ning kirjeldavad gravitatsioonilist liikumist piisava täpsusega juhul, kui üks keha on teisest väga palju suurem. Planeetide massid ongi võrreldes Päikesega tühised.
Inimesed tunnetavad aega muutuste kaudu ja mõõdavad seda perioodiliste nähtuste abil. Enne tehniliste vahendite kasutusse võtmist sobisid pikemate ajavahemike üle arvestuse pidamiseks aastaaegade vaheldumine ja Kuu faasid. Lühemaid aegu aitab arvestada ööpäev. Jagamisel saab veel pisemaid ühikuid – tunde ja minuteid, neile taevast vastet pole ja siitmaalt muutub aja mõõtmine tehniliseks probleemiks, mida aitavad lahendada võnkuvad kehad.
| Joonis 3.5.1. Kalendrid jagavad mitmesugust infot ja tihtipeale kaunistavad meie ruume. Lisaks nädalapäevade ja kuupäevade kokkuviimisele võib kalendriruutudest leida Päikese tõusu ja loojumise ajad, Kuu faasid ning tähtpäevad. Sinna võib igaüks kirjutada endale olulisi sündmusi ja meeldetuletusi. Kliki ja loe pikemalt. | Joonis 3.5.2. Päikesekell ei ole linnainimese minutipealt kiirustavas ja sekundituhandikke hindavas igapäevas enam praktiline ajamõõdu vahend. Pigem on tegu meelelahutuse, aiakaunistuse ja astronoomia õppevahendiga. Päikesekellade valmistamiseks on palju viise, aga tegelikult võib kannatlik vaatleja päikesekellana võtta igapäevast elukeskkonda, näiteks kuurikatuse varju õuemurul. Kliki ja loe pikemalt. |
Ajaarvestuse ajalooliseks aluseks on keskmine päikeseööpäev. Ööpäeva loetakse keskööst, kui Päike läbib taevameridiaani näiva teekonna madalaimas punktis, kuni järgmise keskööni. Tõelised ööpäevad ei ole võrdsed, aga igapäevaselt on mugavam arvutada nagu oleks ja kasutada keskmist päikeseaega. Pikaajaliselt ajabilanss klapib, aga igal kindlal ajahetkel võib keskmine aeg tõelisest päikeseajast erineda.
Tänapäevased kellad kasutavad küll ajaloost pärinevat ööpäeva mõistet, aga tegelikult liidetakse see kokku aatomikellade sekunditest. Alates 1972. aastast on maailmaajana kasutusel UTC (inglise keeles - Universal Time Coordinated), mis asendab varasemat Greenwichi keskmist päikeseaega (GMT - Greenwich Mean Time). Maakera pöörlemise ebaühtlase aeglustumise tõttu läheb aatomikellade ööpäev päikeseööpäevast lahku. Tekkivat lahknemist on vajadust mööda korrigeeritud lisasekunditega.
Päikesesüsteem algab igas mõttes Päikesest. Umbes 99,86% Päikesesüsteemi massist on Päike. Päikese läbimõõt on 1 390 000 000 m, mass 1,99·1030 kg. Suuruselt teine on Jupiter, mass 1047 korda, läbimõõt 9,7 korda Päikesest väiksem. Päikesesüsteemis ei ole kehi, mida saaks mugavalt Päikesega võrrelda, pigem on meile sobiv võrdlus Maaga. Planeete ja nende kaaslasi kirjeldades kasutatakse ühikuna Maa massi ja läbimõõtu. Kaugusi mõõdetakse astronoomilistes ühikutes. 1 aü ehk AU on Maa keskmine kaugus Päikesest, 2012. aasta kokkuleppe järgi 149 597 870 700 meetrit ehk umbes 150 miljonit kilomeetrit.
Päikesesüsteemi suuremad kehad on Päike, planeedid koos mõne suurema kaaslasega, suurim asteroid ja tuntuim kääbusplaneet. Planeetide läbimõõdud tuhandetes kilomeetrites (Mm-megameeter) ja võrdluses Maaga, orbiidid miljonites kilomeetrites (Gm-gigameeter, kaaslastel Mm) ja astronoomilistes ühikutes (aü-Maa keskmine kaugus Päikesest). Planeetide orbiitide mõõdud on keskmised kaugused Päikesest, kaaslastel keskmised kaugused planeedist, Päikesel kaugus galaktika keskmest (kly-kaugus tuhandetes valgusaastates). Vaata tabelit.
Päikesesüsteemi planeedid tiirlevad peaaegu ühes tasandis. Kuiperi vöö kääbusplaneetide orbiidid võivad olla selle suhtes kaldu ja väga ekstsentrilised. Kogu Päiesesüsteemi ümbritseb veel arvatavalt Päikesest 50 000 aü kaugusele ulatuv ligikaudu sfääriline jäistest kehadest koosnev Öpiku-Oorti pilv.
Päikesesüsteemi suurust ei ole lihtne määrata. Piiri võib tõmmata Päikesest lugedes viimase planeedi juurde, aga planeedid ei ole ainsad kehad Päikesesüsteemis. Kaugeim planeet on Neptuun, keskmiselt 2,87 miljardi kilomeetri kaugusel. Pluto, mis kandis aastakümneid kaugeima planeedi auväärset tiitlit, liigub ekstsentrilisel orbiidil keskmise kaugusega Päikesest 5,91 miljardit kilomeetrit, 39,5 korda kaugemal kui Maa. Praegu loetakse Pluto kääbusplaneediks, sarnaseid leidub sealkandis teisigi. Nende tiirlemispiirkonda nimetatakse Kuiperi vööks. Nimesid on otsitud mitmete rahvaste legendidest ja uskumustest: Eris, Sedna, Quaoar, Makemake, Haumea. Kõigile ei ole nimesid pandud, näiteks esimene pärast Plutot avastatud kääbusplaneet kannab tänaseni tähistust (15760) 1992 QB1. Kuiperi vööd võib mõnes mõttes pidada Päikesesüsteemi äärealaks.
Päikesesüsteemi piiri võib panna ka sinna, kus lõpeb Päikese mõju. Valgus ja gravitatsiooniväli nõrgenevad kauguses ja kuigi nende ulatus on lõputa, hakkab kusagil teiste tähtede mõju domineerima. Vaevalt et piiri tegelikult nii kaugele tasub venitada. Teisiti on magnetväljaga. Ka see ulatub lõpmata kaugele, aga siin tuleb arvestada laetud osakeste liikumist. Päikesest lähtuv osakestevoog, päikesetuul, „puhub” läbi planeetidevahelise ruumi gaasi ja tolmu, aeglustub ja kohtub arvatavasti umbes 110 astronoomilise ühiku kaugusel Päikesest tähtedevahelise kiirguse, ioonide, gaasi ja tolmuga. Enamasti peetakse just seda Päikesesüsteemi servaks, heliosfääri piiriks. Sinnakanti on jõudnud mõned 1970-ndatel startinud kosmosesondid. Kõige kaugemale jõudnud Voyager 1 startis 1977, möödus Neptuunist ja jõudis planeetide alast välja 1989. 2012 ja 2013. aasta andmete alusel võib lõpuks öelda, et Voyager 1 on tõesti lahkunud heliosfäärist ja on esimene inimeste valmistatud seade, mis jõudnud tähtedevahelisse ruumi. See ei ole sugugi reisi lõpp. Umbes 300 aasta pärast peaks Voyager jõudma Öpiku-Oorti pilve, kust pärinevad Päikesesüsteemi külastavad pikaperioodilised komeedid. Pilve läbimiseks kulub arvatavalt 30 000 aastat. Kahjuks ei jätku elektrienergiat Maaga sidepidamiseks kauem kui aastani 2025.
| Joonis 3.6.2. Päikesesüsteemi neli sisemist planeeti on Maaga ühte tüüpi, pisikesed, aga suure tihedusega, koosnevad metallidest ja kivimitest. Samas on nad väga erinevad. Kliki joonisel ja loe edasi. | Joonis 3.6.3. Maasarnastel planeetidel pole kuigi palju kaaslasi. Kuu on suur erand, mõõtmete ja koostise poolest oleks ta kindlasti viies maasarnane planeet, kui tiirleks ümber Päikese. Tõsised kaaslaste pilved tiirlevad suurte gaashiidude (jupiterisarnaste planeetide) ümber. Neli Jupiteri suuremat kaaslast – Io, Europa, Ganymedes ja Callisto – avastas Galilei oma esimeste teleskoobivaatlustega (ptk Astronoomia). Hiljem on leitud suur hulk pisikaaslasi, kokku on neid koos 2012. aasta täiendusega nimekirjas 67. |
| Joonis 3.6.4. Iga planeet on omamoodi eriline, Saturn tõuseb esile oma ilusa rõngaga. Rõngas, täpsemal uurimisel rõngad, ei ole Maalt alati vaadeldavad. Vahel on nad meie poole serviti ja pole üldse näha. Arvestades suurust (tiheda põhiosa läbimõõt üle 270 000 km), on rõngad silmapaistavalt õhukesed, erinevates kohtades ja erinevatel hinnangutel 10 m kuni kilomeeter. Rõngad, mis jäävad pildile kui tervikobjektid, koosnevad tegelikult lugematust arvust pisikestest kehadest. Väiksemad on tolmukübeme mõõtu, suuremad kuni 10-meetrised. Kliki joonisele ja loe edasi. | Joonis 3.6.5. Tunnustatuim mudel kirjeldab planeetide teket akretsioooni kaudu. Pisikesed tolmukübemed koonduvad suuremateks klompideks, mis omavahel ühinedes kasvavad väiksemate kehadega põrkudes miljonite aastatega üha suuremaks. Sisemised planeedid tekivad kuumas piirkonnas, kus kergemad ühendid nagu vesi, ammoniaak ja metaan ei saa kondenseeruda. Tekivad kivised ja metalle sisaldavad planeedid. Kauges ja külmas piirkonnas on vesinikuühendite kondenseerumine võimalik. Tekivad suured gaasplaneedid, mis koguvad endasse vesinikku ja heeliumi. Kliki pildile ja loe edasi. |
Esimesed eksoplaneedid avastati 1992. aastal, esimesed planeedid päikesesarnase tähe juures 1995. aastal. Leitud planeetide arv on kindlasti üle tuhande. 2014. aasta aprilli algul oli erinevates andmebaasides 1400 kuni 1800 planeeti ja üle 3500 planeedikandidaadi. Muidugi köidavad meid eelkõige maasarnased planeedid ja nende tingimused. On leitud planeete, mis tiirlevad oma tähe nn elatavas alas, st kaugusel, kus võib leiduda vedelat vett. 17. märtsi 2014 seisuga on teatatud ühest planeedist, mis lisaks on ka õiges mõõdus, et kandideerida Maa kaksiku nimele. Kahjuks ei ole esialgu teada Kepler-186f nime kandva kandidaadi mass. Kuigi eksoplaneetide kohta on kogunemas rohkelt andmeid, ei ole praegu siiski võimalik öelda, millistel neist saaks areneda või on arenenud elu. Kosmobioloogidel ja kosmokeemikutel peaks siin olema oma kaalukas sõna öelda. Uurimismeetodid arenevad väga kiiresti, juba on kandidaatide hulgas ka eksoplaneetide kaaslased, nn eksokuud. Elu, eelkõige mõistusliku elu otsimisega kosmosest tegeleb SETI (Search for Extraterrestrial Intelligence), mida Ameerika Ühendriikides mõnda aega ka riiklikult finantseeriti. Esialgu midagi leitud ei ole.
Päikesesüsteem koosneb Päikesest ja planeetidest. Planeetidel võivad olla kaaslased ja rõngad. Tõepoolest, oluline osa Päikesesüsteemist on sellega nimetatud, aga vähegi täpsem vaatlus näitab, et meie kodune planeedisüsteem sisaldab veel palju huvitavaid ja potentsiaalselt ohtlikke või kasulikke kehi. Väikekehade liigitamine ja nimetamine võib ajaloolistel ja keelelistel põhjustel osutuda üsna keerukaks. Rahvusvaheline Astronoomia Liit (IAU) korrastab ja selgitab taevakehade nomenklatuuri, mis ei takista nii professionaalseid kui ka harrastusastronoome kasutamast harjunud nimetusi. Isegi planeedi definitsioon, mille IAU kehtestas 2006. aastal, on endiselt vaidlusteema. Igal juhul tasub peale Päikese, planeetide ja nende kaaslaste nimetada järgmisi:
- Väikeplaneedid, asteroidid, planetoidid, kääbusplaneedid (nimetused osaliselt kattuvad) ja nende kaaslased.
- Komeedid.
- Meteoorkehad (meteoroidid) ja meteoriidid.
- Planeetidevahelise ruumi tolm, osakesed, päikesetuul ja kiirgus.
| Joonis 3.7.1. Marsi ja Jupiteri orbiitide vahel tiirleb hulk väikeplaneete. Neid nimetatakse asteroidideks ja nende piirkonda asteroidide vööks. Kliki joonist ja loe edasi. | Joonis 3.7.2. Kuulsaim planeet – kääbusplaneet – on kahtlemata 1930. aastal avastatud Pluuto. Kääbusplaneetide koguarv Päikesesüsteemis ei ole teada, sest Neptuunist kaugemaid alasid pole kuigi põhjalikult uuritud. Kliki joonist ja loe edasi. |
| Joonis 3.7.3. Komeetidena tuntakse Päikese lähedale sattunud jääst, tolmust ja väikestest kivimitükkidest kehi, mis päikesekiirguses aurustuvad ja lagunevad. Tekkinud auru- ja tolmupilv kandub päikesetuules eemale ja moodustab komeedi saba, sellest on pärit ka tuntud sabatähe nimetus. Kliki joonisel ja loe pikemalt. | Joonis 3.7.4. Päikesesüsteemis tiirleb päris suur hulk väga pisikesi meteoorkehi ehk meteoroide. Meteoorkehade suurus võib olla tolmukübemest või liivaterast kuni mõne meetrini. Suure kiiruse tõttu on isegi väikesed terakesed ohtlikud kosmosetehnikale. Kliki pildil ja loe pikemalt. |
Kaasaegsele astronoomiale ja kosmoloogiale on olulist mõju avaldanud 20. sajandi teisel poolel alanud ja plahvatuslikult arenenud kosmoseajastu. Arvestades Teise maailmasõja järgseid rahvusvahelisi suhteid ja tehnoloogilist võidujooksu, on kosmoselennud, -tehnoloogia ja teadusuuringud tihedalt seotud rekordite püstitamise ja küsimusega, „kes jõudis esimesena?”
- Esimene Maalt startiva keha orbitaalse liikumise matemaatiline kirjeldus – sir Isaac Newton, Printsiibid, Newtoni kahur, 1687.
- Esimene kosmoselifti idee – Konstantin Tsiolkovski, 1895.
- Esimene raketiteadlane – Konstantin Tsiolkovski, reaktiivaparaatidega kosmilise ruumi uurimise artikkel, 1898 (ilmus 1903).
- Esimene vedelkütusega rakett – Robert Goddard, 1927. Goddard oli paljudes asjades esimene, nende hulgas on mitmeastmeline rakett, güroskoopidega stabiliseerimine, mõõteriistadega raketikatsetus jpm.
- Esimesed kosmoseprogrammide juhid – Verner von Braun, saksa raketiteadlane Teise maailmasõja ajal, hiljem Ameerika Ühendriikide armees, 1960–1970 NASA direktor; Sergei Koroljov, Nõukogude Liidu raketikonstruktor ja kosmoseprogrammide juht, alustas raketiteadusega vangilaagris, oli veel aastaid pärast surma salastatud isik.
- Esimene Maa tehiskaaslane – Sputnik (kaaslane), Nõukogude Liit, 4. oktoober 1957.
- Esimene vaade Kuu tagaküljele – nõukogude automaatseade Luna-3, 7. oktoober 1959, vahetu pilgu Kuu tagaküljele heitsid Apollo 8 pardalt USA astronaudid, 21. detsember 1968.
- Esimene elusolend orbiidil – Nõukogude kosmoseprogrammi koer Laika jõudis orbiidile Sputnik-2-ga, ta pidas ametlikel andmetel vastu mõned päevad, aga võimalik, et vaid mõned tunnid, 3. november 1957.
- Esimesed kosmosest elusalt tagasipöördujad – Belka ja Strelka, nõukogude kosmosekoerte programmi suurim õnnestumine 19. august 1960. Strelka sai hiljem 6 kutsikat, kellest üks kingiti USA president JF Kennedyle.
- Esimene gammateleskoop orbiidil – NASA satelliit Explorer 11, aprillist novembrini 1961.
- Esimene inimene kosmoses – Juri Gagarin, 12. aprill 1962.
- Esimene väljumine avakosmosesse – Aleksei Leonov, 18. märts 1965.
- Esimene maandumine Kuul –Nõukogude kosmosesond Luna-2 jõudis esimese Maalt pärit esemena Kuule 14. septembril 1959, esimese pehme maandumise ja pildid Kuu pinnalt tegi Luna-9 3. veebruaril 1966.
- Esimene inimene Kuul – Apollo 11 maandus Kuul, 20. juuli 1969 kell 20:17:40 UTC. Neil Armstrong astus vasaku jalaga Kuu pinnale 21. juulil kell 02:56:15 UTC.
- Esimesed kuukivimid Maal – Apollo 11 astronaudid tõid Maale 22 kg kuukivimeid, enne seda olid nõukogude automaatjaamade katsed ebaõnnestunud. Esimese täiesti automaatselt võetud 101 grammise proovi tõi Kuult Luna 16 1970. aastal.
- Kõige kaugemal käinud inimesed – Ameerika kuuprogrammi avarii tõttu katkestatud lend Apollo 13 käis siiski Kuu taga ära ja kuna orbiidile polnud võimalik jääda, said neist Maalt kõige kaugemale jõudnud inimesed, 14. aprill 1970, 400 171 km Maast.
- Esimesed uurimisrobotid Marsil – nõukogude jaam Mars-3 maandus Marsil ja jõudis töötada 14,5 sekundit, 2. detsember 1971 kell 13:52 UTC. NASA Viking 1 ja 2 maandusid Marsil 1976 ja töötasid mitu aastat.
- Esimene automaatjaama maandumine Päikesesüsteemi välisosas – satelliidiga Cassini välja saadetud sond Huygens laskus Saturni kaaslasele Titanile, 14. jaanuar 2005.
- Kõige kaugemale jõudnud kosmoseaparaat – Voyager 1, 6. mail 2014 127,7 astronoomilist ühikut Päikesest, kaugenemise kiirus 17 km/s.
- Kõige sügavam vaade Universumi avarusse – Hubble’i kosmoseteleskoop XDF, vaade minevikku ligi 13 miljardi aastat. Kokkuvõte 10 aasta kaadritest avaldati 2012.
Eesti seosed kaasaegse astronoomia ja kosmoseuuringutega on kiiduväärselt tihedad ja pikaajalised. Olulisi seoseid teadusliku astronoomiaga võib välja tuua alates 19. sajandi algusest. Nimetamist väärivaid kohti, inimesi ja sündmusi on kahe sajandiga kogunenud päris pikk rida:
- 1810. aastal rajatud Tartu Tähetorn ja 1824. aastal paigaldatud suurepärane teleskoop võimaldasid F.G.W. Struvel määrata 1837. aastal Vega kauguse.
- Kundast pärit, Moskvas õppinud Eesti astronoom Ernst Öpik määras 1922. aastal oma meetodil Andromeda kauguse. 1930-datel ennustas ta komeedipilve paiknemist Päikesesüsteemi äärealal, uuris tähtede evolutsiooni, kinnitades, et tähtede kiirgus pärineb termotuumareaktsioonidest. Kahjuks pidi ta oma karjääri jätkama välismaal.
- Tartu Observatoorium viidi üle Toomemäelt Tõraverre 1964. aastal. Kosmoslendude ajastu oli just alanud ja Tõravere teadlased osalesid nõukogude kosmoseprogrammides vaatluste ja aparaadiehituse kaudu. Arendati sidemeid kosmoseteadlaste, -inseneride ja kosmonautidega.
- 1977. aastal Tallinnas toimunud teaduskonverentsil tutvustas Jaan Einasto galaktikate ja nende parvede ruumjaotustel põhinevat avastust, Universumi kärgstruktuuri. Tumeaine ja suurima kosmilise struktuuri avastuslugu on kokku võetud Einasto 2013. aastal ilmunud raamatus „Dark Matter and Cosmic Web Story”.
- Tartus ehitatud radiomeeter Faza töötas 1980-ndatel kuulsates orbitaaljaamades Saljut ja Mir.
Pisikeste kuubikujuliste nanosatelliitide ajastu andis võimaluse haridusliku ja teadusliku projekti ESTCube-1 käivitamiseks. Tudengisatelliit on andnud ainet paljudele teadusartiklitele ja selle toel on kaitstud teaduskraade. 7. mail 2013 orbiidile jõudnud satelliidi teaduslikus programmis on elektrilise päikesepurje komponendi katsetamine. ESTCube-1 on varustatud kaameraga. Esimene pilt Maast tehti 15. mail 2013, pildile jäid Vahemeri ja Sahara kõrb.
Hubble’i kosmoseteleskoop (HST - Hubble Space Telescope) ehk lihtsalt Hubble, on ilmselt tuntuim kosmiline vaatlusseade. Hubble’i projekti teoreetilise alguse võib ajalukku märkida aastakümneid enne tegelike kosmoselendude algust, kui suuri rakettmootoreid alles arvutati ja katsetati. 1968. aastal otsustas Ameerika Ühendriikide kosmoseagentuur (NASA) suure peegelteleskoobi Maa orbiidile viimise projekti käiku panna. Kosmoseastronoomia oli selleks ajaks juba tulemusi näidanud. Eelkõige oli orbiidilt mõõdetud Päikese, tähtede ja galaktikate ultraviolettkiirgust. Hubble’i nime sai rahvusvaheline teleskoobiprojekt 1983. aastal. Tegelik ehitus ja mitmesugused ettevalmistused kestsid paarkümmend aastat. Kosmosesüstikute programm, mille raames pidi ka teleskoop orbiidile jõudma, peatati vahepeal Challengeri katastroofi tõttu. Alles 1990. aasta märtsis tõsteti Hubble’i kosmosesüstik Discovery lastiruumist välja ja paigutati 612 kilomeetri kõrgusel orbiidile.
Mõne nädala jooksul selgus, et kuigi Hubble’i pildid on maapealsete teleskoopidega võrreldes väga head, ei ole võimalik saavutada planeeritud kvaliteeti. Uurimine näitas, et peapeegel oli vigane, täpsemalt 2,2 mikromeetri võrra liiga lame. Lõplikul poleerimisel kasutatud ülitäpses kontrollseadmes oli üks lääts paigaldatud 1,3 mm võrra valesti, seega oli saadud enneolematu 10-nanomeetrise täpsusega valesti poleeritud peegel. Kuigi NASA ja Hubble said mõneks ajaks ajakirjanduses ja popkultuuris naerualuseks, töötas Hubble algusest peale hästi, tegeldes nende ülesannetega, kus ilmnenud viga oli vähem häiriv.
Kohe pärast vea avastamist hakkasid astronoomid ja optikud otsima teleskoobi parandamiseks parimat lahendust. Orbiidil peeglit vahetada polnuks võimalik. Teleskoobi parandamiseks allatoomine olnuks liiga kallis. Otsustati valmistada lisaseadmed, millel oleks sama viga, mis peeglil, ainult „vastasmärgiga”. Hubble sai prillid ette 1994. aastal. Alates 2002. aastast on kõik uued seadmed varustatud oma korrigeeriva optikaga.
Hubble’i vaatlusandmete toel toimunud arengud astronoomias on muljetavaldavad. Kuigi tänapäeval Hubble’i tüüpi pikaajalist, vahetatavate seadmetega ja hooldatavat, Maa-lähedast optilist teleskoopi enam ehitama ei hakata, on selle mõju astronoomiale ja meie arusaamadele maailmast raske üle hinnata. Olgu siinkohal nimetatud ainult tähtsamad saavutused.
- Tsefeiidide (muutlike tähtede) kauguse mõõtmine, mis andis võimaluse täpsustada Hubble’i konstanti ja arvutada Universumi paisumist.
- Supernoovade otsing kaugetes galaktikates, mis võimaldas määrata Universumi tumeenergiast tingitud kiireneva paisumise määra ja täpsustada Universumi vanust.
- Galaktikate keskmes asuvate mustade aukude tuvastamine.
- Komeedi Shoemaker-Levy 9 tükkide langemine Jupiterile toimus mõni kuu pärast korrigeeriva optika paigaldamist. Hubble andis erakordselt hea pildi haruldasest komeedi kohtumisest planeediga. – Hubble’i andmed on aidanud leida eksoplaneete ja tekkivaid planeedisüsteeme (protoplanetaarseid kettaid).
- Hubble’i abil on vaadeldud kääbusplaneete Pluto ja Eris. Muu hulgas on leitud Pluto viies pisikaaslane.
- Arvatavasti tuntuimad Hubble’i saavutused on 1995. aastal tehtud Universumi süvavaade (HDF - Hubble Deep Field) ja 2003–2004 tehtud ülisügava välja vaade (HUDF - Hubble Ultra Deep Field). HUDF on kokku pandud 800 kaadrist, ja summaarset säriaega on üle 106 sekundi. Pisikesest taevaalast, vaid kümnendik täiskuu läbimõõdust, leiti üle 10 000 galaktika. 2012. aastal avaldati veel eriti sügav vaade Universumi kaugustesse (XDF - Hubble eXtreme Deep Field). See pandi kokku kümne aasta kaadritest, säriaeg on kokku umbes 23 päeva. Kuigi vaatlusala on veidi väiksem, leiti sealt veel 5500 galaktikat. Hubble vaatab minevikku, me näeme kõige kaugemaid objekte sellisena, nagu nad olid vaid 800 000 aasta vanuses Universumis.
Hubble’i hind on hirmutavalt kõrge. Kogu projekti maksumuseks aastani 2010 on arvutatud umbes 10 miljardit dollarit. Kas Hubble tasub end ära? Arvatavasti ei too Hubble kunagi tagasi kulutatud dollareid, nagu ka paljud teised kosmoseprogrammid, aga me oleme saanud vaadata Universumit sügavamalt, kui keegi oskas oodatagi. Hubble’i tulevik on teadmata. Kui osade parandamist, lisamist või asendamist hooldusreisidel poleks toimunud, oleks arvatavasti kõik olulised seadmed juba rivist väljas. Viimane hooldus, osade vahetamine ja uute vaatlusseadmete paigaldus 2009. aastal, peaks tagama toimimise 2014. aastani ja loodetavalt kauemgi. Kui aga Hubble’i orbiiti ei korrigeerita, kukub see Maale mingil ajal 2019. ja 2032. aasta vahel. Täpne aeg sõltub atmosfääri seisundist, mis on omakorda seotud Päikese aktiivsusega. Kuigi suurem osa teleskoobist peaks atmosfääri sisenemisel ära põlema, võib mingi osa peapeeglist ja selle tugikonstruktsioonist jõuda maapinnani. Hubble’il ei ole päris otsest järeltulijat. Süvakosmose uurimisel peaks tööd jätkama James Webb (JWST - James Webb Space Telescope), mis asub tööle Maast hoopis kaugemas ja külmemas kohas. JWST suudab loodetvalt vaadata veelgi kaugemale kui Hubble. Tegu on põhiliselt infrapunase kiirguse mõõtmistega, nähtava valguse spektrist paistab punane ja oranž osa.
Tähed on hiigelsuured helendavad plasmakerad, mida hoiab koos tähe enda massist tingitud gravitatsiooniline tõmbejõud ja mille kiirguse allikaks on põhiliselt sisemuses toimuv tuumasüntees. Nad on väga kaugel ja paistavad meile seetõttu väikeste helenduvate täppidena. Tähed paistavad erineva heledusega ja terane vaatleja võib heades tingimustes märgata, et ka tähevalguse värvus on erinev.
| Joonis 3.9.1 Päikese ja teiste tähtede siseehitust vaadelda ega mõõta ei saa, mudel on arvutuslik. Päikese tuumas toimub kõrge temperatuuri (kuni 15 MK) ja suure gravitatsioonilise rõhu mõjul termotuumareaktsioon, vesinikust saab heelium (ptk Tuumareaktsioon). Kliki joonisele ja loe pikemalt. | Joonis 3.9.2. Fotosfääri alla tõusvate konvektsioonivoolude kohal on Päikese pinnal eredamad laigud, läbimõõduga umbes 1000 km. Kohad, kus veidi jahtunud gaas alla tagasi läheb, on tumedamad. Nii moodustub pulbitseva Päikese pinnale teraline ehk granuleerunud struktuur. Kliki joonisele ja loe pikemalt. |
Milline täht meile paistab, sõltub tema suurusest, temperatuurist ja kaugusest. Näiva heleduse mõõtühikuks on näiv tähesuurus. Tähtede suurusjärkudesse jagamise idee pärineb Vana-Kreeka astronoomidelt, kes jagasid neid kuude rühma. Mõned kõige heledamad on esimese tähesuurusega. Vaevumärgatavad, mida paljud inimesed üldse ei näe, on kuuenda suuruse tähed. Väiksem arv tähendab heledamat tähte. Sajanditega on süsteemi täpsustatud ja täiendatud. Tänapäevase süsteemi järgi on paar suuremat tähte esimesest tähesuurusest üle. Siriuse näiv tähesuurus on nähtavas valguses –1,45. Betelgeuse tähesuurus on nähtavas valguses 0,42 ja ühes infrapunakiirguse alas (J) –2,99. Esimesest tähesuurusest heledamad on ka Veenus, Marss ja Jupiter, rääkimata muidugi Päikesest ja Kuust.
Tegeliku heleduse kirjeldamiseks arvutatakse tähesuurused ümber, nagu oleksid tähed vaatlejast kõik võrdsel kaugusel 32,6 valgusaastat. Nii saadakse absoluutne tähesuurus, mis annab võimaluse tähtede tõelist heledust võrrelda. Tingimuseks on, et kaugused on määratavad ja kiirguse hajumine teel vaatlejani on teada – see ei pruugi alati nii olla.
Võrdleme kahte tuntud tähte: Vega Lüüras (kaugus 25 valgusaastat) ja Rigel Orionis (860 valgusaastat). Vega näiv heledus on 0,03, Rigelil 0,12. Vega näib heledam, aga mitte väga palju. Absoluutne tähesuurus on Vegal 0,58, Rigelil -7,84. Tegelikult on Rigel palju eredam täht, Vega paistab heledamana, sest on lähemal. Tähti võib võrrelda ja reastada ka massi, läbimõõdu ja tõelise heleduse järgi, enamasti kasutatakse ühikuks Päikest. Värvuse, st ühtlasi pinnatemperatuuri järgi jagatakse tähed kokkulepitud spektriklassidesse.
Tähtede areng on inimlikus mõõtkavas väga aeglane. Rahulikumad etapid kestavad miljardeid aastaid, kiiremaid muutusi saab mõõta miljonites aastates. Pole mingit võimalust, et astronoomid, isegi astronoomide põlvkonnad saaksid kindlaid tähti vaadeldes nende arengu välja uurida. Samas on võimalik vaadelda korraga väga paljusid tähti ja eeldada, et nende hulgas on nii nooremaid kui vanemaid. 20. sajandi algul koostasid kaks astronoomi, Ejnar Hertzsprung Taanis ja Henry Norris Russell Ameerikas sõltumatult paljude tähtede heledust (tõelist heledust võrreldes Päikesega) ja temperatuuri (värvust, spektriklassi) kirjeldava diagrammi. Vasakul üleval on näiteks kuumad (sinised) heledad tähed, all paremal jahedamad (punased) ja tuhmimad. Hertzsprungi-Russelli diagramm (H-R diagramm) näitab, et tähed ei saa olla ükskõik millised. Suurem osa tähtedest koondub diagrammi keskosas peajadasse, seal on ka Päike. Selgelt eristuvad hiidude, ülihiidude ja kääbuste jadad. Tähed on suurema osa oma elueast peajadal „põletades” vesinikku heeliumiks. Kui termotuumareaktsioon hakkab lõppema, läheb täht üle teise piirkonda nii kiiresti, et sellele on raske peale juhtuda. Päikegi lahkub 4,5 miljardi aasta pärast peajadalt ja muutub suhteliselt kiiresti (võrreldes kogu elueaga) punaseks hiiuks ja seejärel valgeks kääbuseks. Mõnede tähtede arengus on vägagi tormilisi etappe, lausa plahvatusi, mida mõõdetakse päevades. Supernoovadena plahvatavatest tähtedest pääseb välja tuumasünteesis tekkinud raskemaid elemente, millest uute tähtede tekkel võivad moodustuda planeedid, sh Maa tüüpi planeedid. Supernoovad on teadolevalt ainus viis, kuidas saavad tekkida rauast raskemate elementide tuumad (ptk Tuumareaktsioon).
Tähtede sünd ja saatus on seotud massiga. Supernoovadena plahvatavad Päikesest suurema massiga vanad tähed ja kaksiktähed, kus üheks paariliseks on valge kääbus. Kui täheks koonduvat ainet on alla 8% Päikese massist, ei käivitu napi siserõhu tõttu termotuumareaktsioon ja tekib pruun kääbus.
Päikesest suuremad tähed võivad lõpetada arengu mustade aukudena. Kui tuumarektsioonid lõpevad, saab otsa ka kiirguse ja gravitatsiooni vaheline tasakaal. Täht paiskab suure osa oma välisosast eemale, mis alles jääb, variseb gravitatsioonilise tõmbumise tõttu kokku. Kui allesjäänud mass koondub väiksesse ruumipiirkonda nn sündmuste horisondi sees, ei pääse sealt enam midagi välja ja tihedus kasvab ülisuureks. Kui näiteks kogu Maa massi saaks suruda alla 2 cm läbimõõduga keraks, tekiks must auk. Musta auku langeb kogu kiirgus, sh valgus, mis liiga lähedale satub. Seepärast ei saa must auk peegeldada ega tavalise kehana kiirata ja teda pole näha. Mustad augud annavad endast märku neisse langeva aine kiirgamise ja taustal oleva pildi gravitatsioonilise moonutuse (gravitatsiooniläätse) kaudu. Teoreetiliselt on mustadel aukudel siiski võimalusi kiirgamiseks. Kuigi see kiirgus on väga nõrk ei pruugi nad olla igavesed aine ja kiirguse neelajad.
Selgel, pimedal ööl, suurlinnade valguskumast eemal on kerge märgata, et üle taevalaotuse ulatub veidi haruline udune vööt. Nii paistab meile kodune Galaktika, mida meil on kombeks nimetada Linnuteeks. Paljudes keeltes ja paljude rahvaste müütides on selle nimi Piimatee (kreeka keeles galaxias - piimjas). Teleskoobivaatluste algus 17. sajandil (ptk Astronoomia) tegi üsna pea selgeks, et Linnutee koosneb suurest hulgast tähtedest, mida palja silmaga näha ei ole, aga mille valgus kokku sulades tundub taevase uduna. Alles 20. sajandil viis vaatlustehnika areng mõistmiseni, et galaktikaid, suuri gravitatsiooniliselt seotud tähtede, gaasi, tolmu ja tumeaine süsteeme, on Universumis palju.
Peale Linnutee tähtede on taevas palja silmaga näha veel kolm galaktikat. Heades tingimustes paistab Andromeda tähtkujus hele udune laik, Andromeda udukogu, galatika M31. Andromeda ja Linnutee on üsna sarnased spiraalsed galaktikad. Lõunapoolses taevas võib leida veel kaks korrapäratut kääbusgalaktikat, Suure ja Väikese Magalhãesi pilve.
Teleskoopidega, eriti kosmoseteleskoopidega, on leitud ja pildistatud tuhandeid galaktikaid. Galaktikate koguarvu on raske öelda, kindlasti on neid üle 100 miljardi. Meie vaatlusvõime on siiski piiratud ja arvatakse, et galaktikaid võib olla isegi 500 miljardit kuni triljon. Galaktikate suurus, kuju ja tähtede liikumine neis võib olla väga erinev. Ilusad pöörlevad spiraalgalaktikad nagu Linnutee ja Andromeda paistavad olevat vähemuses, palju on kääbusgalaktikaid.
Ernst Julius Öpik, väljapaistev Eesti astrofüüsik, õppis astronoomiat Moskva ülikoolis ja töötas paar aastat Taškendis. Keerulistel aegadel Venemaalt Eestisse tagasi jõudnud, sai doktorikraadi Tartu ülikkoolis ja töötas 1921. aastast Tartu observatooriumis, mõned aastad vahepeal Harvardis, oli sunnitud Eestist lahkuma aastal 1944. Pärast põgenikuna Saksamaal veedetud aastaid ja tööd Balti ülikoolis professori ning eesti rektorina, asus ta 1948 Põhja-Iirimaale Armagh observatooriumi, kus töötas aastani 1981.
Öpik oli väga mitmekülgsete huvidega astrofüüsik. 1916. aastal Moskvas õppides avaldas ta teadusliku artikli, kus leidis, et valgete kääbuste hulka kuuluva tähe tihedus paistab olevat 25 000 korda suurem kui Päikese tihedus. Tänapäeval kirjeldavad populaarsed astronoomiaõpikud valgete kääbuste tihedust näitega, et neis on Päikese mass või veidi enamgi koondunud maakera ruumalasse. See teeb tiheduseks umbes 1000 tonni kuupsentimeetri kohta. Pole imestada, et Öpik ja kõik astrofüüsikud tol ajal pidasid seda võimatuks.
1922. aastal ilmus Öpiku artikkel, kus ta esitas Andromeda galaktika kauguse määramiseks oma meetodi ja kasutades sel ajal teadaolevaid andmeid, arvutas kauguse täpsemalt kui suudeti järgnevatel aastakümnetel teiste meetoditega.
1915. aastast arendas Öpik tähtede evolutsiooni teooriaid. Ta jõudis järeldusele, et tähtedes toimuvad termotuumareaktsioonid. 1938. aastal kirjeldas ta Päikese arengut ja tulevikku nii, nagu seda praegu peetakse üldtunnustatud õpikutarkuseks.
1932. aastal ennustas Öpik, et Päikesesüsteemi ümbritseb komeedipilv. Seda väheuuritud ala, mida võib lugeda Päikese mõju kõige viimaseks ääreks, nimetatakse nüüd Öpik-Oorti pilveks.
Öpiku huvid olid väga laialdased ja hõlmasid ka astronoomiaväliseid teemasid. Juba noorena köitsid teda Päikesesüsteemi väikekehad, asteroidid, meteoorid ja komeedid. Ta ennustas meteoriidikraatreid Marsil ja Veenuse atmosfääri omadusi, püüdis Päikese tuumareaktsioonide järgi põhjendada jääaegade perioodilisust. Muu hulgas esitas ta ka tänapäevases mõttes veidraid seisukohti, näiteks päikeseplekkide seotusest poliitiliste pööretega ühiskonnas ja Marsi taimestikust. Ernst Öpik oli ka pianist ja tegeles heliloominguga.
Öpiku nime kannavad asteroid ja kraater Marsi kaaslasel Phobosel.
Suure Paugu teooria on tänapäeva kosmoloogias valitsev Universumi arengu kirjeldamise mudel. Kuigi Suur Pauk on hüpoteetiline sündmus, millel pole midagi pistmist kõigi meile tuntud paukudega, klapib see teooria praegu kõige paremini väga suure hulga erinevate vaatlusandmetega.
Suure Paugu teooria juured ulatuvad antiik- ja keskaegsesse filosoofiasse. Kosmoloogias algasid teaduslikult eriti huvitavad ajad 20. sajandi algul. 1916. aastal avaldas Albert Einstein üldrelatiivsusteooria. 1922. aastal tuletas Alexander Friedmann üldrelatiivsusteooriast Universumi arengut kirjeldavad võrrandid. Selgus, et Universumi paisumine on võimalik. Georges Lemaître avaldas 1927. aastal sõltumatult paisuva Universumi mudeli. 1929 avaldas Edwin Hubble vaatlusliku kinnituse Universumi paisumisele. 1931. aastal pakkus Lemaître välja, et Universum on paisunud algpunktist, mida ta nimetas Ürgaatomiks.
Universumi arengut kujutatakse tavaliselt ajakoonusena. Piki koonust kulgeb ajatelg. Koonuse läbimõõt kujutab Universumi suurust. Vasakul on nullpunkt, aja ja ruumi tekkimine kirjeldamatult väikese ja kirjeldamatult kuumana. Järgneb väga kiire paisumine ja jahtumine, kuni kiirgus saab hakata ruumis levima. Läheb veel mitusada miljonit aastat, kuni tekivad esimesed tähed ja galaktikad. Kiirgus jääb taustana alles ja kui ruum üha laieneb, suureneb selle lainepikkus.
Taustkiirguse, selle omaduste ja mõõdetavuse ideed arenesid alates 1940-ndatest. Mõõtmiseni jõuti 60-ndate keskel. Praeguseks on kosmilist mikrolaine taustkiirgust (CMBR cosmic microwave background radiation) ehk reliktkiirgust väga põhjalikult mõõdetud ja uuritud. Kiirgus vastab absoluutselt musta keha temperatuurile 2,73 K. Neid vaatlusandmeid peetakse tänapäeval koos Hubble'i seadusega kõige olulisemateks kinnituseks Suure Paugu teooriale. Kiirguse vabanemise eelsest ajast ei ole meil vaatlusandmeid. Alles 2014. aasta kevadel avaldati esimesed taustkiirguse polarisatsiooni mõõtmise andmed, mis arvatavasti kannavad kaudset infot inflatsioonilise paisumise ajast.
| Joonis 3.10.4. Uurides Linnutee tähtede liikumist, galaktikate pöörlemist, mustade aukude gravitatsioonilist toimet, gaasi jaotust galaktikates jpm suuri ning kaugeid asju, on kosmoloogid leidnud, et nähtava aine massist ei piisa nende nähtuste seletamiseks. Kliki joonisele ja loe pikemalt. | Joonis 3.10.5. Millest koosneb Universum? Sektordiagrammis on välja toodud põhiline sellele küsimusele vastamisel. Selgub, et olulise osa annavad tumeaine, tumeenergia, edasi tulevad vesinik ja heelium. Raskeid elemente on isegi vähem kui neutriinosid. Kliki joonisel ja loe pikemalt. |
Suure Paugu mudel kirjeldab Maailma tekkimist. Kõik algas umbes 13,8 miljardit aastat tagasi. Meil ei ole infot, millest see algas, aga seda on kombeks nimetada ürgaatomiks või singulaarsuseks. Kui Suur Pauk ise ei pruugi kirjelduda teadaolevate füüsikaseadustega, siis järgnevat võib siiski panna nii võrranditesse kui ka sõnadesse. Algul paisus Universum inflatsiooniliselt, st palju-palju enam kui kiiresti. Esimese kümne sekundiga toimus Universumis paljugi põnevat, mille kohta on teooriaid, aga pole esialgu kuigi palju vaatlusandmeid. Arvatavasti tekkisid pärast kümnendat sekundit prootonitest esimesed aatomituumad, heeliumi isotoobid, veidi deuteeriumi, liitiumi ja berüllimi tuumi.
380 000 aastaga oli Universum jahtunud umbes 3600 kelvinini. Elektronid ja prootonid moodustasid vesiniku aatomeid. Siis sai valgus levima hakata, kosmoloogid ütlevad, et kiirgus vabanes ja Universum hakkas läbi paistma. Tumeainest oli juba moodustunud suuremõõduline struktuur. Nüüd sai ka aine gravitatsiooni mõjul samades kohtades koonduma hakata. Moodustusid galaktikad ja tähed. Praegu teame, et galaktikad on koondunud kettidesse ja kihtidesse, mille vahel on hoomamatult palju tühjust. Nii on moodustunud Universumi kõige suurem struktuur, mida tihti nimetatakse kärgstruktuuriks, kuigi väga suurt sarnasust sel näiteks mesilaskärjega pole.
Linnutee galaktikas hakkas umbes 9 miljardit aastat pärast Suurt Pauku kosmilisest gaasist ja tolmust moodustuma uus täht, Päike. Kokkutõmbuv ja kuumenev gaasipilv haaras kaasa hukkunud tähtedest pärit aatomeid. Kui Päike oli end gravitatsioonijõuga piisavalt kokku surunud ja kuumenenud, algas termotuumareaktsioon. Osa täheainest, sh veidi aatomeid, mis vesinikust ja heeliumist raksemad, ei jõudnud Päiksesse koonduda, neist moodustus planeedisüsteem, nii nagu see juhtub paljude tähtede juures. Päikese kiirgus ja päikesetuul mõjutasid planeetide arengut. Kaugemad suured planeedid said rohkem kergeid elemente ja on gaasilised. Lähemad planeedid tulid kivised ja sisaldavad palju metalle.
Kui kivised planeedid olid väga kuumad ja põhiosas vedelad, sattus üks neist, Maa, kosmilise kokkupõrke osaliseks. Teine osaline oli väiksem ja hävis täielikult. Osa põrkel laiali paiskunud ainest moodustas Maale kaaslase, Kuu. Kuu on erandlik, erakordselt kaunis ja väärtuslik taevakeha. Pole tähtsusetu, et Kuud on tore vaadata. Täiskuu rõõmustab meid kuuvalgete öödega. Umbes kord kuus on Päike ja Kuu Maalt vaadates samas suunas. Siis pole Kuud üldse näha, sest vaatleja poole pööratud külg ei saa valgust. Öeldakse, et käib kuuloomine. Näiv muutumine kitsast sirbist täiskettaks ja tagasi on Maa loodusliku kaaslase eripära, mis on innustanud inimesi Kuu poole õhkama, Kuu peale lootma. On loodud legende Kuu tulemisest ja minemisest, on püütud oma elu ja tegevust Kuu faasidega kooskõlla viia.
Raske on ülehinnata Kuu osa loodusteadusliku meetodi kujunemisel. Küllap oli just Kuu esimene taevakeha, mida vaadati läbi pikksilma. Newtoni Printsiipide kirjutamise ajendiks oli Kuu trajektoori kirjeldamise probleem ja seal leiavad käsitlemist nii Kuu liikumise gravitatsioonilised häired kui ka loodelised nähtused. Kuu on ainus taevakeha, mida inimesed on jõudnud külastada ja kust on Maale kivimiproove toodud.
Arvatakse, et Kuul on olnud täita veel üks tähtis ülesanne. Maa ja Kuu vaheline gravitatsiooniline vastastikmõju tekitab loodelisi jõude. Ookeanide tõusud ja mõõnad on miljoneid aastaid loksutanud vett madalates rannikumeredes. Igal ringil deformeerib Kuu veidi maakoort, mõjutades laamtektoonikat, maavärinaid ja vulkanismi. Kõik see ja lisaks sobiv kaugus Päikesest on toitnud elurikkuse teket ja püsimist ning teinud Maast just selle, mis ta on – meie kodu.