Keemilise vooluallika põhiosadeks on negatiivne ja positiivne elektrood ning elektrolüüt. Elektroodide pinnal on elektrokeemiliselt aktiivsed ained, metallid või nende ühendid. Elektrolüüdiks on hapete, aluste ja soolade lahused või ioonvedelik.
Elektrokeemilised protsessid põhinevad redoksreaktsioonidel. Vooluallika negatiivsel elektroodil toimub elektrolüüdiga reageerides metalli oksüdeerumine ja elektronide loovutamine. Kui ühendada vooluallika klemmidega tarbija, siis elektronid hakkavad suunatult miinusklemmilt läbi tarbija pluss- klemmile liikuma, kus nad redutseeritakse. Näitena olgu toodud plii- ehk happeakus toimuv reaktsioon.
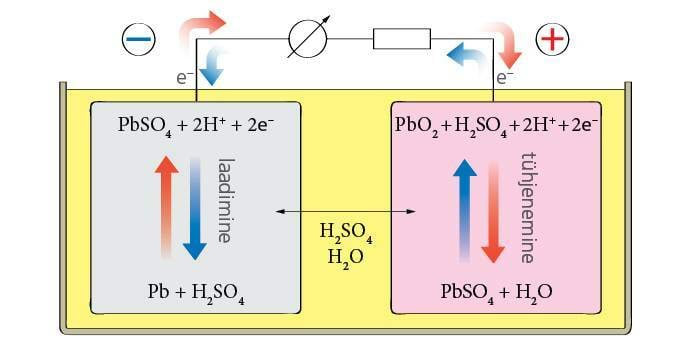
Laetud akus on ühel elektroodil peaaegu puhas plii ja teisel pliioksiid ning nende vahel väävelhappe ( vol) vesilahus (vt järgnev joonis). Tühjas akus seevastu on elektroodidel plii(II)sulfaat ja nende vahel vesi.
Peale happeakude on veel kasutusel mitmesugused leelisakud ja suhteliselt hiljuti leiutatud liitiumakud. Uuemaks tehniliseks rakenduseks on päikese- paneelid, kus kiirgusenergia muudetakse ventiilfotoefektiga vahetult elektrienergiaks, kuid paneelide hind on laialdaseks kasutuselevõtuks veel liiga kõrge.
Keemiliste vooluallikate põhilisteks näitajateks on elektromotoorjõud, nimipinge, sisetakistus, nimilaeng ehk mahutavus (), energiatihedus (Wh/kg), laadimise kasutegur ja säilivus (alles on nimilaengust).