Vahendid:
- Nõudepesuvahend
- Glütseriin
- Suur läbipaistev anum (umbes 2 l)
- kaltsiumkarbonaati (CaCO3) või söögisoodat (NaHCO3) ja vesinikkloriidhapet (HCl vesilahus) või ainult süsiniktetrakloriidi
- Suur kõrs
- Väike klaas
Protseduur:
1. Sega klaasi kokku 1 osa nõudepesuvahendit, 2.5 osa glütseriini ja 3 osa vett. Ole valmis kõrrega sealt üks mull puhuma.
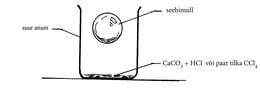
2. Pane suure anuma põhja natuke CaCO3 või söögisoodat, lisa HCl. Alternatiivina võib panna anuma põhja paar tilka CCl4.
3. Puhu üks mull ja lase sel rahulikult anumasse langeda.
4. Jälgi mulli (seda tuleb teha siseruumis, kus ei ole tuuletõmmet).
Selgitus CaCO3 või söögisooda reageerimisel HCl-ga tekib CO2. CCl4 aurustub anumas. Selle tulemusena on anuma põhjas õhust raskem gaas, mis ei saa sealt väljuda (see püsib anumas nii, nagu vesigi püsiks). Seebimulli tihedus on õhu tihedusest vaid veidi suurem ja seega on see CO2-st hõredam ja ujub selles. Samas on see gaas nähtamatu nagu õhkki ning on võimatu näha, kus on õhk ja kus gaas. Seetõttu jääb mulje, et mull lihtsalt hõljub.